From Wikipedia, the free encyclopedia
|
|
|
|

|
|
| Names | |
|---|---|
| Other names
Magnesite |
|
| Identifiers | |
|
CAS Number |
|
|
3D model (JSmol) |
|
| ChEBI |
|
| ChEMBL |
|
| ChemSpider |
|
| ECHA InfoCard | 100.008.106 |
| E number | E504(i) (acidity regulators, …) |
|
PubChem CID |
|
| RTECS number |
|
| UNII |
|
|
CompTox Dashboard (EPA) |
|
|
InChI
|
|
|
SMILES
|
|
| Properties | |
|
Chemical formula |
MgCO3 |
| Molar mass | 84.3139 g/mol (anhydrous) |
| Appearance | Colourless crystals or white solid Hygroscopic |
| Odor | Odorless |
| Density | 2.958 g/cm3 (anhydrous) 2.825 g/cm3 (dihydrate) 1.837 g/cm3 (trihydrate) 1.73 g/cm3 (pentahydrate) |
| Melting point | 350 °C (662 °F; 623 K) decomposes (anhydrous) 165 °C (329 °F; 438 K) (trihydrate) |
|
Solubility in water |
Anhydrous: 0.0139 g/100 ml (25 °C) 0.0063 g/100 ml (100 °C)[1] |
|
Solubility product (Ksp) |
10−7.8[2] |
| Solubility | Soluble in acid, aqueous CO2 Insoluble in acetone, ammonia |
|
Magnetic susceptibility (χ) |
−32.4·10−6 cm3/mol |
|
Refractive index (nD) |
1.717 (anhydrous) 1.458 (dihydrate) 1.412 (trihydrate) |
| Structure | |
|
Crystal structure |
Trigonal |
|
Space group |
R3c, No. 167[3] |
| Thermochemistry | |
|
Heat capacity (C) |
75.6 J/mol·K[1] |
|
Std molar |
65.7 J/mol·K[1][4] |
|
Std enthalpy of |
−1113 kJ/mol[4] |
|
Gibbs free energy (ΔfG⦵) |
−1029.3 kJ/mol[1] |
| Pharmacology | |
|
ATC code |
A02AA01 (WHO) A06AD01 (WHO) |
| Hazards | |
| NFPA 704 (fire diamond) |
1 0 0 |
| Flash point | Non-flammable |
| NIOSH (US health exposure limits): | |
|
PEL (Permissible) |
|
| Safety data sheet (SDS) | ICSC 0969 |
| Related compounds | |
|
Other anions |
Magnesium bicarbonate |
|
Other cations |
Beryllium carbonate Calcium carbonate Strontium carbonate Barium carbonate Radium carbonate |
|
Related compounds |
Artinite Hydromagnesite Dypingite |
|
Except where otherwise noted, data are given for materials in their standard state (at 25 °C [77 °F], 100 kPa).
Infobox references |
Magnesium carbonate, MgCO3 (archaic name magnesia alba), is an inorganic salt that is a colourless or white solid. Several hydrated and basic forms of magnesium carbonate also exist as minerals.
Forms[edit]
The most common magnesium carbonate forms are the anhydrous salt called magnesite (MgCO3), and the di, tri, and pentahydrates known as barringtonite (MgCO3·2H2O), nesquehonite (MgCO3·3H2O), and lansfordite (MgCO3·5H2O), respectively.[6] Some basic forms such as artinite (Mg2CO3(OH)2·3H2O), hydromagnesite (Mg5(CO3)4(OH)2·4H2O), and dypingite (Mg5(CO3)4(OH)2·5H2O) also occur as minerals. All of those minerals are colouress or white.
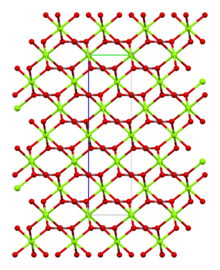
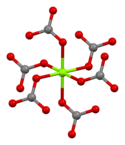
Magnesite consists of colourless or white trigonal crystals. The anhydrous salt is practically insoluble in water, acetone, and ammonia. All forms of magnesium carbonate react with acids. Magnesite crystallizes in the calcite structure wherein Mg2+ is surrounded by six oxygen atoms.[3]
| Carbonate coordination | Magnesium coordination | Unit cell |
|---|---|---|

|
|

|
The dihydrate has a triclinic structure, while the trihydrate has a monoclinic structure.
References to «light» and «heavy» magnesium carbonates actually refer to the magnesium hydroxy carbonates hydromagnesite and dypingite, respectively.[7]
Preparation[edit]
Magnesium carbonate is ordinarily obtained by mining the mineral magnesite. Seventy percent of the world’s supply is mined and prepared in China.[8]
Magnesium carbonate can be prepared in laboratory by reaction between any soluble magnesium salt and sodium bicarbonate:
- MgCl2(aq) + 2 NaHCO3(aq) → MgCO3(s) + 2 NaCl(aq) + H2O(l) + CO2(g)
If magnesium chloride (or sulfate) is treated with aqueous sodium carbonate, a precipitate of basic magnesium carbonate – a hydrated complex of magnesium carbonate and magnesium hydroxide – rather than magnesium carbonate itself is formed:
- 5 MgCl2(aq) + 5 Na2CO3(aq) + 5 H2O(l) → Mg4(CO3)3(OH)2·3H2O(s) + Mg(HCO3)2(aq) + 10 NaCl(aq)
High purity industrial routes include a path through magnesium bicarbonate, which can be formed by combining a slurry of magnesium hydroxide and carbon dioxide at high pressure and moderate temperature.[6] The bicarbonate is then vacuum dried, causing it to lose carbon dioxide and a molecule of water:
- Mg(OH)2 + 2 CO2 → Mg(HCO3)2
- Mg(HCO3)2 → MgCO3 + CO2 + H2O
Chemical properties[edit]
With acids[edit]
Like many common group 2 metal carbonates, magnesium carbonate reacts with aqueous acids to release carbon dioxide and water:
- MgCO3 + 2 HCl → MgCl2 + CO2 + H2O
- MgCO3 + H2SO4 → MgSO4 + CO2 + H2O
Decomposition[edit]
At high temperatures MgCO3 decomposes to magnesium oxide and carbon dioxide. This process is important in the production of magnesium oxide.[6] This process is called calcining:
- MgCO3 → MgO + CO2 (ΔH = +118 kJ/mol)
The decomposition temperature is given as 350 °C (662 °F).[9][10]
However, calcination to the oxide is generally not considered complete below 900 °C due to interfering readsorption of liberated carbon dioxide.
The hydrates of the salts lose water at different temperatures during decomposition.[11] For example, in the trihydrate MgCO3·3H2O, which molecular formula may be written as Mg(HCO3)(OH)·2H2O, the dehydration steps occur at 157 °C and 179 °C as follows:[11]
- Mg(HCO3)(OH)·2(H2O) → Mg(HCO3)(OH)·(H2O) + H2O at 157 °C
- Mg(HCO3)(OH)·(H2O) → Mg(HCO3)(OH) + H2O at 179 °C
Uses[edit]
The primary use of magnesium carbonate is the production of magnesium oxide by calcining. Magnesite and dolomite minerals are used to produce refractory bricks.[6] MgCO3 is also used in flooring, fireproofing, fire extinguishing compositions, cosmetics, dusting powder, and toothpaste. Other applications are as filler material, smoke suppressant in plastics, a reinforcing agent in neoprene rubber, a drying agent, and colour retention in foods.
Climber Jan Hojer blows surplus chalk from his hand. Boulder World Cup 2015
Because of its low solubility in water and hygroscopic properties, MgCO3 was first added to salt in 1911 to make it flow more freely. The Morton Salt company adopted the slogan «When it rains it pours», meaning that its salt containing MgCO3 would not stick together in humid weather.[12] Magnesium carbonate, most often referred to as «chalk», is also used as a drying agent on athletes’ hands in rock climbing, gymnastics, weightlifting and other sports in which a firm grip is necessary.[8]
As a food additive, magnesium carbonate is known as E504. Its only known side effect is that it may work as a laxative in high concentrations.[13]
Magnesium carbonate is used in taxidermy for whitening skulls. It can be mixed with hydrogen peroxide to create a paste, which is spread on the skull to give it a white finish.
Magnesium carbonate is used as a matte white coating for projection screens.[14]
Medical use[edit]
It is a laxative to loosen the bowels.
In addition, high purity magnesium carbonate is used as an antacid and as an additive in table salt to keep it free flowing. Magnesium carbonate can do this because it does not dissolve in water, only in acid, where it will effervesce (bubble).[15]
Safety[edit]
Magnesium carbonate is non-toxic and non-flammable.
Compendial status[edit]
- British Pharmacopoeia[16]
- Japanese Pharmacopoeia[17]
See also[edit]
- Calcium acetate/magnesium carbonate
- Upsalite, a reported amorphous form of magnesium carbonate
Notes and references[edit]
- ^ a b c d «Magnesium carbonate».
- ^ Bénézeth, Pascale; Saldi, Giuseppe D.; Dandurand, Jean-Louis; Schott, Jacques (2011). «Experimental determination of the solubility product of magnesite at 50 to 200 °C». Chemical Geology. 286 (1–2): 21–31. Bibcode:2011ChGeo.286…21B. doi:10.1016/j.chemgeo.2011.04.016.
- ^ a b Ross, Nancy L. (1997). «The equation of state and high-pressure behavior of magnesite». Am. Mineral. 82 (7–8): 682–688. Bibcode:1997AmMin..82..682R. doi:10.2138/am-1997-7-805. S2CID 43668770.
- ^ a b Zumdahl, Steven S. (2009). Chemical Principles 6th Ed. Houghton Mifflin Company. p. A22. ISBN 978-0-618-94690-7.
- ^ NIOSH Pocket Guide to Chemical Hazards. «#0373». National Institute for Occupational Safety and Health (NIOSH).
- ^ a b c d Margarete Seeger; Walter Otto; Wilhelm Flick; Friedrich Bickelhaupt; Otto S. Akkerman. «Magnesium Compounds». Ullmann’s Encyclopedia of Industrial Chemistry. Weinheim: Wiley-VCH. doi:10.1002/14356007.a15_595.pub2.
- ^ Botha, A.; Strydom, C.A. (2001). «Preparation of a magnesium hydroxy carbonate from magnesium hydroxide». Hydrometallurgy. 62 (3): 175. Bibcode:2001HydMe..62..175B. doi:10.1016/S0304-386X(01)00197-9.
- ^ a b Allf, Bradley (21 May 2018). «The Hidden Environmental Cost of Climbing Chalk». Climbing Magazine. Cruz Bay Publishing. Retrieved 22 May 2018.
In fact, China produces 70 percent of the world’s magnesite. Most of that production—both mining and processing—is concentrated in a small corner of Liaoning, a hilly industrial province in northeast China between Beijing and North Korea.
- ^ «IAState MSDS».
- ^ Weast, Robert C.; et al. (1978). CRC Handbook of Chemistry and Physics (59th ed.). West Palm Beach, FL: CRC Press. p. B-133. ISBN 0-8493-0549-8.
- ^ a b «Conventional and Controlled Rate Thermal analysis of nesquehonite Mg(HCO3)(OH)·2(H2O)» (PDF).
- ^ «Her Debut — Morton Salt». Retrieved 27 December 2017.
- ^ «Food-Info.net : E-numbers : E504: Magnesium carbonates». 080419 food-info.net
- ^ Noronha, Shonan (2015). Certified Technology Specialist-Installation. McGraw Hill Education. p. 256. ISBN 978-0071835657.
- ^ «What Is Magnesium Carbonate?». Sciencing. Retrieved 15 April 2018.
- ^ British Pharmacopoeia Commission Secretariat (2009). «Index, BP 2009» (PDF). Archived from the original (PDF) on 11 April 2009. Retrieved 31 January 2010.
- ^ «Japanese Pharmacopoeia, Fifteenth Edition» (PDF). 2006. Archived from the original (PDF) on 22 July 2011. Retrieved 31 January 2010.
External links[edit]
- International Chemical Safety Card 0969
- NIST Standard Reference Database
Магний углекислый технический

Международное название Magnesium carbonate
Синонимы Магний карбонат, Магниевая соль угольной кислоты, Магний углекислый
Формула: MgCO3
Нормативно-техническая документация ТУ 2144-027-05761270-2005
Внешний вид Порошок белого цвета
Оптовые поставки магния углекислого технического
Наш завод по производству химических реагентов, производит технический углекислый магний в любых объемах. Так же Вы можете заказать его доставку, в каком бы городе России Вы ни находились, товар дойдет в полной сохранности, т.к. мы используем тару только по ГОСТу.
| Показатели качества | |
| Наименование показателя | Требования ТУ |
| 1. Массовая доля магния (Mg), %, не менее | 24,5 |
| 2. Массовая доля нерастворимых в соляной кислоте веществ, %, не более | 1,0 |
| 3. Массовая доля серы общей (SO4), %, не более | 0,03 |
| 4. Массовая доля хлоридов (Сl), %, не более | 0,08 |
| 5. Массовая доля мышьяка (Аs), %, не более | 0,0002 |
| 6. Массовая доля тяжелых металлов (Рb), %, не более | 0,01 |
Работаем со всеми городами России
А
Абакан
Альметьевск
Анапа
Ангарск
Арзамас
Артём
Архангельск
Астрахань
Ачинск
Б
Балаково
Балашиха
Барнаул
Батайск
Белгород
Бердск
Березняки
Бийск
Благовещенск
Братск
Брянск
В
Великий Новгород
Владивосток
Владимир
Волгоград
Волгодонск
Волжский
Вологда
Воронеж
Д
Дзержинск
Дмитровград
Долгопрудный
Домодедово
Е
Евпатория
Екатеринбург
Елец
Ессентуки
Ж
Железногорск
Жуковский
З
Златоуст
И
Иваново
Ижевск
Иркутск
Йошкар Ола
К
Казань
Калининград
Калуга
Каменск-Уральский
Камышин
Кемерово
Керчь
Киров
Кисловодск
Коломна
Комсомольск На Амуре
Копейск
Королёв
Кострома
Красногорск
Краснодар
Красноярск
Курган
Курск
Л
Липецк
Люберцы
М
Магнитогорск
Междуреченск
Миасс
Москва
Мурманск
Муром
Н
Набережные Челны
Назрань
Находка
Невинномысск
Нефтекамск
Нефтеюганск
Нижневартовск
Нижнекамск
Нижний Новгород
Нижний Тагил
Новоалтайск
Новокузнецк
Новокуйбышевск
Новосибирск
Новый Уренгой
Новомосковск
Новороссийск
Новочебоксарск
Новочеркасск
Новошахтинск
Ногинск
Норильск
Ноябрьск
О
Обнинск
Одинцово
Октябрьский
Омск
Оренбург
Орехово-Зуево
Орёл
Орск
П
Пенза
Первоуральск
Пермь
Петрозаводск
Петропавловск-Камчатский
Подольск
Прокопьевск
Псков
Пушкино
Р
Раменское
Реутов
Ростов На Дону
Рубцовск
Рыбинск
Рязань
С
Салават
Самара
Санкт-Петербург
Саранск
Саратов
Севастополь
Северодвинск
Северск
Сергиев Посад
Серпухов
Симферополь
Славгород
Смоленск
Сочи
Ставрополь
Старый Оскол
Сургут
Сызрань
Сыктывкар
Т
Таганрог
Тамбов
Тверь
Тольятти
Томск
Тула
Тюмень
У
Улан-Уде
Ульяновск
Уссурийск
Уфа
Х
Хабаровск
Химки
Ч
Чебоксары
Челябинск
Череповец
Чита
Ш
Шахты
Щёлково
Э
Электросталь
Элиста
Энгельс
Ю
Южно-Сахалинск
Я
Якутск
Яровое
Ярославль
Ялта
Михайловский завод химических реактивов. Алтайский край, Барнаул, Социалистический проспект, 130а
| Карбонат магния | |
 |
|
 |
|
| Общие | |
|---|---|
| Химическая формула | MgCO3 |
| Физические свойства | |
| Состояние (ст. усл.) | белое гигроскопическое вещество |
| Молярная масса | 84.3139 г/моль |
| Плотность | (ангидрид) 2.958 г/см³
(дигидрат) 2.825 г/см³ (тригидрат) 1.837 г/см³ (пентагидрат) 1.73 г/см³ |
| Термические свойства | |
| Температура плавления | (с разл.) 540 °C |
| Энтальпия образования (ст. усл.) | −1111.69 кДж/моль |
| Химические свойства | |
| Растворимость в воде | (25 °C, ангидрид) 0.0012 г/100 мл
(20 °C, пентагидрат) 0.375 г/100 мл |
| Оптические свойства | |
| Показатель преломления | (ангидрид) 1.717
(дигидрат) 1.458 (тригидрат) 1.412 |
| Структура | |
| Кристаллическая структура | тригональная |
| Классификация | |
| Рег. номер CAS | 546-93-0 (ангидрид)
13717-00-5 (моногидрат) 5145-48-2 (дигидрат) 14457-83-1 (тригидрат) 61042-72-6 (пентагидрат) |
| RTECS | OM2470000 |
Карбонат магния, магний углекислый, MgCO3 — магниевая соль угольной кислоты.
Свойства
Бесцветные кристаллы, плотность 3,037 г/см³. При 500 °C заметно, а при 650 °C полностью разлагается на MgO и CO2. Растворимость карбоната магния в воде незначительна (22 мг/л при 25 °C) и уменьшается с повышением температуры. При насыщении CO2 водной суспензии MgCO3 последний растворяется вследствие образования гидрокарбоната Мg(HCO3)2. Из водных растворов в отсутствие избытка CO2 выделяются основные карбонаты магния. С карбонатами ряда металлов карбонат магния образует двойные соли, к которым относится и природный минерал доломит MgCO3·CaCO3.
Распространённость в природе
Карбонат магния широко распространён в природе в виде минерала магнезита.
Применение
Основной карбонат магния 3MgCO3·Mg(OH)2·3H2O (так называемая белая магнезия) применяют как наполнитель в резиновых смесях, для изготовления теплоизоляционных материалов.
В медицине и в качестве пищевой добавки E504 используется основной карбонат магния 4MgCO3·Mg(OH)2·nH2O
Спортивная магнезия 4MgCO3·Mg(OH)2·4H2O используется для подсушивания рук и, как следствие, увеличения надежности хвата.
Карбонат магния необходим в производстве стекла, цемента, кирпича.
См. также
- Сульфат магния (лекарство)
- Цитрат магния
Карбонат магния, характеристика, свойства и получение, химические реакции.
Карбонат магния – неорганическое вещество, имеет химическую формулу MgСО3.
Краткая характеристика карбоната магния
Физические свойства карбоната магния
Получение карбоната магния
Химические свойства карбоната магния
Химические реакции карбоната магния
Применение и использование карбоната магния
Краткая характеристика карбоната магния:
Карбонат магния – неорганическое вещество белого цвета.
Химическая формула карбоната магния MgСО3.
Карбонат магния (углекислый магний) – неорганическое химическое соединение, соль угольной кислоты и магния.
Практически не растворяется в воде.
Карбонат магния при прокаливании при температуре 500 °C заметно, а при 650 °C полностью разлагается на MgO и CO2.
Хорошо поглощает влагу.
В земной коре карбонат магния находится в свободном чистом состоянии, в форме кристаллогидратов, а также в составе основных и двойных солей.
Карбонат магния в чистом состоянии распространён в природе в виде минерала магнезита. Магнезит известен с глубокой древности. Название минерал получил от области Магнесия (Фессалия, Греция), где был впервые обнаружен.
Карбонат магния образует с водой кристаллогидраты. Их формула MgCO3·nH2O, где n может быть 2, 3 или 5. К кристаллогидратам карбоната магния относятся минералы баррингтонит MgCO3·2H2O, несквегонит MgCO3·3H2O и лансфордит MgCO3·5H2O.
Карбонат магния с гидроксидом магния и водой образует т.н. водные основные карбонаты магния. Их формула mMgCO3·MgOH·nH2O, где m – может быть 1, 3 или 4, n – 3, 4, 5 или 6. К ним относятся следующие минералы: артинит MgCO3·Mg(OH)2·3H2O, гидромагнезит 4MgCO3·Mg(OH)2·4H2O, дипингит 4MgCO3·Mg(OH)2·5H2O, йошикаваит 4MgCO3·Mg(OH)2·8H2O.
Двойные соли карбонат магния образует с карбонатами ряда металлов, к которым, к примеру, относится и природный минерал доломит MgCO3·CaCO3.
В пищевой промышленности используется 2 типа карбоната магния:
– добавка Е504(i) – карбонат магния (Magnesium carbonate) с химической формулой MgCO3;
– добавка Е504(ii) – гидрокарбонат магния (Magnesium hydrogen carbonate), именуемая также белая магнезия, с химической формулой 4MgCO3·Mg(OH)2·nH2O.
Физические свойства карбоната магния:
| Наименование параметра: | Значение: |
| Химическая формула | MgСО3 |
| Синонимы и названия иностранном языке | magnesium carbonate (англ.)
магнезит (рус.) магний углекислый (рус.) |
| Тип вещества | неорганическое |
| Внешний вид | белые тригональные кристаллы |
| Цвет | белый |
| Вкус | без вкуса |
| Запах | без запаха |
| Агрегатное состояние (при 20 °C и атмосферном давлении 1 атм.) | твердое вещество |
| Плотность (состояние вещества – твердое вещество, при 20 °C), кг/м3 | 3037 |
| Плотность (состояние вещества – твердое вещество, при 20 °C), г/см3 | 3,037 |
| Температура разложения, °C | 500-650 |
| Температура плавления, °C | — |
| Молярная масса, г/моль | 84,3139 |
| Растворимость в воде (25 oС), г/100 г | 0,0139 |
Получение карбоната магния:
Промышленный способ получения карбоната магния заключается в разработке его месторождений в природе.
В лаборатории карбонат магния получают в результате следующих химических реакций:
- 1. взаимодействия оксида магния и оксида углерода:
MgO + CO2 → MgCO3.
- 2. взаимодействия суспензии гидроксида магния и оксида углерода (углекислого газа) и последующего прокалывания образовавшегося гидрокарбоната магния:
Mg(OH)2 + 2CO2 → Mg(HCO3)2,
Mg(HCO3)2 → MgCO3 + CO2 + H2O (t = 130 °C).
- 3. взаимодействия сульфата магния и карбоната натрия:
MgSO4 + Na2CO3 → Na2SO4 + MgCO3.
- 4. взаимодействия сульфата магния и гидрокарбоната калия:
MgSO4 + 2KHCO3 → MgCO3 + K2SO4 + H2O + CO2.
- 5. взаимодействия гидрокарбоната магния и гидроксида кальция:
Mg(HCO3)2 + Ca(OH)2 → MgCO3 + CaCO3 + 2H2O.
Химические свойства карбоната магния. Химические реакции карбоната магния:
Химические свойства карбоната магния аналогичны свойствам карбонатов других металлов. Поэтому для него характерны следующие химические реакции:
1. реакция карбоната магния и оксида титана:
TiO2 + MgCO3 → MgTiO3 + CO2 (t = 800-1100 °C).
В результате реакции образуются оксид магния-титана и оксид углерода (IV).
2. реакция карбоната магния и фтороводорода:
MgCO3 + 2HF → MgF2 + CO2 + H2O.
В результате реакции образуются фторид магния, оксид углерода (IV) и вода. При этом фтороводород в качестве исходного вещества используется в виде концентрированного горячего раствора.
Аналогично проходят реакции карбоната магния и с другими кислотами.
3. реакция взаимодействия карбоната магния и воды:
2MgCO3 + H2O → Mg2(OH)2CO3 + CO2 (t°).
В результате реакции образуются дигидроксид-карбонат магния и оксид углерода (IV). Реакция протекает в горячей воде.
4. реакция взаимодействия карбоната магния, оксида углерода и воды:
MgCO3 + H2O + CO2 → Mg(HCO3)2.
В результате реакции образуется гидрокарбонат магния. Реакция протекает при комнатной температуре.
5. реакция взаимодействия карбоната магния и гидроксида натрия:
MgCO3 + 2NaOH → Mg(OH)2 + Na2CO3.
В результате реакции образуются карбонат натрия и гидроксид магния.
6. реакция взаимодействия карбоната магния и гидроксида кальция:
MgCO3 + Ca(OH)2 → Mg(OH)2 + CaCO3.
В результате реакции образуются карбонат кальция и гидроксид магния.
7. реакция взаимодействия карбоната магния и сульфата аммония:
MgCO3 + (NH4)SO4 → MgSO4 + 2NH3 + CO2 + H2O (to).
В результате реакции образуются сульфат магния, аммиак, вода и оксид углерода (IV). Реакция протекает при кипении. Сульфат аммония в ходе реакции используется в виде концентрированного раствора.
8. реакция взаимодействия карбоната магния и карбоната калия:
MgCO3 + K2CO3 → K2Mg(CO3)2.
В результате реакции образуется карбонат магния-дикалия. Реакция протекает при комнатной температуре.
9. реакция термического разложения карбоната магния:
MgCO3 → MgO + CO2 (t = 500-650 °C).
В результате реакции образуются оксид магния и оксид углерода (IV).
Применение и использование карбоната магния:
Карбонат магния используется во множестве отраслей промышленности и для бытовых нужд:
– в изготовлении огнеупорного кирпича, футеровки металлургических печей, цемента;
– в производстве стекла;
– в качестве пигмента при производстве красок и керамики,
– в медицине как лекарственное средство;
– в пищевой промышленности – в качестве пищевой добавки 504 как регулятор кислотности, антислеживающий агент, фиксатор окраски;
– в спорте как порошок, предназначенный для подсушивания рук (спортивная магнезия),
– как наполнитель в резиновых смесях,
– как наполнитель при изготовления теплоизоляционных материалов.
Примечание: © Фото //www.pexels.com, //pixabay.com
Коэффициент востребованности
4 386

|
|

|
|
| Имена | |
|---|---|
| Другие имена
Магнезит |
|
| Идентификаторы | |
|
Количество CAS |
|
|
3D модель ( JSmol ) |
|
| ЧЭБИ | |
| ЧЭМБЛ | |
| ChemSpider | |
| ECHA InfoCard |
100.008.106 |
| Номер E | E504 (i) (регуляторы кислотности, …) |
|
PubChem CID |
|
| Номер RTECS | |
| UNII | |
|
Панель управления CompTox ( EPA ) |
|
|
ИнЧИ
|
|
|
Улыбки
|
|
| Характеристики | |
|
Химическая формула |
MgCO 3 |
| Молярная масса | 84,3139 г / моль (безводный) |
| Появление | Белое твердое вещество гигроскопично |
| Запах | Без запаха |
| Плотность | 2,958 г / см 3 (безводный) 2,825 г / см 3 (дигидрат) 1,837 г / см 3 (тригидрат) 1,73 г / см 3 (пентагидрат) |
| Температура плавления | 350 ° C (662 ° F, 623 K) разлагается (безводный) 165 ° C (329 ° F, 438 K) (тригидрат) |
|
Растворимость в воде |
Безводный: 0,0139 г / 100 мл (25 ° C) 0,0063 г / 100 мл (100 ° C) |
|
Произведение растворимости ( K уд ) |
10 −7,8 |
| Растворимость | Растворим в кислоте, водном CO 2 Нерастворим в ацетоне , аммиаке |
|
Магнитная восприимчивость (χ) |
−32,4 · 10 −6 см 3 / моль |
|
Показатель преломления ( n D ) |
1,717 (безводный) 1,458 (дигидрат) 1,412 (тригидрат) |
| Состав | |
|
Кристальная структура |
Тригональный |
| Термохимия | |
|
Теплоемкость ( C ) |
75,6 Дж / моль · К |
|
Стандартная мольная |
65,7 Дж / моль · К |
|
Std энтальпия |
−1113 кДж / моль |
|
Свободная энергия Гиббса (Δ f G ˚) |
-1029,3 кДж / моль |
| Фармакология | |
|
Код УВД |
A02AA01 ( ВОЗ ) A06AD01 ( ВОЗ ) |
| Опасности | |
| Паспорт безопасности | ICSC 0969 |
| NFPA 704 (огненный алмаз) |
1 0 0 |
| точка возгорания | Не воспламеняется |
| NIOSH (пределы воздействия на здоровье в США): | |
|
PEL (Допустимо) |
|
| Родственные соединения | |
|
Другие анионы |
Бикарбонат магния |
|
Другие катионы |
Карбонат бериллия Карбонат кальция Карбонат стронция Карбонат бария Карбонат радия |
|
Родственные соединения |
Артинит Гидромагнезит Дипингит |
|
Если не указано иное, данные приведены для материалов в их стандартном состоянии (при 25 ° C [77 ° F], 100 кПа). |
|
|
|
|
| Ссылки на инфобоксы | |
Карбонат магния , Mg CO 3 (архаичное название magnesia alba ), представляет собой неорганическую соль, представляющую собой белое твердое вещество. Некоторые гидратированные и основные формы карбоната магния также существуют в виде минералов .
Формы
Наиболее распространенными формами карбоната магния являются безводная соль, называемая магнезитом (MgCO 3 ), и ди-, три- и пентагидраты, известные как баррингтонит (MgCO 3 · 2 H 2 O), несквегонит (MgCO 3 · 3 H 2 O) и лансфордит. (MgCO 3 · 5 H 2 O) соответственно. Некоторые основные формы, такие как артинит (MgCO 3 · Mg (OH) 2 · 3 H 2 O), гидромагнезит (4 MgCO 3 · Mg (OH) 2 · 4 H 2 O) и дипингит (4 MgCO 3 · Mg (OH ) 2 · 5 H 2 O) также встречаются в виде минералов .
Магнезит состоит из белых треугольных кристаллов . Безводная соль практически не растворяется в воде , ацетоне и аммиаке . Все формы карбоната магния реагируют с кислотами . Карбонат магния кристаллизуется в структуре кальцита, в которой Mg 2+ окружен шестью атомами кислорода . Дигидрат имеет триклинную структуру, а тригидрат — моноклинную .
Ссылки на «легкие» и «тяжелые» карбонаты магния фактически относятся к гидроксикарбонатам магния, гидромагнезиту и дипингиту (соответственно).
Подготовка
Карбонат магния обычно получают при добыче минерального магнезита . Семьдесят процентов мировых запасов добывается и готовится в Китае.
Карбонат магния можно получить в лаборатории путем реакции между любой растворимой солью магния и бикарбонатом натрия:
- MgCl 2 (водн.) + 2 NaHCO 3 (водн.) → MgCO 3 (т.) + 2 NaCl (водн.) + H 2 O (l) + CO 2 (г)
Если хлорид (или сульфат) магния обработать водным карбонатом натрия, образуется осадок основного карбоната магния — гидратированный комплекс карбоната магния и гидроксида магния — а не сам карбонат магния:
- 5 MgCl 2 (водн.) + 5 Na 2 CO 3 (водн.) + 5 H 2 O (l) → Mg (OH) 2 · 3 MgCO 3 · 3 H 2 O (тв.) + Mg (HCO 3 ) 2 (водн. ) + 10 NaCl (водн.)
Промышленные пути высокой чистоты включают путь через бикарбонат магния , который может быть образован путем объединения суспензии гидроксида магния и диоксида углерода при высоком давлении и умеренной температуре. Затем бикарбонат сушат в вакууме, в результате чего теряется углекислый газ и молекула воды:
- Mg (OH) 2 + 2 CO 2 → Mg (HCO 3 ) 2
- Mg (HCO 3 ) 2 → MgCO 3 + CO 2 + H 2 O
Химические свойства
С кислотами
Как и многие обычные карбонаты металлов группы 2, карбонат магния реагирует с водными кислотами с выделением диоксида углерода и воды :
- MgCO 3 + 2 HCl → MgCl 2 + CO 2 + H 2 O
- MgCO 3 + H 2 SO 4 → MgSO 4 + CO 2 + H 2 O
Разложение
При высоких температурах MgCO 3 разлагается на оксид магния и диоксид углерода . Этот процесс важен при производстве оксида магния. Этот процесс называется прокаливанием :
- MgCO 3 → MgO + CO 2 (ΔH = +118 кДж / моль)
Температура разложения составляет 350 ° C (662 ° F). Однако прокаливание до оксида обычно не считается завершенным при температуре ниже 900 ° C из-за препятствования повторной абсорбции высвобожденного диоксида углерода.
Гидраты солей при разложении теряют воду при разных температурах. Например, в тригидрате, молекулярная формула которого может быть записана как Mg (HCO 3 ) (OH) • 2 (H 2 O), стадии дегидратации происходят при 157 ° C и 179 ° C следующим образом:
- Mg (HCO 3 ) (OH) • 2 (H 2 O) → Mg (HCO 3 ) (OH) • (H 2 O) + H 2 O при 157 ° C
- Mg (HCO 3 ) (OH) • (H 2 O) → Mg (HCO 3 ) (OH) + H 2 O при 179 ° C
Использует
Основное применение карбоната магния — производство оксида магния путем прокаливания. Минералы магнезита и доломита используются для производства огнеупорного кирпича . MgCO 3 также используется в напольных покрытий , огнестойкость , огнетушащих составов , косметических средств , присыпки , и зубной пасты . Другие области применения — это наполнитель , подавитель дыма в пластмассах, усиливающий агент в неопреновом каучуке, осушающий агент , слабительное средство для разрыхления кишечника и сохранение цвета в пищевых продуктах. Кроме того, карбонат магния высокой чистоты используется в качестве антацида и добавки к поваренной соли, чтобы она оставалась сыпучей. Карбонат магния может сделать это, потому что он не растворяется в воде, а только в кислоте, где он будет шипеть (пузыриться).
Альпинист Ян Хойер выдувает из руки излишки мела . Чемпионат мира по боулдерингу 2015
Из-за его низкой растворимости в воде и гигроскопических свойств MgCO 3 впервые был добавлен в соль в 1911 году, чтобы она текла более свободно. Компания Morton Salt использовала слоган «Когда идет дождь, он льет» со ссылкой на тот факт, что ее соль, содержащая MgCO 3 , не слипается во влажную погоду. Карбонат магния, чаще всего называемый «мелом», также используется в качестве сушильного агента для рук спортсменов в скалолазании , гимнастике , поднятии тяжестей и других видах спорта, в которых необходим крепкий захват.
В качестве пищевой добавки карбонат магния известен как E504, единственным известным побочным эффектом которого является то, что он может работать как слабительное в высоких концентрациях.
Карбонат магния используется в таксидермии для отбеливания черепа. Его можно смешать с перекисью водорода, чтобы получить пасту, которую затем намазывают на череп, чтобы придать ему белый цвет.
Карбонат магния используется в качестве белого матового покрытия для проекционных экранов .
Безопасность
Карбонат магния нетоксичен и негорючий.
Компендиальный статус
- Британская фармакопея
- Японская фармакопея
Смотрите также
- Ацетат кальция / карбонат магния
- Упсалит , известная аморфная форма карбоната магния.
Примечания и ссылки
внешние ссылки
- Международная карта химической безопасности 0969
- Стандартная справочная база данных NIST


