Калий углекислый
Химическая формула:
K2CO3
Международное название:
POTASSIUM CARBONATE
CAS No:
584-08-7
Квалификация:
Имп. «ч», пр-во Тайвань, Китай, Ю.Корея
Внешний вид:
гранулы белого цвета
Фасовка:
мешки, 25 кг
Условия хранения:
в сухом, хорошо проветриваемом помещении, предохраняя от попадания влаги
Сделать заказ
Синонимы:
карбонат калия, калий карбонат, поташ
Мы предлагаем Калий углекислый, Калий карбонат пр-ва Тайвань и Китай для пищевой промышленности по привлекательным ценам с доставкой по всей России.
| Спецификация | |
|---|---|
| Молекулярный вес | 138.21 |
| Плотность | 2.43 |
| Температура плавления | 891ºC |
| Растворимость в воде | 1120 г/л (20 ºC) |
| Спецификация (пр-во Тайвань) | % |
| Основного вещества, не менее | 99,5 % (по факт.99,82%) |
| Содержание Fe, не более | 0,0005 % |
| Содержание KOH, не более | 0,20 % |
| Содержание Na, не более | 0,30 % |
| Содержание K2SO4, не более | 0,01 % |
| Содержание KCL, не более | 0,01 % |
| Тяжелых металлов (Pb), не более | 0,0002 % |
| Потери при прокаливании, не более | 0,50 % |
| Спецификация (пр-во Китай) | % |
| Основного вещества, не менее | 99,0 % (по факт.99,34%) |
| Содержание Fe, не более | 0,001 % |
| Содержание As, не более | 0,0002 % |
| Потери при прокаливании, не более | 0,6 % (по факт. 0,16%) |
| Содержание K2SO4, не более | 0,01 % |
| Содержание хлоридов KCL, не более | 0,015 % |
| Тяжелых металлов (Pb), не более | 0,001 % |
| Нерастворимый в воде остаток, не более | 0,002 % |
Для согласования условий оплаты, звоните нашим менеджерам по телефонам в Москве:
(495) 787-01-37, 36, 38
(495) 787-43-51
и Санкт- Петербурге:
(812) 309-38-06 (многоканальный)
Калий углекислый или Калий карбонат K2CO3 — средняя соль калия и угольной кислоты. Калий углекислый — белое кристаллическое вещество, хорошо растворимое в воде.
Старое название калия углекислого — поташ, отсюда английское наименование калия — potassium. Поташ — одна из наиболее древних солей, известных людям.
Получение
До XX века в Европе поташ или калий углекислый был одним из важнейших промышленных химических реагентов. Его получали путём водной экстракции из растительной золы, с дальнейшей очисткой до необходимого уровня. Производство карбоната калия было сосредоточено в местах, богатых лесом — кое-где в Европе, но в основном в России и Северной Америке. Карбонат калия, углекислый калий в промышленности, главным образом получают из солей калия или как побочный продукт переработки нефтелина на глинозем.
Применение
Карбонат калия (углекислый калий, поташ) используется
• в строительстве (в качестве противоморозной добавки),
• в стекольной отрасли,
• в электровакуумной отрасли,
• в химической и других отраслей промышленности,
• применялся при изготовлении сукна, мыла, ценных сортов стекла, красок, выделке кож,
• в пищевой промышленности, фармацевтике и др.
Всегда в наличии по выгодным ценам
В нашем ассортименте всегда в наличии на складе по выгодной цене:
Трилон б,
Оксиэтилендифосфоновая кислота (ОЭДФК),
Ортофосфорная кислота и др.
Для покупки этой и другой химической продукции в Москве или Санкт-Петербурге, звоните нам!
-
Выгодные цены
Даже при изначально низких ценах, мы
предоставляем значительные скидки в
зависимости от объема закупаемой продукции - Быстрая отгрузка
Четкая работа нашего склада позволяет
осуществить быструю отгрузку необходимой
продукции - Высокое качество
Работая напрямую с производителями по всему
миру, мы обеспечиваем наших клиентов
продукцией высокого качества -
Доставка по России
Ускоренная доставка продукции:- автотранспортом;
- железнодорожными контейнерами, вагонами;
- авиатранспортом;
- через транспортные компании.
Для получения подробной информации о ценах на химреактивы
и согласования условий оплаты звоните по телефонам:
в Москве:
+7 (495) 787-01-37
+7 (495) 787-43-51
в Санкт- Петербурге:
+7 (812) 309-38-06
карбонат калия
- карбонат калия
-
хлорат калия, хлорноватокислый калий, углекислый калий
Cловарь химических синонимов I .
.
2013.
Смотреть что такое «карбонат калия» в других словарях:
-
Карбонат калия — Карбонат калия … Википедия
-
КАРБОНАТ КАЛИЯ — (углекислый калий, поташ, К2СО3), белое твердое вещество. В промышленности обычно получают путем ЭЛЕКТРОЛИЗА хлорида калия с последующей обработкой получившегося ГИДРОКСИДА КАЛИЯ ДИОКСИДОМ УГЛЕРОДА. Применяется как удобрение, а также в… … Научно-технический энциклопедический словарь
-
карбонат калия — поташ (K2CO3) [http://slovarionline.ru/anglo russkiy slovar neftegazovoy promyishlennosti/] Тематики нефтегазовая промышленность Синонимы поташ EN potassium carbonate … Справочник технического переводчика
-
Калия карбонат — Поташ Карбонат калия (углекислый калий, поташ) K2CO3 средняя соль калия и угольной кислоты. Это белое кристаллическое вещество, хорошо растворимое в воде. Старое традиционное название соли поташ, оно связано с латинским наименованием калия … … Википедия
-
Калия цианид — Цианид калия Общие Систематическое наименование калия цианид Химическая формула KCN Молярная масса 65,11 г/моль … Википедия
-
Карбонат железа(II) — Общие Систематическое наименование Карбонат железа(II) Традиционные названия Углекислое железо Химическая формула FeCO3 Физические свойства Состо … Википедия
-
Карбонат аммония — Карбонат аммония, углекислый аммоний, (NH4)2CO3 аммониевая соль угольной кислоты. Содержание 1 Свойства 2 Применение 3 Примечания … Википедия
-
Карбонат меди(II) — Общие … Википедия
-
Карбонат кобальта(II) — Общие Систематическое наименование Карбонат кобальта(II) Традиционные названия Углекислый кобальт Химическая формула CoCO3 Физические свойства … Википедия
-
Карбонат марганца(II) — Карбонат марганца(II) … Википедия
импорт
импорт
импорт
импорт
Б сорт1/ порошкообразный
импорт
Мешок 25 кг
металлургический
2455-055-58901825-2008
импорт
изм.№1,
импорт
6318-77,
2141-084-56238216-2010
МКР 600 кг, 800 кг, 1250 кг
Мешок 50 кг
импорт
5870-002-58042865-2003
From Wikipedia, the free encyclopedia
|
|
|
|

|
|
| Names | |
|---|---|
| IUPAC name
Potassium carbonate |
|
| Other names
Carbonate of potash, dipotassium carbonate, sub-carbonate of potash, pearl ash, potash, salt of tartar, salt of wormwood. |
|
| Identifiers | |
|
CAS Number |
|
|
3D model (JSmol) |
|
| ChEBI |
|
| ChemSpider |
|
| ECHA InfoCard | 100.008.665 |
| E number | E501(i) (acidity regulators, …) |
|
PubChem CID |
|
| RTECS number |
|
| UNII |
|
|
CompTox Dashboard (EPA) |
|
|
InChI
|
|
|
SMILES
|
|
| Properties | |
|
Chemical formula |
K 2CO 3 |
| Molar mass | 138.205 g/mol |
| Appearance | White, hygroscopic solid |
| Density | 2.43 g/cm3 |
| Melting point | 891 °C (1,636 °F; 1,164 K) |
| Boiling point | Decomposes |
|
Solubility in water |
110.3 g/100 mL (20 °C) 149.2 g/100 mL (100 °C) |
| Solubility |
|
| Acidity (pKa) | 10.25 |
|
Magnetic susceptibility (χ) |
−59.0·10−6 cm3/mol |
| Thermochemistry[1] | |
|
Heat capacity (C) |
114.4 J·mol−1·K−1 |
|
Std molar |
155.5 J·mol−1·K−1 |
|
Std enthalpy of |
−1151.0 kJ·mol−1 |
|
Gibbs free energy (ΔfG⦵) |
−1063.5 kJ·mol−1 |
|
Enthalpy of fusion (ΔfH⦵fus) |
27.6 kJ·mol−1 |
| Hazards | |
| GHS labelling: | |
|
Pictograms |

|
|
Signal word |
Warning |
|
Hazard statements |
H302, H315, H319, H335 |
|
Precautionary statements |
P261, P305+P351+P338 |
| NFPA 704 (fire diamond) |
1 0 0 |
| Flash point | Non-flammable |
| Lethal dose or concentration (LD, LC): | |
|
LD50 (median dose) |
1870 mg/kg (oral, rat)[2] |
| Safety data sheet (SDS) | ICSC 1588 |
| Related compounds | |
|
Other anions |
Potassium bicarbonate |
|
Other cations |
Lithium carbonate Sodium carbonate Rubidium carbonate Caesium carbonate |
|
Related compounds |
Ammonium carbonate |
|
Except where otherwise noted, data are given for materials in their standard state (at 25 °C [77 °F], 100 kPa).
Infobox references |
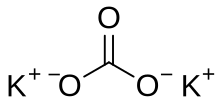
Potassium carbonate is the inorganic compound with the formula K2CO3. It is a white salt, which is soluble in water and forms a strongly alkaline solution. It is deliquescent, often appearing as a damp or wet solid. Potassium carbonate is mainly used in the production of soap and glass.[3]
History[edit]
Potassium carbonate is the primary component of potash and the more refined pearl ash or salts of tartar. Historically, pearl ash was created by baking potash in a kiln to remove impurities. The fine, white powder remaining was the pearl ash. The first patent issued by the US Patent Office was awarded to Samuel Hopkins in 1790 for an improved method of making potash and pearl ash.
In late 18th-century North America, before the development of baking powder, pearl ash was used as a leavening agent for quick breads.[4][5]
Production[edit]
Potassium carbonate is prepared commercially by the reaction of potassium hydroxide with carbon dioxide:[3]
- 2 KOH + CO2 → K2CO3 + H2O
From the solution crystallizes the sesquihydrate K2CO3·3⁄2H2O («potash hydrate»). Heating this solid above 200 °C (392 °F) gives the anhydrous salt. In an alternative method, potassium chloride is treated with carbon dioxide in the presence of an organic amine to give potassium bicarbonate, which is then calcined:
- 2 KHCO3 → K2CO3 + H2O + CO2
Applications[edit]
- (historically) for soap, glass, and dishware production
- as a mild drying agent where other drying agents, such as calcium chloride and magnesium sulfate, may be incompatible. It is not suitable for acidic compounds, but can be useful for drying an organic phase if one has a small amount of acidic impurity. It may also be used to dry some ketones, alcohols, and amines prior to distillation.[6]
- in cuisine, where it has many traditional uses. It is used in some types of Chinese noodles and mooncakes, as well as Asian grass jelly and Japanese ramen. German gingerbread recipes often use potassium carbonate as a baking agent, although in combination with hartshorn.
- in the alkalization of cocoa powder to produce Dutch process chocolate by balancing the pH (i.e., reduce the acidity) of natural cocoa beans; it also enhances aroma. The process of adding potassium carbonate to cocoa powder is usually called «Dutching» (and the products referred to as Dutch-processed cocoa powder), as the process was first developed in 1828 by Dutchman Coenraad Johannes van Houten.
- as a buffering agent in the production of mead or wine.
- in antique documents, it is reported to have been used to soften hard water.[7]
- as a fire suppressant in extinguishing deep-fat fryers and various other B class-related fires.
- in condensed aerosol fire suppression, although as the byproduct of potassium nitrate.
- as an ingredient in welding fluxes, and in the flux coating on arc-welding rods.
- as an animal feed ingredient to satisfy the potassium requirements of farmed animals such as broiler breeder chickens.
- as an acidity regulator in Swedish snus snuff tobacco
References[edit]
- ^ CRC handbook of chemistry and physics : a ready-reference book of chemical and physical data. William M. Haynes, David R. Lide, Thomas J. Bruno (2016-2017, 97th ed.). Boca Raton, Florida. 2016. ISBN 978-1-4987-5428-6. OCLC 930681942.
{{cite book}}: CS1 maint: others (link) - ^ Chambers, Michael. «ChemIDplus — 584-08-7 — BWHMMNNQKKPAPP-UHFFFAOYSA-L — Potassium carbonate [USP] — Similar structures search, synonyms, formulas, resource links, and other chemical information». chem.sis.nlm.nih.gov. Archived from the original on 2014-08-12.
- ^ a b H. Schultz, G. Bauer, E. Schachl, F. Hagedorn, P. Schmittinger (2005). «Potassium Compounds». Ullmann’s Encyclopedia of Industrial Chemistry. Weinheim: Wiley-VCH. doi:10.1002/14356007.a22_039. ISBN 3527306730.
{{cite encyclopedia}}: CS1 maint: uses authors parameter (link) - ^ See references to «pearl ash» in «American Cookery» by Amelia Simmons, printed by Hudson & Goodwin, Hartford, 1796.
- ^ Civitello, Linda (2017). Baking powder wars : the cutthroat food fight that revolutionized cooking. Urbana, Illinois: University of Illinois Press. pp. 18–22. ISBN 9780252041082.
- ^ Leonard, J.; Lygo, B.; Procter, G. «Advanced Practical Organic Chemistry» 1998, Stanley Thomas Publishers Ltd
- ^ Child, Lydia M. «The American Frugal Housewife» 1832
Bibliography[edit]
- A Dictionary of Science, Oxford University Press, New York, 2004
- Yu. Platonov, Andrew; Evdokimov, Andrey; Kurzin, Alexander; D. Maiyorova, Helen (29 June 2002). «Solubility of Potassium Carbonate and Potassium Hydrocarbonate in Methanol». Journal of Chemical & Engineering Data. 47 (5): 1175–1176. doi:10.1021/je020012v.
External links[edit]
- International Chemical Safety Card 1588
Алф. указатель:
1-9
A-Z
А
Б
В
Г
Д
Е
Ж
З
И
К
Л
М
Н
О
П
Р
С
Т
У
Ф
Х
Ц
Ч
Щ
Э
Я
калия карбонат
Синонимы:
поташ
Внешний вид:
бесцветн. моноклинные кристаллы
Брутто-формула (система Хилла): CK2O3
Формула в виде текста: K2CO3
Молекулярная масса (в а.е.м.): 138,21
Температура плавления (в °C): 891
Растворимость (в г/100 г или характеристика):
ацетон: не растворим
вода: 107 (0°C)
вода: 109,2 (10°C)
вода: 111 (20°C)
вода: 112,3 (25°C)
вода: 113,7 (30°C)
вода: 116,9 (40°C)
вода: 125,7 (60°C)
вода: 139,2 (80°C)
вода: 155,8 (100°C)
вода: 274 (200°C)
глицерин: 39,4 (20°C)
этанол: не растворим
Вкус, запах, гигроскопичность:
гигроскопичен
Плотность:
2,43 (19°C, г/см3)
Динамическая вязкость жидкостей и газов (в мПа·с):
3,03 (917°C)
1,66 (977°C)
Поверхностное натяжение (в мН/м):
168,4 (910°C)
162,1 (1010°C)
Стандартная энтальпия образования ΔH (298 К, кДж/моль):
-1146,1 (т)
Стандартная энергия Гиббса образования ΔG (298 К, кДж/моль):
-1059,8 (т)
Стандартная энтропия образования S (298 К, Дж/моль·K):
156,32 (т)
Стандартная мольная теплоемкость Cp (298 К, Дж/моль·K):
115,7 (т)
Энтальпия плавления ΔHпл (кДж/моль):
32,6
Дополнительная информация:
При насыщении карбонатом калия водно-спиртового раствора при 23-25 С образуется двухслойная система содержащая в нижнем слое 53,6% карбоната калия и 0,28% этанола, а в верхнем слое 0,095% карбоната калия и 90,65% этанола.
- «Справочник химика» т.3, Л.-М.: Химия, 1965 стр. 299, 301
- Рабинович В.А., Хавин З.Я. «Краткий химический справочник» Л.: Химия, 1977 стр. 68
Источники информации:
Алф. указатель:
1-9
A-Z
А
Б
В
Г
Д
Е
Ж
З
И
К
Л
М
Н
О
П
Р
С
Т
У
Ф
Х
Ц
Ч
Щ
Э
Я
Еще по теме:
- КАЛИЯ КАРБОНАТ — химическая энциклопедия
- калия карбонат — химическая энциклопедия
- Калия карбонат — лекарственные препараты
- Калия карбонат — лекарственные препараты

