From Wikipedia, the free encyclopedia
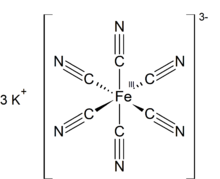
|
|

|
|
| Names | |
|---|---|
| IUPAC name
Potassium hexacyanoferrate(III) |
|
| Other names
Red prussiate of Potash, |
|
| Identifiers | |
|
CAS Number |
|
|
3D model (JSmol) |
|
| ChEBI |
|
| ChemSpider |
|
| ECHA InfoCard | 100.033.916 |
| EC Number |
|
|
Gmelin Reference |
21683 |
|
PubChem CID |
|
| RTECS number |
|
| UNII |
|
|
CompTox Dashboard (EPA) |
|
|
InChI
|
|
|
SMILES
|
|
| Properties | |
|
Chemical formula |
K3[Fe(CN)6] |
| Molar mass | 329.24 g/mol |
| Appearance | deep red crystals, sometimes small pellets, orange to dark red powder |
| Density | 1.89 g/cm3, solid |
| Melting point | 300 °C (572 °F; 573 K) |
| Boiling point | decomposes |
|
Solubility in water |
330 g/L («cold water») 464 g/L (20 °C) 775 g/L («hot water»)[1] |
| Solubility | slightly soluble in alcohol soluble in acid soluble in water |
|
Magnetic susceptibility (χ) |
+2290.0·10−6 cm3/mol |
| Structure | |
|
Crystal structure |
monoclinic |
|
Coordination geometry |
octahedral at Fe |
| Hazards | |
| GHS labelling: | |
|
Pictograms |

|
|
Signal word |
Warning |
|
Hazard statements |
H302, H315, H319, H332, H335 |
|
Precautionary statements |
P261, P264, P270, P271, P280, P301+P312, P302+P352, P304+P312, P304+P340, P305+P351+P338, P312, P321, P330, P332+P313, P337+P313, P362, P403+P233, P405, P501 |
| NFPA 704 (fire diamond) |
1 0 0 |
| Flash point | Non-flammable |
| Lethal dose or concentration (LD, LC): | |
|
LD50 (median dose) |
2970 mg/kg (mouse, oral) |
| Safety data sheet (SDS) | MSDS |
| Related compounds | |
|
Other anions |
Potassium ferrocyanide |
|
Other cations |
Prussian blue |
|
Except where otherwise noted, data are given for materials in their standard state (at 25 °C [77 °F], 100 kPa).
Infobox references |
Potassium ferricyanide when milled has lighter color
Potassium ferricyanide is the chemical compound with the formula K3[Fe(CN)6]. This bright red salt contains the octahedrally coordinated [Fe(CN)6]3− ion.[2] It is soluble in water and its solution shows some green-yellow fluorescence. It was discovered in 1822 by Leopold Gmelin.[3][4]
Preparation[edit]
Potassium ferricyanide is manufactured by passing chlorine through a solution of potassium ferrocyanide. Potassium ferricyanide separates from the solution:
- 2 K4[Fe(CN)6] + Cl2 → 2 K3[Fe(CN)6] + 2 KCl
Structure[edit]
Like other metal cyanides, solid potassium ferricyanide has a complicated polymeric structure. The polymer consists of octahedral [Fe(CN)6]3− centers crosslinked with K+ ions that are bound to the CN ligands.[5] The K+—NCFe linkages break when the solid is dissolved in water.
Applications[edit]
The compound is also used to harden iron and steel, in electroplating, dyeing wool, as a laboratory reagent, and as a mild oxidizing agent in organic chemistry.
Photography[edit]
Blueprint, cyanotype, toner[edit]
The compound has widespread use in blueprint drawing and in photography (Cyanotype process). Several photographic print toning processes involve the use of potassium ferricyanide.
Bleaching[edit]
Potassium ferricyanide was used as an oxidizing agent to remove silver from color negatives and positives during processing, a process called bleaching. Because potassium ferricyanide bleaches are environmentally unfriendly, short-lived, and capable of releasing hydrogen cyanide gas if mixed with high concentrations and volumes of acid, bleaches using ferric EDTA have been used in color processing since the 1972 introduction of the Kodak C-41 process. In color lithography, potassium ferricyanide is used to reduce the size of color dots without reducing their number, as a kind of manual color correction called dot etching.
Farmers Reducer[edit]
Ferricyanide is also used in black-and-white photography with sodium thiosulfate (hypo) to reduce the density of a negative or gelatin silver print where the mixture is known as Farmer’s reducer; this can help offset problems from overexposure of the negative, or brighten the highlights in the print.[6]
Reagent in organic synthesis[edit]
Potassium ferricyanide is a used as an oxidant in organic chemistry.[7][8] It is an oxidant for catalyst regeneration in Sharpless dihydroxylations.[9][10]
Sensors and indicators[edit]
Potassium ferricyanide is also one of two compounds present in ferroxyl indicator solution (along with phenolphthalein) that turns blue (Prussian blue) in the presence of Fe2+ ions, and which can therefore be used to detect metal oxidation that will lead to rust. It is possible to calculate the number of moles of Fe2+ ions by using a colorimeter, because of the very intense color of Prussian blue.
In physiology experiments potassium ferricyanide provides a means increasing a solution’s redox potential (E°’ ~ 436 mV at pH 7). As such, it can oxidize reduced cytochrome c (E°’ ~ 247 mV at pH 7) in isolated mitochondria. Sodium dithionite is usually used as a reducing chemical in such experiments (E°’ ~ −420 mV at pH 7).
Potassum ferricyanide is used to determine the ferric reducing power potential of a sample (extract, chemical compound, etc.).[11] Such a measurement is used to determine of the antioxidant property of a sample.
Potassium ferricyanide is a component of amperometric biosensors as an electron transfer agent replacing an enzyme’s natural electron transfer agent such as oxygen as with the enzyme glucose oxidase. It is an ingredient in commercially available blood glucose meters for use by diabetics.
Other[edit]
Potassium ferricyanide is combined with potassium hydroxide (or sodium hydroxide as a substitute) and water to formulate Murakami’s etchant. This etchant is used by metallographers to provide contrast between binder and carbide phases in cemented carbides.
Prussian blue[edit]
Prussian blue, the deep blue pigment in blue printing, is generated by the reaction of K3[Fe(CN)6] with ferrous (Fe2+) ions as well as K4[Fe(CN)6] with ferric salts.[12]
In histology, potassium ferricyanide is used to detect ferrous iron in biological tissue. Potassium ferricyanide reacts with ferrous iron in acidic solution to produce the insoluble blue pigment, commonly referred to as Turnbull’s blue or Prussian blue. To detect ferric (Fe3+) iron, potassium ferrocyanide is used instead in the Perls’ Prussian blue staining method.[13] The material formed in the Turnbull’s blue reaction and the compound formed in the Prussian blue reaction are the same.[14][15]
Safety[edit]
Potassium ferricyanide has low toxicity, its main hazard being that it is a mild irritant to the eyes and skin. However, under very strongly acidic conditions, highly toxic hydrogen cyanide gas is evolved, according to the equation:
- 6 H+ + [Fe(CN)6]3− → 6 HCN + Fe3+[16]
See also[edit]
- Ferricyanide
- Ferrocyanide
- Potassium ferrocyanide
References[edit]
- ^ Kwong, H.-L. (2004). «Potassium Ferricyanide». In Paquette, L. (ed.). Encyclopedia of Reagents for Organic Synthesis. New York: J. Wiley & Sons. doi:10.1002/047084289X. hdl:10261/236866. ISBN 9780471936237.
- ^ Sharpe, A. G. (1976). The Chemistry of Cyano Complexes of the Transition Metals. London: Academic Press.
- ^ Gmelin, Leopold (1822). «Ueber ein besonderes Cyaneisenkalium, and über eine neue Reihe von blausauren Eisensalzen» [On a particular potassium iron cyanate, and on a new series of iron salts of cyanic acid]. Journal für Chemie und Physik (in German). 34: 325–346.
- ^ Ihde, A.J. (1984). The Development of Modern Chemistry (2nd ed.). New York: Dover Publications. p. 153.
- ^ Figgis, B. N.; Gerloch, M.; Mason, R. (1969). «The crystallography and paramagnetic anisotropy of potassium ferricyanide». Proceedings of the Royal Society of London. A. Mathematical and Physical Sciences. 309 (1496): 91–118. Bibcode:1969RSPSA.309…91F. doi:10.1098/rspa.1969.0031. S2CID 96689342.
- ^ Stroebel, L.; Zakia, R. D. (1993). «Farmer’s Reducer». The Focal Encyclopedia of Photography. Focal Press. p. 297. ISBN 978-0-240-51417-8.
- ^ Prill, E. A.; McElvain, S. M. (1935). «1-Methyl-2-Pyridone». Organic Syntheses. 15: 41. doi:10.15227/orgsyn.015.0041.
- ^ Würfel, Hendryk; Jakobi, Dörthe (2018). «Syntheses of Substituted 2-Cyano-benzothiazoles». Organic Syntheses. 95: 177–191. doi:10.15227/orgsyn.095.0177.
- ^ Gonzalez, Javier; Aurigemma, Christine; Truesdale, Larry (2002). «Synthesis of (+)-(1S,2R)- and (−)-(1R,2S)-trans-2-Phenylcyclohexanol via Sharpless Asymmetric Dihydroxylation (AD)». Organic Syntheses. 79: 93. doi:10.15227/orgsyn.079.0093.
- ^ Oi, Ryu; Sharpless, K. Barry (1996). «3-[(1S)-1,2-Dihydroxyethyl]-1,5-Dihydro-3H-2,4-Benzodioxepine». Organic Syntheses. 73: 1. doi:10.15227/orgsyn.073.0001.
- ^ Nakajima, Y., Sato, Y., & Konishi, T. (2007). Antioxidant Small Phenolic Ingredients in
Inonotus obliquus (persoon) Pilat (Chaga). Chemical & Pharmaceutical Bulletin, 55(8), 1222–1276. - ^ Dunbar, K. R.; Heintz, R. A. (1997). «Chemistry of Transition Metal Cyanide Compounds: Modern Perspectives». Progress in Inorganic Chemistry. Progress in Inorganic Chemistry. Vol. 45. pp. 283–391. doi:10.1002/9780470166468.ch4. ISBN 9780470166468.
- ^ Carson, F. L. (1997). Histotechnology: A Self-Instructional Text (2nd ed.). Chicago: American Society of Clinical Pathologists. pp. 209–211. ISBN 978-0-89189-411-7.
- ^ Tafesse, F. (2003). «Comparative Studies on Prussian Blue or Diaquatetraamine-Cobalt(III) Promoted Hydrolysis of 4-Nitrophenylphosphate in Microemulsions» (PDF). International Journal of Molecular Sciences. 4 (6): 362–370. doi:10.3390/i4060362.
- ^ Verdaguer, M.; Galvez, N.; Garde, R.; Desplanches, C. (2002). «Electrons at Work in Prussian Blue Analogues» (PDF). Electrochemical Society Interface. 11 (3): 28–32. doi:10.1002/chin.200304218.
- ^ «MSDS for potassium ferricyanide» (PDF).
External links[edit]
- International Chemical Safety Card 1132
- National Pollutant Inventory – Cyanide compounds fact sheet
железосинеродистый калий
- железосинеродистый калий
-
красная кровяная соль, гексацианоферриат калия
Cловарь химических синонимов I .
.
2013.
Смотреть что такое «железосинеродистый калий» в других словарях:
-
Железосинеродистый калий — Гексацианоферрат (III) калия (красная кровяная соль) Гексацианоферрат(III) калия (железосинеродистый калий, феррицианид калия, гексацианоферрат калия) комплексное соединение трёхвалентного железа K3[Fe(CN)6]. Содержание 1 Тривиальные названия … Википедия
-
Железосинеродистый калий — K3[Fe(CN)6], то же, что красная кровяная соль, или Калия гексацианоферриат … Большая советская энциклопедия
-
Железосинеродистый калий — см. Гмелина соль … Энциклопедический словарь Ф.А. Брокгауза и И.А. Ефрона
-
Калий железосинеродистый — Жёлтая кровяная соль Гексацианоферрат(II) калия (железистосинеродистый калий, ферроцианид калия, гексацианоферриат калия) комплексное соединение двухвалентного железа K4[Fe(CN)6], существуюшее обычно в виде тригидрата K4[Fe(CN)6]·3H2O. Содержание … Википедия
-
Калия гексацианоферриат — железосинеродистый калий, феррицианид калия, красное синькали, красная кровяная соль, K3[Fe (CN)6], комплексное соединение 3 валентного железа; тёмно красные кристаллы, плотность 1,86 г/см3. Получают окислением Калия гексацианоферроата. С … Большая советская энциклопедия
-
Калия гексацианоферроат — железосинеродистый калий, ферроцианид калия, жёлтое синькали, жёлтая кровяная соль, K4[Fe (CN)6]·3H2O, комплексное соединение 2 валентного железа; светло желтые кристаллы, устойчивые на воздухе, плотность 1,85 г/см3. К. г. получали… … Большая советская энциклопедия
-
красная кровяная соль — железосинеродистый калий, гексацианоферриат калия … Cловарь химических синонимов I
-
Обращаемые фотоматериалы — Обращаемые фотоматериалы светочувствительные материалы (фотоплёнка, киноплёнка, фотобумага), позволяющие после лабораторной обработки получать[1] готовое позитивное изображение непосредственно на материале, на который проводилась съёмка, в… … Википедия
-
Микрохимия — К М. в широком смысле должны были бы быть отнесены вообще все методы химического анализа над веществами в минимальных количествах; но обыкновенно к микрохимическим исследованиям причисляют только те, которые связаны с употреблением микроскопа,… … Энциклопедический словарь Ф.А. Брокгауза и И.А. Ефрона
-
Цианистоводородная кислота — (цианистый водород, синильная кислота, формонитрил) HCN; открыта Шееле в 1782 г. при действии железных опилок и разведенной серной кислоты на раствор цианистой ртути: Hg(CN)2 + Fe + H2SO4 = 2HCN + FeSO4 + Hg. Более подробно исследовали ее… … Энциклопедический словарь Ф.А. Брокгауза и И.А. Ефрона
CAS номер: 13943-58-3
Синонимы: Гексацианоферрат (II) калия; Феррицианид калия; Жёлтое синь-кали; Желтая кровяная соль; Potassium ferrocyanide; Potassium hexacyanoferrate(II)
Описание и внешний вид:
Калий железистосинеродистый является неорганическим соединением группы гексацианоферратов. Вещество легко растворяется в воде при этом образует кристаллогидрат. Практически не растворяется в эфире, этилацетате и этиловом спирте. Представляет собой кристаллическое вещество от бесцветного до бледно-желтого цвета. Впервые о получении данного реактива сообщил французский химик Пьер Жозеф Маккер в 1752 году.
Получают вещество промышленным способом из цианистого водорода, хлорида железа и гидроксида кальция. А также из отработанного оксида газовых заводов (очистка газа от цианистого водорода), далее обрабатывают суспензией гидроокиси кальция, затем фильтрат подвергается обработке путем добавления калийной соли и углекислого калия.
Физико-химические свойства:
Химическая формула: C6FeN6•4K или K4[Fe(CN)6]
Молярная масса: 368,34 г/моль
Плотность: 1,886 г/см³
Температура:
— плавления 69-71°C
— разложения 650°C
— кипения 104,2°С
Меры безопасности:
Причинения вреда человеку этим реактивом, научно не доказано, однако ученые и доктора сходятся во мнении, что ферроцианид калия может спровоцировать проблемы с кожей, нарушение работы печени, ЖКТ и интоксикацию организма. Так как вещество содержит в своём составе цианиды, вредные не только для человеческого, но и для водных организмов с долгосрочными последствиями.
Область применения:
Используется в изготовлении пигментов для окрашивания шелка, является компонентом для цианистых соединений, цветной бумаги, ферритов.
Входит в состав ингибирующих покрытий, применяют для цианирования в сталелитейном производстве.
Также используют при выделении и утилизации радиоактивного цезия.
В аналитических исследованиях с его помощью обнаруживают некоторые катионы.
В сельском хозяйстве служит в виде удобрения.
Реактив зарегистрирован как пищевая добавка с индексом Е536.
Используют как добавку к поваренной соли, так как она препятствует комкованию и слеживанию продукта. Нередко добавляют в готовые вкусовые добавки, где содержится соль. Крайне редко используется в процессах изготовления вина, творожных и колбасных продуктов.
| Фасовка | 500 г, 1 кг |
| Квалификация | Чистый |
CAS номер: 13943-58-3
Синонимы: Гексацианоферрат (II) калия; Феррицианид калия; Жёлтое синь-кали; Желтая кровяная соль; Potassium ferrocyanide; Potassium hexacyanoferrate(II)
Описание и внешний вид:
Калий железистосинеродистый является неорганическим соединением группы гексацианоферратов. Вещество легко растворяется в воде при этом образует кристаллогидрат. Практически не растворяется в эфире, этилацетате и этиловом спирте. Представляет собой кристаллическое вещество от бесцветного до бледно-желтого цвета. Впервые о получении данного реактива сообщил французский химик Пьер Жозеф Маккер в 1752 году.
Получают вещество промышленным способом из цианистого водорода, хлорида железа и гидроксида кальция. А также из отработанного оксида газовых заводов (очистка газа от цианистого водорода), далее обрабатывают суспензией гидроокиси кальция, затем фильтрат подвергается обработке путем добавления калийной соли и углекислого калия.
Физико-химические свойства:
Химическая формула: C6FeN6•4K или K4[Fe(CN)6]
Молярная масса: 368,34 г/моль
Плотность: 1,886 г/см³
Температура:
— плавления 69-71°C
— разложения 650°C
— кипения 104,2°С
Меры безопасности:
Причинения вреда человеку этим реактивом, научно не доказано, однако ученые и доктора сходятся во мнении, что ферроцианид калия может спровоцировать проблемы с кожей, нарушение работы печени, ЖКТ и интоксикацию организма. Так как вещество содержит в своём составе цианиды, вредные не только для человеческого, но и для водных организмов с долгосрочными последствиями.
Область применения:
Используется в изготовлении пигментов для окрашивания шелка, является компонентом для цианистых соединений, цветной бумаги, ферритов.
Входит в состав ингибирующих покрытий, применяют для цианирования в сталелитейном производстве.
Также используют при выделении и утилизации радиоактивного цезия.
В аналитических исследованиях с его помощью обнаруживают некоторые катионы.
В сельском хозяйстве служит в виде удобрения.
Реактив зарегистрирован как пищевая добавка с индексом Е536.
Используют как добавку к поваренной соли, так как она препятствует комкованию и слеживанию продукта. Нередко добавляют в готовые вкусовые добавки, где содержится соль. Крайне редко используется в процессах изготовления вина, творожных и колбасных продуктов.
Калий железистосинеродистый
Химическая формула:
K4(Fe(CN)6)*3H2O
Международное название:
POTASSIUM FERROCYANIDE
CAS No:
13943-58-3 (Anhydrous); 14459-95-1 (Trihydrate)
Квалификация:
Имп. «ч», ГОСТ 4207-75
Внешний вид:
кристаллы лимонно-желтого цвета
Фасовка:
мешки, 25 кг
Условия хранения:
в сухом, хорошо проветриваемом помещении
Сделать заказ
Синонимы:
Калия гексацианоферроат, Гексацианоферрат (II) калия, ферроцианид калия, жёлтая кровяная соль
Мы предлагаем Калий железистосинеродистый по выгодным ценам с доставкой по всей России.
| Спецификация | |
|---|---|
| Молекулярный вес | 422.39 |
| Плотность | 1,853 г/см³ при 17 °C. |
| Растворимость в воде | 31,5 г/100 г при 25 °C. |
| Основное вещество, не менее | 99,0% (по факт. 99,5%) |
| Нерастворимый в воде остаток, не более | 0,01% (по факт. 0,005%) |
| Содержание хлоридов, не более | 0,3 % (по факт. 0,15%) |
| Содержание Na, не более | 0,2% (по факт. 0,13%) |
Для согласования условий оплаты, звоните нашим менеджерам по телефонам в Москве:
(495) 787-01-37, 36, 38
(495) 787-43-51
и Санкт- Петербурге
Тел: (812) 309-38-06 (многоканальный)
Калий железистосинеродистый (его также еще называют Гексацианоферратт(II) калия, ферроцианид калия и желтая кровяная соль) — комплексное соединение двухвалентного железа K4[Fe(CN)6], существующее обычно в виде тригидрата K4[Fe(CN)6]·3H2O. Калий железистосинеродистый — светло-жёлтые кристаллы с тетрагональной решеткой. Растворим в воде, практически не растворяется в эфире, этаноле, пиридине, анилине, этилацетате. Калия гексацианоферроат диамагнитен.
Тривиальное название «жёлтая кровяная соль» появилось из-за того, что ранее ее получали путем сплавления отходов с боен (в частности, крови) с поташом и железными опилками. Это, а также жёлтый цвет кристаллов, обусловили название соединения.
Получение
В настоящее время Калий железистосинеродистый в промышленности получают из отработанной массы (содержит цианистые соединения) после очистки газов на газовых заводах; эту массу обрабатывают суспензией Ca(OH)2, фильтрат содержащий Ca2[Fe(CN)6], перерабатывают путём последовательного добавления сначала KCl, а затем K2CO3.
Он так же может быть получен путём взаимодействия суспензии FeS с водным раствором KCN.
Применение
Калия гексацианоферроат применяется
• при изготовлении пигментов,
• крашении шёлка,
• в производстве цианистых соединений, ферритов,
• в производстве цветной бумаги,
• как компонент ингибирующих покрытий
• при цианировании сталей, для выделения и утилизации радиоактивного цезия и др.
• в аналитической химии как реактив для обнаружения некоторых катионов
• в пищевой промышленности ферроцианид калия зарегистрирован в качестве пищевой добавки E536, препятствующей слёживанию и комкованию, например как добавка к поваренной соли и др.
Всегда в наличии по выгодным ценам
В нашем ассортименте всегда в наличии на складе по выгодной цене:
Трилон б,
Оксиэтилендифосфоновая кислота (ОЭДФК),
Ортофосфорная кислота и др.
Для покупки этой и другой химической продукции в Москве или Санкт-Петербурге, звоните нам!
-
Выгодные цены
Даже при изначально низких ценах, мы
предоставляем значительные скидки в
зависимости от объема закупаемой продукции - Быстрая отгрузка
Четкая работа нашего склада позволяет
осуществить быструю отгрузку необходимой
продукции - Высокое качество
Работая напрямую с производителями по всему
миру, мы обеспечиваем наших клиентов
продукцией высокого качества -
Доставка по России
Ускоренная доставка продукции:- автотранспортом;
- железнодорожными контейнерами, вагонами;
- авиатранспортом;
- через транспортные компании.
Для получения подробной информации о ценах на химреактивы
и согласования условий оплаты звоните по телефонам:
в Москве:
+7 (495) 787-01-37
+7 (495) 787-43-51
в Санкт- Петербурге:
+7 (812) 309-38-06


