CAS номер: 139-13-9
Синонимы: 2,2′,2»-Нитрилотриуксусная кислота; N,N-бис(карбоксиметил)глицин; 2-[Бис(карбоксиметил)амино] уксусная кислота; Трис-(карбоксиметил)-амин; NTA; Трилон А; НТА; Комплексон I; Хелатон I; Nitrilotriacetic acid; 2,2′,2′′-Nitrilotriacetic acid; N,N-Bis(carboxymethyl)glycine; Triglycine; Triglycollamic acid; Nitrilotriacetate;
Физико-химические свойства:
Химическая формула: C₆H₉NO₆ или N(СH₂CООН)₃
Молярная масса: 191,1 г/моль
Плотность: 1,6 г/см³
Температура:
— плавления 242°C (разлагается)
— разложения 242°C
Описание и внешний вид:
Нитрилотриуксусная кислота является органическим химическим соединением. Представляет собой бесцветное (белое) твёрдое кристаллическое вещество или порошок, без запаха. Легко растворяется в этиловом спирте, кислотах и щелочах, плохо растворяется в воде и диметилсульфоксиде. Нерастворим в большинстве органических растворителях. Под воздействием высоких температур разлагается на диметиламин, аммиак и диоксид углерода. Получают кислоту из аммиака, формальдегида и цианида водорода или цианида натрия.
Область применения:
Используется для смягчения воды, как хелатируйющий агент и удаления следов щелочноземельных и тяжелых металлов.
Применяется при производстве чистящих и моющих средств.
В лаборатории это соединение используется при комплексонометрическом титровании.
Используется в промышленности, в качестве добавки к краскам и специальным покрытиям.
Меры безопасности:
Горючий при определенных условиях.
Мелкодисперсные частицы образуют в воздухе взрывоопасные смеси, облако из пыли может взорваться при воспламенении в закрытом помещении.
При горении выделяет ядовитые и токсичные пары или газы, оксиды азота.
Воздействие вещества способствуют возникновению сильного раздражения слизистых оболочек глаз, дыхательных путей и кожных покров.
Может причинить значительный вред организму при проглатывании и попадании внутрь организма, вызывает повреждение почек и мочевого пузыря.
Предположительно является канцерогеном для человека, вызывает генетические дефекты, онкологические заболевания, рак.
Стабилен при нормальных условиях использования и хранения.
Хранить рекомендуется в плотно закрытой таре, в прохладном, сухом, хорошо проветриваемом помещении, избегая контакта с несовместимыми веществами, отдельно от сильных окислителей и сильных оснований, вдали от источников тепла, искр или пламени.
При работе необходимо использовать респиратор, спецодежду, защитные перчатки, сапоги и очки.
Запрещается принимать пищу, пить и курить во время работы с реактивом.
| Фасовка | 100 г, 1 кг |
| Квалификация | Чистый |
- О компании
- Контакты
- Условия оплаты
- Условия доставки
- Вопрос-ответ
- Компания
- Новости
- Каталог
- Услуги
- Контакты
- Акции
- Прайс-лист
Нитрилотриуксусная кислота
Нет в наличии
Нашли дешевле?
Цена действительна только для интернет-магазина и может отличаться от цен в розничных магазинах
- Характеристики
- Отзывы о товаре
- Задать вопрос
- Наличие на складе
- Дополнительно
-
Базовая ед. изм.
кгАртикул
580Формула
N(CH2COOH)3Группа фасовки
III, IVПлотность
0CAS#
139-13-9Синонимы
Идранал®I; Трилон А; Трис(карбоксиметил)амин; НТА; Комплексон I; Хелаплекс I -
Вы можете задать любой интересующий вас вопрос по товару или работе магазина.
Наши квалифицированные специалисты обязательно вам помогут.
-
Задать вопрос
- Персональные рекомендации
Нитрилотриуксусная кислота
NTA
Нитрилотриуксусная кислота — это органический хелатирующий агент, используемый для контроля концентрации ионов металлов в водных системах.
Нитрилотриуксусная кислота — белое кристаллическое твердое соединение. Нитрилотриуксусная кислота в основном используется в качестве хелатирующего и элюирующего агента и содержится в моющих средствах для стирки.
Нитрилотриуксусная кислота — это трикарбоновая кислота и NTA.
Нитрилотриуксусная кислота (NTA) представляет собой аминополикарбоновую кислоту с формулой N (CH2CO2H) 3.
Нитрилотриуксусная кислота представляет собой бесцветное твердое вещество, которое используется в качестве хелатирующего агента, который образует координационные соединения с ионами металлов (хелатами), такими как Ca2 +, Co2 +, Cu2 + и Fe3 +.
Нитрилотриуксусная кислота — хелатирующий агент, который образует координационные соединения с ионами металлов. Нитрилотриуксусная кислота используется для комплексометрического титрования, а также для выделения и очистки белков методом His-tag.
Нитрилотриуксусная кислота используется в качестве элюирующего агента при очистке редкоземельных элементов, в качестве добавки к питательной воде котлов, при обработке воды и текстиля, при металлизации и очистке, а также при переработке целлюлозы и бумаги.
КЛЮЧЕВЫЕ СЛОВА:
139-13-9, Нитрилотриуксусная кислота, ТРИЛОН АС, Аминотриуксусная кислота, Комплексон I, НТА, Нитрилотриацетат, Трилон А, Комплексон I, Титриплекс I
EC / Номер списка: 205-355-7
№ CAS: 139-13-9
Мол. формула: C6H9NO6
Нитрилотриуксусная кислота используется в качестве хелатирующего и связывающего агента, а также в качестве компонента синтетических моющих средств.
Он также используется в качестве элюирующего агента при очистке редкоземельных элементов, в качестве добавки к питательной воде для котлов, при обработке воды и текстиля, при нанесении металлических покрытий и очистке, а также при переработке целлюлозы и бумаги.
Нитрилотриуксусная кислота, ее соли и комплексы не встречаются в природе.
Альтернативные названия: N, N-бис (карбоксиметил) глицин; НТА; Трис (карбоксиметил) амин
Применение: Нитрилотриуксусная кислота действует как отличный хелатирующий агент.
Нитрилотриуксусная кислота Химические свойства, применение, производство
Химические свойства
Белый кристаллический порошок. Нерастворим в воде и большинстве органических растворителей; образует одно-, двух- и трехосновные соли, растворимые в воде. Горючие. 70% биоразлагаемый.
Химические свойства
Нитрилотриуксусная кислота — это кристаллическое соединение.
Использует
Нитрилотриуксусная кислота — хелатирующий агент, который образует координационные соединения с ионами металлов. Нитрилотриуксусная кислота используется для комплексометрического титрования, а также для выделения и очистки белков методом His-tag.
Использует
Используется для секвестрации металлов; хелометрический анализ.
Общее описание
Белое твердое вещество без запаха. Тонет и смешивается с водой.
Реакции воздуха и воды
Нерастворим в воде.
Профиль реактивности
Нитрилотриуксусная кислота несовместима с сильными окислителями, алюминием, медью, медным сплавом и никелем. Нитрилотриуксусная кислота также несовместима с сильными основаниями.
Химическая природа: Активным ингредиентом, содержащимся в нитрилотриуксусной кислоте, является нитрилотриуксусная кислота (NTA-H3) с номером CAS. 139-13-9.
Нитрилотриуксусная кислота представляет собой NTA, C6H9NO6, представляет собой аминокарбоновую кислоту с четырьмя функциональными группами.
Внешний вид: Нитрилотриуксусная кислота представляет собой мелкий белый порошок.
Обращение и хранение нитрилотриуксусной кислоты
Материалы
Для резервуаров и бочек можно использовать следующие материалы:
а) Нержавеющая сталь 1.4541 — Нержавеющая сталь AISI 321 (X6 CrNiTi 1810)
б) Нержавеющая сталь 1.4571 — Нержавеющая сталь AISI 316 Ti (X6 CrNiMoTi 17122)
c) Нержавеющая сталь 1.4306 — Нержавеющая сталь AISI 321 L (X2 CrNi 1911)
г) полиэтилен высокой плотности (HDPE)
д) полиэтилен низкой плотности (LDPE)
Срок годности
При правильном хранении и плотно закрытых бочках нитрилотриуксусная кислота имеет срок хранения не менее 36 месяцев в оригинальной упаковке.
Характеристики
Некоторые физические свойства нитрилотриуксусной кислоты перечислены в таблице ниже.
Это только типичные значения, и не все они отслеживаются на регулярной основе.
Они верны на момент публикации и не обязательно являются частью спецификации продукта.
Нитрилотриуксусная кислота Единица Значение
Физическая форма (25 ° C): порошок.
Молекулярная масса (ММ) г / моль: 191.
Концентрация (пот. Титрование раствором FeCl3)
в пересчете на тринатриевую соль (NTA-Na3): прибл. 135%
в пересчете на свободную кислоту (NTA-H3): прибл. 100%
Насыпная плотность (DIN ISO 697, диаметр 40 мм) г / л: прибл. 800
Значение pH (DIN 19268, 1% в воде, 23 ° C): прибл. 2,2 (суспензия)
Кальций-связывающая способность (метод BASF, pH 11) мг CaCO3 / г т. В .: прибл. 525
Содержание воды (DIN EN 13267, Карл Фишер)%: прибл. 0,2
Температура плавления (DIN 51004) ° C: прибл. 245
Растворимость в воде (метод BASF, 25 ° C г в 1 литре: прибл. 1
Распределение частиц
Следующая кривая показывает распределение частиц нитрилотриуксусной кислоты (все значения приблизительны):
Комплексное образование
Наиболее важным свойством нитрилотриуксусной кислоты является ее способность образовывать водорастворимые комплексы с поливалентными ионами (например, кальцием, магнием, свинцом, медью, цинком, кадмием, ртутью, марганцем, железом) в широком диапазоне pH от 2 до 13,5.
NTA обычно образует комплексы 1: 1, т.е. е. 1 моль хелатов NTA связывается с 1 моль ионов металлов, но он также может образовывать комплексы 2: 1 с некоторыми металлами, если присутствует стехиометрический избыток NTA.
Эти комплексы остаются стабильными, особенно в щелочных средах и даже при температурах до 100 ° C.
Из закона действия масс уравнение для константы устойчивости K для комплексов 1: 1 можно записать следующим образом:
[MeZ (m-n) -] K = [Men +] [Zm-]
где
[MeZ (m-n) -] — концентрация образующегося хелата,
[Men +] — это концентрация свободных положительно заряженных ионов металла, [Zm-] — концентрация лиганд-аниона, в данном случае NTA, K — константа стабильности хелата.
Константы логарифмической устойчивости (log K) комплексов MGDA и выбранных ионов металлов:
Ионы металлов log K
Fe3 + 15,9
Hg2 + 14,6
Cu2 + 12,9
Ni2 + 11,5
Pb2 + 11,3
Zn2 + 10,7
Co2 + 10,4
Кd2 + 9.8
Fe2 + 8,3
Mn2 + 7,5
Ca2 + 6,4
Mg2 + 5,5
Ba2 + 4,8
NTA-H3 — это трехосновная кислота, диссоциирующая в три этапа.
Константы кислотной диссоциации pKa следующие.
NTA-H3 pKa1 1,9
НТА-Н2- pKa2 2,5
NTA-H2- pKa3 9,7
В водных растворах нитрилотриуксусная кислота конкурирует за ионы металлов с другими анионами, такими как гидроксид, сульфат, сульфид, карбонат и оксалат, которые образуют труднорастворимые соли металлов.
Образование хелатов снижает концентрацию свободных ионов металлов [Men +] до такой степени, что продукты растворимости многих труднорастворимых солей металлов больше не превышаются.
В результате соли больше не выпадают в осадок или даже могут снова растворяться.
Условные константы стабильности [log Kcond] учитывают константу стабильности K, а также равновесие диссоциации кислотных оснований.
Следующие кривые показывают условные константы стабильности для выбранных хелатов NTA.
Химическая стабильность: Нитрилотриуксусная кислота химически очень стабильна.
Нитрилотриуксусная кислота демонстрирует более высокую стабильность, чем другие органические хелатирующие агенты, такие как лимонная кислота, винная кислота и глюконаты, особенно при повышенных температурах.
В то время как неорганические связывающие агенты (например, фосфаты) могут гидролизоваться при высоких температурах, нитрилотриуксусная кислота устойчива — даже при нагревании до 200 ° C под давлением.
Нитрилотриуксусная кислота плавится прибл. 245 ° С.
Нитрилотриуксусная кислота устойчива к действию сильных кислот и щелочей.
Он постепенно разрушается хромовой кислотой, перманганатом калия и другими сильными окислителями.
Стабильность в присутствии перекиси водорода, перкарбоната и пербората достаточна для совместного нанесения.
Тем не менее, мы не рекомендуем комбинировать нитрилотриуксусную кислоту и пероксиды в жидких составах.
Гипохлорит натрия и другие вещества, выделяющие хлор, вызывают разложение нитрилотриуксусной кислоты.
Разлагаются комплексы щелочноземельных металлов и тяжелых металлов.
Коррозия: нитрилотриуксусная кислота стабилизирует ионы поливалентных металлов, что означает, что она может увеличить скорость растворения металлов.
Тем не менее, за исключением алюминия, для возникновения коррозии всегда должен присутствовать окислитель, такой как воздух.
Нелегированная сталь склонна к коррозии в средах, содержащих воздух, но коррозию можно существенно снизить, если pH находится в щелочном диапазоне, и можно почти полностью устранить, если исключить кислород и другие окислители.
Сталь, очищенная нитрилотриуксусной кислотой в слабощелочном диапазоне, который является оптимальным диапазоном pH для нитрилотриуксусной кислоты, гораздо менее подвержена коррозии, чем если бы ее очищали кислотами.
Единственный тип коррозии, который был связан с нитрилотриуксусной кислотой, — это равномерная коррозия: точечная коррозия или растрескивание под напряжением не наблюдались в средах с низким содержанием хлоридов.
Одним из преимуществ нитрилотриуксусной кислоты является то, что она может поставляться с очень низким содержанием хлоридов.
Следующая информация о материалах носит очень общий характер, поскольку коррозия зависит от многих различных факторов, таких как воздействие воздуха, гальваническая коррозия, вызванная присутствием различных материалов и схемами течения жидкостей.
Совместимость нитрилотриуксусной кислоты с различными материалами необходимо проверять в каждом отдельном случае.
Экология и токсикология: нитрилотриуксусная кислота легко поддается биологическому разложению в стандартных тестах OECD, она полностью минерализована.
и он не образует стойких метаболитов.
Степень удаления нитрилотриуксусной кислоты из-за биоразложения обычно выше, чем на очистных сооружениях, составляет 95%.
Безопасность: Нам неизвестно о каких-либо вредных последствиях, которые могут возникнуть в результате использования нитрилотриуксусной кислоты по назначению и ее обработки в соответствии с существующими практиками.
Согласно накопленному нами за многие годы опыту и другой информации, имеющейся в нашем распоряжении, нитрилотриуксусная кислота не оказывает вредного воздействия на здоровье при условии правильного использования, должное внимание уделяется мерам предосторожности, необходимым при обращении с химическими веществами, а также информации и информации. соблюдаются рекомендации, данные в наших паспортах безопасности.
Маркировка: пожалуйста, обратитесь к текущим Паспортам безопасности для получения информации о классификации и маркировке наших продуктов, а также другой информации, относящейся к безопасности.
Нитрилотриуксусная кислота коммерчески доступна в виде свободной кислоты и в виде натриевой соли. Его получают из аммиака, формальдегида и цианида натрия или цианистого водорода.
Мировая мощность оценивается в 100 тысяч тонн в год.
NTA также образуется в качестве примеси при синтезе EDTA, возникающей в результате реакций с побочным продуктом аммиака.
Координационная химия и приложения
NTA представляет собой триподентный тетрадентатный трианионный лиганд.
Использование NTA аналогично использованию EDTA, поскольку оба являются хелатирующими агентами.
Он используется для смягчения воды и в качестве замены трифосфата натрия и калия в моющих и чистящих средствах.
В одном применении NTA в качестве хелатирующего агента удаляет Cr, Cu и As из древесины, обработанной хромированным арсенатом меди.
Лаборатория использует
В лаборатории это соединение используется при комплексометрическом титровании. Вариант NTA используется для выделения и очистки белка в методе His-tag.
Модифицированный NTA используется для иммобилизации никеля на твердой подложке. Это позволяет очищать белки, содержащие метку, состоящую из шести остатков гистидина на любом конце.
His-tag связывает металл комплексов хелаторов металлов.
Ранее для этой цели использовалась иминодиуксусная кислота. Сейчас чаще используется нитрилотриуксусная кислота.
Для лабораторных исследований используются Ernst Hochuli et al. 1987 г. связывает лиганд NTA и ионы никеля с гранулами агарозы.
Эта Ni-NTA агароза является наиболее часто используемым инструментом для очистки меченных им белков с помощью аффинной хроматографии.
Нитрилотриуксусная кислота
Нитрилотриуксусная кислота
нитрилотриуксусная кислота
NTA
ЕВРОСОЮЗ. Маркировка содержания моющих средств (648/2004)
Имена CAS
Глицин, N, N-бис (карбоксиметил) —
Имена ИЮПАК
2,2 ‘, 2’ ‘- нитрилотриуксусная кислота
2- [бис (карбоксиметил) амино] уксусная кислота
Глицин, N, N-бис (карбоксиметил) —
N, N-бис (карбоксиметил) глицин, NTA, трис (карбоксиметил) амин
Нитрилотриуксусная кислота
Нитрилотриуксусная кислота
нитрилотриуксусная кислота
Нитрилотриуксусная кислота
нитрилотриуксусная кислота
Нитрилотриуксусное название
Nitrilotriessigsäure
НТА кислота
Торговые наименования
Уксусная кислота, нитрилотри-
альфа, альфа, альфа-триметиламинетрикарбоновая кислота
Глицин, N, N-бис (карбоксиметил) —
Нитрило-2,2`, 2`-триуксусная кислота
нитрилотриуксусная кислота
NTA
Синонимы: Chel 300; Комплексон I; HamshipreR NTA кислота; IDRANALR I; Titriplex I; Тригликолламиновая кислота; Триглицин; а, а ‘, а «-триметиламинетрикарбоновая кислота; нитрило-2,2’, 2» -триуксусная кислота; Versene NTA кислота
Синонимы: Нитрило-2,2 ′, 2 ′ ′ — триуксусная кислота; нитрилотрис (метиленкарбоновая кислота); НТА; триглицин; тригликолламиновая кислота; α, α ′, α ′ ′ — триметиламинетрикарбоновая кислота
НИТРИЛОТРИАКУСНАЯ КИСЛОТА И ЕЕ СОЛИ
Это вещество рассматривалось предыдущей рабочей группой в 1989 г. (IARC, 1990).
С тех пор стали доступны новые данные, которые были включены в монографию и учтены в настоящей оценке.
Нитрилотриуксусная кислота
Chem. Abstr. Серв. Рег. №: 139-13-9
Удален CAS Reg. №: 26627-44-1; 26627-45-2; 80751-51-5
Chem. Abstr. Название: N, N-бис (карбоксиметил) глицин
Систематическое название ИЮПАК: Нитрилотриуксусная кислота.
Синонимы: Нитрило-2,2 ′, 2 ′ ′ — триуксусная кислота; нитрилотрис (метиленкарбоновая кислота); НТА, триглицин; тригликолламиновая кислота; α, α ′, α ′ ′ — триметиламинетрикарбоновая кислота
Нитрилотриуксусная кислота, натриевая соль
Chem. Abstr. Серв. Рег. №: 10042-84-9
Chem. Abstr. Название: N, N-бис (карбоксиметил) глицин, натриевая соль
Систематическое название ИЮПАК: Нитрилотриуксусная кислота, натриевая соль.
Синонимы: натриевая соль нитрилотриуксусной кислоты; Натриевая соль NTA; NTA, натриевая соль;
аминотриацетат натрия; нитрилоацетат натрия; нитрилотриацетат натрия; натрий НТА
Нитрилотриуксусная кислота, мононатриевая соль
Chem. Abstr. Серв. Рег. №: 18994-66-6
Chem. Abstr. Название: N, N-бис (карбоксиметил) глицин, мононатриевая соль
Систематическое название ИЮПАК: Нитрилотриуксусная кислота, мононатриевая соль.
Синонимы: нитрилотриацетат натрия; NTA, мононатриевая соль
Нитрилотриуксусная кислота, динатриевая соль
Chem. Abstr. Серв. Рег. №: 15467-20-6
Chem. Abstr. Название: N, N-бис (карбоксиметил) глицин, динатриевая соль
Систематическое название ИЮПАК: Нитрилотриуксусная кислота, динатриевая соль.
Синонимы: Нитрилотриацетат водорода динатрия; нитрилотриацетат динатрия; динатриевая соль нитрилотриуксусной кислоты; NTA, динатриевая соль
Нитрилотриуксусная кислота, динатриевая соль, моногидрат
Chem. Abstr. Серв. Рег. №: 23255-03-0
Chem. Abstr. Название: N, N-бис (карбоксиметил) глицин, динатриевая соль, моногидрат
Систематическое название ИЮПАК: Нитрилотриуксусная кислота, динатриевая соль, моногидрат.
Синонимы: моногидрат нитрилотриуксусной кислоты динатрия; NTA, динатриевая соль, моногидрат
Нитрилотриуксусная кислота, тринатриевая соль
Chem. Abstr. Серв. Рег. №: 5064-31-3
Удален CAS Reg. №: 37291-81-9
Chem. Abstr. Название: N, N-бис (карбоксиметил) глицин, тринатриевая соль
Систематическое название ИЮПАК: Нитрилотриуксусная кислота, тринатриевая соль.
Синонимы: тринатриевая соль нитрилотриуксусной кислоты; Тринатриевая соль NTA; НТА, тринатрий
соль; тринатрий нитрилотриацетат; тринатрий 2,2 ‘, 2’ ‘- нитрилотриацетат; тринатрий НТА
Нитрилотриуксусная кислота, тринатриевая соль, моногидрат
Chem. Abstr. Серв. Рег. №: 18662-53-8
Chem. Abstr. Название: N, N-бис (карбоксиметил) глицин, тринатриевая соль, моногидрат
Систематическое название ИЮПАК: нитрилотриуксусная кислота, тринатриевая соль, моногидрат.
Синонимы: NTA, тринатриевая соль, моногидрат; моногидрат тринатрийнитрилотриацетата
НИТРИЛОТРИАКУСНАЯ КИСЛОТА
139-13-9
2,2 ‘, 2’ ‘- нитрилотриуксусная кислота
Тригликолламиновая кислота
Нитрилотриацетат
Аминотриуксусная кислота
Комплексон I
Трилон А
NTA
Глицин, N, N-бис (карбоксиметил) —
N, N-бис (карбоксиметил) глицин
2- [бис (карбоксиметил) амино] уксусная кислота
Komplexon I
Титриплекс I
Versene NTA кислота
Нитрилотриесигзаер
Гемпширская кислота NTA
Три (карбоксиметил) амин
Трис (карбоксиметил) амин
Уксусная кислота, нитрилотри-
Нитрило-2,2 ‘, 2’ ‘- триуксусная кислота
MFCD00004287
ЧЕЛ 300
NCI-C02766
Нитрилотриуксусная кислота
Нитрилотриуксусная кислота (NTA)
UNII-KA90006V9D
альфа, альфа ‘, альфа’ — триметиламинетрикарбоновая кислота
2- (бис (карбоксиметил) амино) уксусная кислота
ЧЕБИ: 44557
KA90006V9D
Нитрилоацетат
DSSTox_CID_939
DSSTox_RID_75878
Нитрилотриуксусная кислота, 99%
DSSTox_GSID_20939
CAS-139-13-9
CCRIS 436
Аминотриэтановая кислота
N, N-бис (карбоксиметил) глизин
HSDB 2853
Киселина нитрилотриоктова [чешский]
Киселина нитрилотриоктова
NSC 2121
EINECS 205-355-7
BRN 1710776
AI3-52483
H3nta
Нитрилотриацетат кадмия калия
EINECS 256-488-2
нитрилотриуксусная кислота
PubChem15712
WLN: QV1N1VQ1VQ
205-355-7 по К.Э.
Кембридж, идентификатор: 5122183
Nitrilotriessigs
ACMC-1BQ36
N (CH2-COOH) 3
NTA (нитрилотриуксусная кислота)
SCHEMBL20409
4-04-00-02441 (Справочник Beilstein)
KSC176I7T
MLS000069464
BIDD: ER0361
Глицин, N-бис (карбоксиметил) —
Нитрило-2,2 » — триуксусная кислота
CHEMBL1234848
DTXSID6020939
CTK0H6479
NSC2121
HMS2232K17
CCG-2133
НБК-2121
STR02791
ZINC1849692
Нитрилотриуксусная кислота, год, 99%
Tox21_202195
Tox21_300156
ANW-20498
BBL002469
SBB006593
STK387109
АКОС005441655
DB03040
MCULE-5696288379
КС-00000В43
NCGC00091141-01
NCGC00091141-02
NCGC00091141-03
NCGC00091141-04
NCGC00254116-01
NCGC00259744-01
БП-30104
Кадмат (1-), (N, N-бис ((карбокси-каппаО) метил) глицинато (3 -) — каппаN, каппаО) -, калий (1: 1), (Т-4) —
Кадмат (1-), (N, N-бис ((карбокси-каппаО) метил) глицинато (3 -) — каппаN, каппаО) -, калий, (Т-4) —
I536
SMR000054748
2- [бис (карбоксиметил) амино] эфир
DB-042463
FT-0631809
N0098
НИТРИЛОТРИАКУСНАЯ КИСЛОТА ACS МАРКА 100Г
Нитрилотриуксусная кислота, класс Sigma,> = 99%
ST50306920
T7392
C14695
Нитрилотриуксусная кислота, реагент ACS,> = 99,0%
84771-EP2270017A1
84771-EP2301941A1
84771-EP2305808A1
90564-EP2272834A1
90564-EP2301929A1
90564-EP2301935A1
90564-EP2305674A1
90564-EP2372017A1
90564-EP2374780A1
90564-EP2374781A1
Нитрилотриуксусная кислота, BioUltra,> = 99,0% (T)
.альфа., .альфа. » — Триметиламинетрикарбоновая кислота
Q425340
J-007239
F1905-6980
Z1889996324
Нитрилотриуксусная кислота, реактив ACS, для комплексометрии> = 98%
Нитрилотриуксусная кислота, Справочный стандарт фармакопеи США (USP)
(N, N-бис (карбоксиметил) глицинато (3 -) — N, O, O ‘, O’ ‘) кадмат (1-) калия
Токсичность и окружающая среда
Нитрилоуксусная кислота может вызвать раздражение глаз, кожи и дыхательных путей; и может вызвать повреждение почек и мочевого пузыря.
Предполагается, что соединение может вызывать рак у человека.
В отличие от EDTA, NTA легко разлагается микроорганизмами и почти полностью удаляется при очистке сточных вод.
Воздействие NTA на окружающую среду минимально. Несмотря на широкое использование в чистящих средствах, концентрация в воде слишком мала, чтобы оказывать заметное влияние на здоровье человека или качество окружающей среды.
Нитрилотриуксусная кислота
Количество CAS
139-13-9
Синоним
АИ-52483; Аминотриуксусная кислота; н, н-бис (карбоксиметил) глицин; Комплексон I; Гемпширская кислота NTA; NCI-C02766; НТА; Titriplex I; Три (карбоксиметил) амин; Триглицин; TGA; Тригликоламиновая кислота; Трилон А; Versene NTA кислота
Возникновение / использование
Хелатирующий агент в стирке и других моющих средствах; умягчение воды
Продукты VERSENE NTA — хелатирующие агенты общего назначения
ВЕРСЕН NTA 148 — Na3
NTA — используется в чистящих средствах.
ВЕРСЕН NTA 152 — Na3
NTA — хелатирующий агент общего назначения
VERSENE NTA LC — Na3
NTA — Низкоцветная версия VERSENE NTA 148
Кристалл VERSENE NTA — Na3
NTA — Сухая кристаллическая форма VERSENE NTA 148 или VERSENE NTA 152.
ВЕРСЕН НТА кислота — H3
NTA — Сухая кислотная форма VERSENE NTA 148 или VERSENE NTA 152.
Хелатирующий агент VERSENE NTA LC представляет собой низкоцветную версию хелатирующего агента VERSENE NTA 148.
NTA представляет собой легко биоразлагаемый низкомолекулярный хелатирующий агент общего назначения. Согласно определению ОЭСР, он классифицируется как легко разлагаемый микроорганизмами.
Это следует учитывать, когда (1) максимальная стабильность хелатного комплекса металла не требуется; и (2) требуется экономичное хелатирование ионов жесткости при щелочном pH.
версен нта кислота
Название: Нитрилотриуксусная кислота.
CAS: 139-13-9
Молекулярная формула: C6H9NO6
Молекулярный вес: 191,14
ГлавнаяCASCAS 139 CAS 139-13-9
versene nta acid — Имена и идентификаторы
Название Нитрилотриуксусная кислота
Синонимы альфа, альфа ‘, альфа’ ‘- триметиламинетрикарбоновая кислота
аминотриуксусная кислота
чел 300
хэмпширская нта кислота
нитрило-2,2 ‘, 2’ ‘- триуксусная кислота
N, N-бис (карбоксиметил) глицин
NTA
Комплексон I
титриплекс я
три (карбоксиметил) амин
триглицин
тригликолламиновая кислота
Трилон А
версен нта кислота
ai3-52483
Chel300
комплексони
Глицин, N, N-бис (карбоксим
Hampshirentaacid
комплексони
киселинанитрилотриоктова
kyselinanitrilotrioctova (чешский)
Триметиламин-α, α ‘, α ”-трикарбоновая кислота
Нитрило триуксусная кислота
CAS 139-13-9
EINECS 205-355-7
Водоподготовка, Промышленная
Джон М. Донохью, в Энциклопедии физической науки и техники (третье издание), 2003 г.
III.B.3 Хелатирование
Катионы металлов, содержащиеся в котловой воде, такие как кальций, магний, железо и медь, могут растворяться для предотвращения осаждения и образования накипи.
Функциональные агенты в этом типе лечения известны как хелатирующие агенты. Хеланты — это органические анионные химические вещества, которые образуют растворимые соединения с металлами.
Двумя основными хелатирующими химическими веществами, используемыми при очистке промышленных котловых вод, являются этилендиаминтетрауксусная кислота (ЭДТА) и нитрилотриуксусная кислота (НТА).
Хелатирующие агенты добавляются непрерывно в стехиометрическом количестве, необходимом для растворения любых металлических примесей, присутствующих в котловой воде.
Стабильность образующихся металл-хелатных реакционных соединений значительно различается.
EDTA имеет больше координационных центров, чем NTA, и образует более сильные растворимые комплексы с катионами металлов.
Однако ЭДТА, превышающая то, что требуется для хелатирования загрязняющих веществ, может разлагаться в котловой воде, а большие избытки ЭДТА и NTA могут вступить в реакцию с пленкой магнетита (Fe3O4), защищающей бойлер.
Другие анионы, присутствующие в котловой воде (например, фосфат, силикат и гидроксид), имеют тенденцию конкурировать с хелатирующими агентами, ограничивая их эффективность.
По этим причинам химия обработки хелантами должна быть точной.
Частые аналитические испытания питательной и внутренней воды котла необходимы для поддержания надлежащей скорости подачи хелатирующего агента.
Полимерные диспергаторы используются в дополнение к хелатирующей обработке.
Полимеры особенно эффективны для диспергирования оксидов металлов и шламов, образующихся из-за нестабильности хелатов.
Правильное применение хелатно-диспергирующей обработки приводит к чистым поверхностям теплопередачи и эффективной работе котла.
Лечение хелантами
Понимая недостатки химического состава остаточного фосфата в способе борьбы с загрязнением питательной воды (осаждения) жесткостью, были разработаны альтернативные химические методы очистки.
Первым было использование хелаторов для растворения примесей, повышающих твердость. Наиболее распространенными хелантами были этилендиаминтетрауксусная кислота (EDTA) и нитрилотриуксусная кислота (NTA).
И EDTA, и NTA образуют растворимые комплексы с кальцием и магнием, устойчивые к относительно высоким температурам, до 6,8 МПа изб. (1000 фунтов на кв. Дюйм).
Удаление примесей жесткости из котла, теперь уже в растворимой форме, больше не ограничивается ограниченной способностью непрерывной продувки удалять взвешенные твердые частицы из циркулирующей котловой воды.
Если рассматриваемые частицы растворимы в питательной воде, остаются растворимыми в котловой воде и нелетучими, непрерывная продувка удаляет эти частицы со 100% эффективностью.
Теоретически, если бы поддерживалось требуемое стехиометрическое соотношение хелатирующего агента к жесткости, в бойлере не было бы накопления отложений на основе твердости.
Однако на практике уровни жесткости загрязняющих веществ в питательной воде варьируются, и для учета этих изменений необходимо постоянно вносить некоторую избыточную подачу.
Эту избыточную подачу обычно контролируют, чтобы получить небольшую остаточную концентрацию хелатирующего агента в котловой воде, превышающую требуемую для фактической жесткости.
Было обнаружено, что этот остаток хелатирующего агента котловой воды должен контролироваться очень строго, поскольку высокие уровни остатка могут привести к коррозии основного материала котла.
Эта коррозия наиболее вероятна в областях с высокой скоростью жидкости или турбулентностью в котле.
По этой причине контрольные пределы остаточного содержания хелатов варьируются в зависимости от рабочего давления котла и составляют примерно 1–5 мг / л (1–5 частей на миллион).
Хеленты применялись при давлениях в бойлере более 6,8 МПа изб. (1000 фунт / кв. Дюйм изб.) В начале их истории, но позже они обычно применялись только до приблизительно 2,7 МПа (изб.) Для ЭДТА и приблизительно до 6,2 МПа (изб.) Для ЭДТА. NTA.
Нитрилотриуксусная кислота является производным уксусной кислоты, N (CH2COOH) 3. Это комплексообразующий (секвестрирующий) агент, который образует стабильные комплексы также с Zn2 +.
Синонимы
нитрило-2,2 ‘, 2’ ‘- триуксусная кислота
Нитрилотриацетат
Триглицин
Тригликолламиновая кислота
α, α ‘, α’ ‘- триметиламинетрикарбоновая кислота
139-13-9 [RN]
1710776 [Beilstein]
2,2 ‘, 2’ ‘- нитрилотриуксусная кислота [название ACD / IUPAC]
2,2 ‘, 2’ ‘- Nitrilotriessigsäure [немецкий] [название ACD / IUPAC]
205-355-7 [EINECS]
4-04-00-02441 [Байльштейн]
a, a ‘, a’ ‘- Триметиламинетрикарбоновая кислота
Acide 2,2 ‘, 2’ ‘- nitrilotriacétique [французский] [название ACD / IUPAC]
ácido nitrilotriacético [португальский]
AJ0175000
аминотриуксусная кислота
Глицин, N, N-бис (карбоксиметил) — [ACD / название индекса]
KA90006V9D
Kwas nitrylotrioctowy [польский]
Киселина нитрилотриоктова [чешский]
MFCD00004287 [номер в леях]
N, N-бис (карбоксиметокси) глицин
N, N-бис (карбоксиметил) глицин
нитрилоацетат
нитрилотриацетат
нитрилотриуксусная кислота [Wiki]
Нитрилотриесигзаер
NTA
Нтана3
три (карбоксиметил) амин
Триглицин
Тригликолламиновая кислота
Трис (карбоксиметил) амин
UNII-KA90006V9D
α, α ‘, α’ ‘- Триметиламинетрикарбоновая кислота
(Бис-карбоксиметиламино) уксусная кислота
2- (бис (карбоксиметил) амино) уксусная кислота
2- (бис (карбоксиметил) амино) этановая кислота
2,2 ‘, 2’ ‘- нитрилотриуксусная кислота (нежелательное название)
2- [бис (карбоксиметил) амино] уксусная кислота
2- [Бис (карбоксиметил) амино] уксусная кислота, NTA
уксусная кислота, нитрилотри-
Аминотриэтановая кислота
Бензойная кислота, 4- (аминометил) — (9Cl)
Комплексон I [Торговое наименование]
Глицин, N, N-бис (карбоксиметил) —
H3nta
http://en.atomaxchem.com/139-13-9.html
https://www.ebi.ac.uk/chebi/searchId.do?chebiId=CHEBI:44557
IDRANAL [Торговое наименование]
IDRANAL I [Торговое наименование]
Komplexon I [Торговое наименование]
N, N-бис (карбоксиметил) -глицин
N, N-бис (карбоксиметил) глизин
Нитрило-2,2 ‘, 2’ ‘- триуксусная кислота
нитрило-2,2 ‘, 2’ ‘- триуксусная кислота
нитрило-триуксусная кислота
нитрилотриуксусная кислота 98%
нитрилотриуксусная кислота, 99%
нитрилотриуксусная кислота, cp
нитрилотриуксусная кислота, реактив, ац
QV1N1VQ1VQ [WLN]
STR02791
титриплекс я
Титриплекс (R) I
тригликолламиновая кислота 98,5%
Трилон А
α, α ‘, α’ ‘- триметиламинетрикарбоновая кислота
Классификация ролей
Химическая роль: кислота Бренстеда
Молекулярный объект, способный отдавать гидрон акцептору (основание Бренстеда).
(через оксокислоту)
хелатор
Лиганд с двумя или более отдельными сайтами связывания, которые могут связываться с одним центральным атомом металла, образуя хелат.
(через NTA)
База Бронстеда
Молекулярный объект, способный принимать гидрон от донора (кислота Бренстеда).
(через органическое аминосоединение)
нитрилотриуксусная кислота является NTA
нитрилотриуксусная кислота — трикарбоновая кислота
нитрилотриуксусная кислота — сопряженная кислота нитрилотриацетата (1-)
Входящий
2,2 ‘- [(2-амино-2-оксоэтил) имино] диуксусная кислота имеет функциональную исходную нитрилотриуксусную кислоту.
нитрилотриацетат (1-) представляет собой сопряженное основание нитрилотриуксусной кислоты
Название ИЮПАК
N, N-бис (карбоксиметил) глицин
Название ИЮПАК
N, N-бис (карбоксиметил) глицин
Синонимы
α, α ‘, α’ ‘- триметиламинетрикарбоновая кислота
Complexon I Deutsch
H3nta
Komplexon I
N (CH2 ‒ COOH) 3
нитрило-2,2 ‘, 2’ ‘- триуксусная кислота
Нитрилотриацетат
НИТРИЛОТРИАКУСНАЯ КИСЛОТА
Нитрилотриуксусная кислота
Nitrilotriessigsäure
NTA
три (карбоксиметил) амин
триглицин
Тригликолламиновая кислота
Трилон А
Нитрилотриуксусная кислота (NTA) или ее производные присутствуют во многих сложных структурах, в которых атом металла связан с несколькими атомами полидентатного комплексообразователя. Однако известно лишь несколько структур нехелатированных кислот, анионов или производных NTA: нитрилотриуксусная кислота (Stanford, 1967); дигидрат нитрилотриацетата кальция (Whitlow, 1972); 2,2 ‘, 2 «-нитрилотриэтанол (Mootz, Brodalla & Wiebcke, 1989); N-метилнитрилотриацетамид (Skrzypczak-Jankun & Smith, 1994a).
В последних двух из этих структур центральный атом N не протонирован, связи N — C короче (1,467 и 1,463, A соответственно), а углы C — N — C меньше (110,7 и 110,9 °, соответственно), чем в протонированных соединениях.
В CaNTA.2H20 пять из шести атомов O NTA связаны с ионами металлов, но каждый атом O присоединен к другому иону Ca, так что цвиттер-ион NTA является не хелатирующим лигандом, а частью трехмерной ионной сети. аналогично тому, что видно в самом NTA
Нитрилотриуксусная кислота участвует в качестве мультидентатного лиганда во многих хелатирующих соединениях металлов: A1, B, Bi, Ca, Co, Cr, Cu, Fe, Mo, Nd, Ni, Pb, Ti, W, Zn и Zr.
Структура этого популярного лиганда была уточнена и сравнена со структурой дигидрата нитрилотриацетата кальция [Whitlow (1972).
Acta Cryst. B28, 1914-1919], которая представляет собой другую структуру, в которой на этот лиганд не влияет хелатирование.
Согласно данным, представленным в соответствии с разделом 71 CEPA 1999 и из других общедоступных источников, NTA, как сообщается, используется в Канаде в промышленных и промышленных чистящих средствах, средствах для чистки транспортных средств, асфальте, удобрениях, растворах для проявки фотографий и средствах для удаления накипи для добычи нефти и горнодобывающей промышленности деятельности (Environment Canada 2009a). Согласно информации, содержащейся в доступной литературе, чистящие средства для учреждений и промышленных предприятий составляют самое крупное применение NTA в Канаде; к ним относятся общие чистящие средства, обезжириватели, средства для мытья автомобилей, дезинфицирующие средства, дезинфицирующие средства, моющие средства для стирки и моющие средства для механических посудомоечных машин (Mueller et al. 2006; Glauser et al. 2007; Ahmed 2009).
Другие применения NTA в Канаде связаны с его функцией в качестве хелатирующего агента в различных промышленных процессах, таких как обработка котловой воды и целлюлозно-бумажные процессы для производства изделий из бумаги и картона.
Ранее НТА предлагался в научной литературе в качестве терапевтического хелатирующего агента при отравлении марганцем и для лечения перегрузки железом.
NTA — известная примесь в этилендиаминтетрауксусной кислоте (ЭДТА) и ее солях, в совокупности известные как эдетаты (Dow Chemical Company 1987; Crosbie et al. 2003; Hart 2005).
Эдетаты представляют собой хелатирующие агенты, которые можно использовать в бытовых чистящих средствах, косметических составах, пищевых продуктах, сельскохозяйственных продуктах, фармацевтических продуктах и промышленных процессах (Hart 2005). Эдетаты также используются для лечения отравлений тяжелыми металлами и для снижения уровня холестерина в крови (Lanigan and Yamarik 2002). В соответствии с Фармакопеей США (USP 2000a, b, c), Европейской фармакопеей (EP 2001) и Кодексом пищевых химикатов (электронные письма 2009 г. от Управления пищевых продуктов Министерства здравоохранения Канады в Бюро управления рисками Министерства здравоохранения Канады; без ссылок), максимальный предел NTA в эдетатах составляет 0,1% по весу.
Тринатриевая соль нитрилотриуксусной кислоты NTA 3NA
Описание
Синонимы: Трилон А, Нитрилотриуксусная кислота тринатриевая соль
CAS №: 5064-31-3
Химическая формула: С6Н6NO6Na3
Тринатриевая соль нитрилотриуксусной кислоты или Трилон А высококачественный комплексообразователь, образовывает стабильные хелаты с поливалентными ионами металлов в широком диапазоне рН. Биоразлагаемый комплексообразователь: высушенная тринатриевая соль НУК, сохраняет стабильность в условиях высоких температур (> 150 С)
Применение
Трилон А используется в производстве бытовой химии и синтетических моющих средств, в виде стабилизатора в процессах полимеризации, целлюлозно-бумажной индустрии, в теплоэнергетике при чистке теплообменников и котлов от отложений солей, при производстве каучука, и в многих других областях.
Характеристики
|
Наименование показателя |
Результаты |
|
Внешний вид |
Белый кристаллический порошок |
|
Содержание основного вещества, %, не менее |
92,00 |
|
Массовая доля железа (Fe) , %, не более |
0,001 |
|
Массовая доля тяжёлых металлов (Pb), %, не более |
0,001 |
|
pН (1% раствора) |
10,5 – 11,5 |
Упаковка и условия хранения
Полипропиленовый мешок с полиэтиленовым мешком-вкладышем 25 кг.
Хранение в крытых сухих складских помещениях.
Гарантийный срок хранения 36 месяцев со дня изготовления.
- Выдавший орган
- Роспотребнадзор (Федеральная Служба)
- Типографский номер бланка
- 191934
- Продукция
- Trilon AS; Наименование вещества: Нитрилотриуксусная кислота; синонимы и торговое название: N,N-Бис(карбоксиметил)глицин; три(карбокси-метил)амин; альфа,альфа’,альфа’ ‘-триметиламинотрикабоновая кислота (CAS: 139-13-9) (ЕС: 205-355-7)
- Изготовлена в соответствии с документами
- лист безопасности (MSDS)
- Продукция соответствует
- Единым санитарно-эпидемиологическим и гигиеническим требованиям к товарам, подлежащим санитарно-эпидемиологическому надзору (контролю)
- Изготовитель (производитель)
- BASF SE (БАСФ СЕ), Carl-Bosch-Strasse, 38, D-67056 Ludwigshafen, Germany, (Производственный филиал: BASF Corporation, 100 Campus Drive, Florham Park, NJ 07932-1089, USA) (ФРГ)
- Получатель
- ЗАО «БАСФ», 119017, г. Москва, Кадашевская наб., д. 14, к. 3 (Российская Федерация)
- Область применения
- комплексообразующие реагенты для использования в промышленности и бытовой химии.
- Протоколы исследований
- экспертное заключение о токсичности и опасности вещества ФБУЗ «Российский регистр потенциально опасных химических и биологических веществ» Роспотребнадзора № 07/22-2894 от 23.12.2011 г.; Информационная карта потенциально опасного химического и биологического вещества серия ВТ № 003611; лист безопасности продукции, спецификация, макет этикетки
- Этикетка
- наименование продукции, страна, фирма-изготовитель, меры безопасности при обращении с продуктом
- Гигиеническая характеристика
-
Острая токсичность: продукт по параметрам острой токсичности при однократном внутрижелудочном введении отнесен к умеренно опасным веществам (3 класс опасности), при ингаляционном поступлении в организм — к высокоопасным веществам (2 класс опасности). Кумулятивность: обладает слабой кумулятивной способностью. Продукт выраженно раздражает кожу и слизистые оболочки глаз. Может проникать через неповрежденные кожные покровы. Обладает мутагенным эффектом в экспериментах на животных и клетках человека.
Документ получен с сервера поиска по Реестрам Роспотребнадзора и санитарно-эпидемиологической службы России
- Справочник
- Справочник структурных формул
- н
- Нитрилотриуксусная кислота
Нитрилотриуксусная кислота
HO/O`/|N<|`/`O|OH>/|O`|/OH
HO<=O>`/N<-<=O>`/HO>`/`-<`\O>`/HO
Ca_(y-1.5)N`_q<`=O>_q6O_#1; #N_(x.5,y-.7)_(x.4,y.8)<_(A-60,N2)O>_(x-.2,y.6)O_(d-)#1; #N/_p<=O>_p6O_#1; #1_(A140,L1.2,w+)H2O; OH2_(A-140,L1.2,w-)#1_(y1.5)OH2; «[«_(x3,N0)#1_(x3,N0)»]»^-
N(CH2COOH)3
Брутто-формула: C6H9NO6
Молекулярная масса: 191.139
Химический состав
| Символ | Элемент | Атомный вес | Число атомов | Процент массы |
|---|---|---|---|---|
| C | Углерод (Carbon) | 12.011 | 6 | 37.7% |
| H | Водород (Hydrogen) | 1.008 | 9 | 4.7% |
| N | Азот (Nitrogen) | 14.007 | 1 | 7.3% |
| O | Кислород (Oxygen) | 15.999 | 6 | 50.2% |
Синонимы
- НТА
- Нитрилотриуксусная кислота
- комплексон I
- трилон А
- хелатон I
- 2-[bis(carboxymethyl)amino]acetic acid(IUPAC)
- Aminotriacetic acid
- Complexon I
- Glycine, N,N-bis(carboxymethyl)-Glycine, N,N-bis(carboxymethyl)-(CAS)
- Hampshire NTA acid
- NSC 2121
- NTA
- NTA N,N-Bis(carboxymethyl)glycine
- Nitrilotriacetic Acid
- Titriplex I
- Tricollamic acid
- Triglycine
- Triglycollamic acid
- Trilon A
- Versene NTA acid
Входит в группы
Карбоновые кислоты Хелаторы
From Wikipedia, the free encyclopedia
|
|
| Names | |
|---|---|
| Preferred IUPAC name
2,2′,2′′-Nitrilotriacetic acid[3] |
|
| Other names
N,N-Bis(carboxymethyl)glycine |
|
| Identifiers | |
|
CAS Number |
|
|
3D model (JSmol) |
|
|
Beilstein Reference |
1710776 |
| ChEBI |
|
| ChemSpider |
|
| DrugBank |
|
| ECHA InfoCard | 100.004.869 |
| EC Number |
|
|
Gmelin Reference |
3726 |
| KEGG |
|
| MeSH | Nitrilotriacetic+Acid |
|
PubChem CID |
|
| RTECS number |
|
| UNII |
|
| UN number | 2811 |
|
CompTox Dashboard (EPA) |
|
|
InChI
|
|
|
SMILES
|
|
| Properties | |
|
Chemical formula |
C6H9NO6 |
| Molar mass | 191.14 [4] |
| Appearance | White crystals |
| Melting point | 246[4] °C (475 °F; 519 K) |
|
Solubility in water |
Insoluble. <0.01 g/100 mL at 23°C [4] |
| Thermochemistry | |
|
Std enthalpy of |
−1.3130–−1.3108 MJ mol−1 |
| Hazards | |
| GHS labelling: | |
|
Pictograms |
 
|
|
Signal word |
Warning |
|
Hazard statements |
H302, H319, H351 |
|
Precautionary statements |
P281, P305+P351+P338 |
| Flash point | 100 °C (212 °F; 373 K) |
| Lethal dose or concentration (LD, LC): | |
|
LD50 (median dose) |
1.1 g kg−1 (oral, rat) |
| Related compounds | |
|
Related alkanoic acids |
|
|
Related compounds |
|
|
Except where otherwise noted, data are given for materials in their standard state (at 25 °C [77 °F], 100 kPa).
Infobox references |
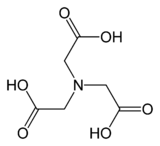
Nitrilotriacetic acid (NTA) is the aminopolycarboxylic acid with the formula N(CH2CO2H)3. It is a colourless solid that is used as a chelating agent, which forms coordination compounds with metal ions (chelates) such as Ca2+, Co2+, Cu2+, and Fe3+.[5]
Production and use[edit]
Nitrilotriacetic acid is commercially available as the free acid and as the sodium salt. It is produced from ammonia, formaldehyde, and sodium cyanide or hydrogen cyanide. Worldwide capacity is estimated at 100 thousand tonnes per year.[6] NTA is also cogenerated as an impurity in the synthesis of EDTA, arising from reactions of the ammonia coproduct.[7] Older routes to NTA included alkylation of ammonia with chloroacetic acid and oxidation of triethanolamine.
Coordination chemistry and applications[edit]
NTA is a tripodal tetradentate trianionic ligand.[8]
The uses of NTA are similar to those of EDTA, both being chelating agents. It is used for water softening and as a replacement to sodium and potassium triphosphate in detergents, and cleansers.
In one application, NTA as a chelating agent removes Cr, Cu, and As from wood that had been treated with chromated copper arsenate.[9]
Laboratory uses[edit]
In the laboratory, this compound is used in complexometric titrations. A variant of NTA is used for protein isolation and purification in the His-tag method.[10] The modified NTA is used to immobilize nickel on a solid support. This allows purification of proteins containing a tag consisting of six histidine residues at either terminus.[11]
The his-tag binds the metal of metal chelator complexes. Previously, iminodiacetic acid was used for that purpose. Now, nitrilotriacetic acid is more commonly used.[12]
For laboratory uses Ernst Hochuli et al. 1987 coupled the NTA ligand and Nickel-ions to agarose beads.[13] This Ni-NTA Agarose is the most used tool to purify his tagged proteins via affinity chromatography.
- NTA complexes
-
Three views of the structure of [Ni(NTA)(H2O)2]−.
-
Structure of the nitrilotriacetate anion [Ca(NTA)(H2O)3]−.
Toxicity and environment[edit]
Nitriloacetic acid can cause eye, skin, and respiratory tract irritation; and can cause kidney and bladder damage. The compound is anticipated to have the potential to cause human cancers.[1]
In contrast to EDTA, NTA is easily biodegradable and is almost completely removed during wastewater treatment.[6] The environmental impacts of NTA are minimal. Despite widespread use in cleaning products, the concentration in the water supply is too low to have a sizeable impact on human health or environmental quality.[14]
References[edit]
- ^ a b «Nitrilotriacetic Acid — Compound Summary». PubChem Compound. USA: National Center for Biotechnology Information. 26 March 2005. Identification. Retrieved 13 July 2012.
- ^ Nitrilotriacetic acid
- ^ Favre, Henri A.; Powell, Warren H. (2014). Nomenclature of Organic Chemistry : IUPAC Recommendations and Preferred Names 2013 (Blue Book). Cambridge: The Royal Society of Chemistry. pp. 21, 679. doi:10.1039/9781849733069. ISBN 978-0-85404-182-4.
- ^ a b c ChemBK Chemical Database http://www.chembk.com/en/chem/Nitrilotriacetic%20acid
- ^ Nitrilotriacetic Acid and Its Salts, International Agency for Research on Cancer
- ^ a b Thomas Schmidt, Charalampos Gousetis, Hans-Joachim Opgenorth (2022). «Nitrilotriacetic Acid». Ullmann’s Encyclopedia of Industrial Chemistry. Weinheim: Wiley-VCH. doi:10.1002/14356007.a17_377.pub3.
{{cite encyclopedia}}: CS1 maint: multiple names: authors list (link) - ^ Hart, J. Roger (2005) «Ethylenediaminetetraacetic Acid and Related Chelating Agents» in Ullmann’s Encyclopedia of Industrial Chemistry, Wiley-VCH, Weinheim. doi:10.1002/14356007.a10_095
- ^ B. L. Barnett, V. A. Uchtman (1979). «Structural Investigations of Calcium-Binding Molecules. 4. Calcium Binding to Aminocarboxylates. Crystal Structures of Ca(CaEDTA).7H2O and Na(CaNTA)». Inorg. Chem. 18 (10): 2674–2678. doi:10.1021/ic50200a007.
- ^ Fang-Chih, C.; Ya-Nang, W.; Pin-Jui, C.; Chun-Han, K. Factors affecting chelating extraction of Cr, Cu, and As from CCA-treated wood. J. Environ. Manag. 2013, 122.
- ^ Liu, Weijing (2016). «Layer-by-Layer Deposition with Polymers Containing Nitrilotriacetate, A Convenient Route to Fabricate Metal- and Protein-Binding Films». ACS Applied Materials & Interfaces. 8 (16): 10164–73. doi:10.1021/acsami.6b00896. PMID 27042860.
- ^ qiaexpressionist
- ^ Lauer, Sabine A.; Nolan, John P. (2002). «Development and characterization of Ni-NTA-bearing microspheres». Cytometry. 48 (3): 136–145. doi:10.1002/cyto.10124. ISSN 1097-0320. PMID 12116359.
- ^ Hochuli, E.; Döbeli, H.; Schacher, A. (January 1987). «New metal chelate adsorbent selective for proteins and peptides containing neighbouring histidine residues». Journal of Chromatography A. 411: 177–184. doi:10.1016/s0021-9673(00)93969-4. ISSN 0021-9673. PMID 3443622.
- ^ Brouwer, N.; Terpstra, P. Ecological and Toxicological Properties of Nitrilotriacetic Acid (NTA) as a Detergent Builder. Tenside Surfactants Detergents 1995, 32, 225-228.
22 ноября 2017
4634
Тринатриевая соль нитрилотриуксусной кислоты (аналог Трилона А / Trilon A92R*)
Описание
Химическое название вещества по IUPAC: Нитрилотриацетат тринатрия
CAS No. 5064-31-3
Молекулярная (эмпирическая) формула: C6H9NNa3O7
Молекулярный вес: 275.0995
Технические характеристики
| наименование | значение |
|---|---|
| внешний вид | белые кристаллы |
| содержание основного вещества, % | ≥ 99.0 |
| содержание тяжелых металлов: | |
| Свинец (Pb), % | ≤ 0.001 % |
| Мышьяк (As), % | ≤ 0.0002 % |
| Железо (Fe ) % | ≤ 0.001 % |
| Цветность по шкале APHA | ≤ 20 |
| Частиц размером 40меш | ≥ 70% |
| pH 2% р-ра | 10.5-11.5 |
Синонимы
N,N-Бис(карбоксиметил)глицин тринатрия; аминотриацетат тринатрия
Торговые названия
Нитрилотриуксусная кислота тринатриевая соль (NITRILOTRIACETIC ACID, TRISODIUM SALT, NTA 3NA); продукт Диссолвин А-40, Dissolvine A-40, VERSENE 100

![Three views of the structure of [Ni(NTA)(H2O)2]−.](https://upload.wikimedia.org/wikipedia/commons/thumb/1/14/Ni%28NTA%29%28aq%2923views.png/500px-Ni%28NTA%29%28aq%2923views.png)
![Structure of the nitrilotriacetate anion [Ca(NTA)(H2O)3]−.](https://upload.wikimedia.org/wikipedia/commons/thumb/0/06/Calcium_complex_of_NTA_trianion.svg/210px-Calcium_complex_of_NTA_trianion.svg.png)
