Поиск по сайту:
Синонимы. Метаарсенит натрия.
Скачать страницу
[Выходные данные]
| Метаарсенит натрия | |
 |
|
| Общие | |
|---|---|
| Систематическое наименование | Метаарсенит натрия |
| Традиционные названия | Метаарсенат(III) натрия, мышьяковистокислый (мета) натрий |
| Химическая формула | NaAsO2 |
| Физические свойства | |
| Молярная масса | 129,90 г/моль |
| Плотность | 1,87 г/см³ |
| Термические свойства | |
| Температура плавления | разл. 550 °C |
| Химические свойства | |
| Растворимость в воде | 15625 г/100 мл |
| Классификация | |
| Рег. номер CAS | 7784-46-5 |
| Рег. номер PubChem | 443495 |
| Безопасность | |
| ЛД50 | 40 мг/кг |
Метаарсенит натрия — неорганическое соединение, соль щелочного металла натрия и метамышьяковистой кислоты с формулой NaAsO2, бесцветные кристаллы, растворимые в воде.
Получение
- Растворение мышьяка в кипящем растворе едкого натра:
- Растворение триоксида мышьяка в разбавленном растворе щёлочи:
- или концентрированном растворе карбоната натрия:
Физические свойства
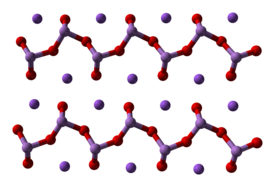
Метаарсенит натрия образует бесцветные кристаллы в котором анионы AsO2— образуют бесконечные цепочки.
Хорошо растворяется в холодной воде с частичным гидролизом по аниону.
Химические свойства
- При нагревании разлагается (диспропорционирует):
- Разлагается горячей водой:
- Медленно окисляется кислородом воздуха:
- В щелочных растворах окисление идёт иначе:
- Реагирует в разбавленными кислотами:
- и концентрированными:
- Реагирует с щелочами:
- Может окисляться:
- и восстанавливаться:
- Вступает в обменные реакции:
Литература
- Химическая энциклопедия / Редкол.: Кнунянц И.Л. и др.. — М.: Советская энциклопедия, 1988. — Т. 1. — 623 с.
- Справочник химика / Редкол.: Никольский Б.П. и др.. — 3-е изд., испр. — Л.: Химия, 1971. — Т. 2. — 1168 с.
- Лидин Р.А. и др. Химические свойства неорганических веществ: Учеб. пособие для вузов. — 3-е изд., испр. — М.: Химия, 2000. — 480 с. — ISBN 5-7245-1163-0
| Метаарсенит натрия | |
|---|---|
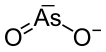  |
|
| Общие | |
| Систематическое наименование |
Метаарсенит натрия |
| Традиционные названия | Метаарсенат(III) натрия, мышьяковистокислый (мета) натрий |
| Хим. формула | NaAsO2 |
| Физические свойства | |
| Молярная масса | 129,90 г/моль |
| Плотность | 1,87 г/см³ |
| Термические свойства | |
| Температура | |
| • плавления | разл. 550 °C |
| Химические свойства | |
| Растворимость | |
| • в воде | 15625 г/100 мл |
| Классификация | |
| Рег. номер CAS | 7784-46-5 |
| PubChem | 443495 |
| Безопасность | |
| ЛД50 | 40 мг/кг |
| Приведены данные для стандартных условий (25 °C, 100 кПа), если не указано иное. |
Метаарсенит натрия — неорганическое соединение, соль щелочного металла натрия и метамышьяковистой кислоты с формулой NaAsO2, бесцветные кристаллы, растворимые в воде.
Получение
- Растворение мышьяка в кипящем растворе едкого натра:
-
- [math]displaystyle{ mathsf{2As + 2NaOH + 2H_2O xrightarrow{100^oC} 2NaAsO_2 + 3H_2uparrow } }[/math]
- Растворение триоксида мышьяка в разбавленном растворе щёлочи:
-
- [math]displaystyle{ mathsf{As_2O_3 + 2NaOH xrightarrow{} 2NaAsO_2 + H_2O } }[/math]
- или концентрированном растворе карбоната натрия:
-
- [math]displaystyle{ mathsf{As_2O_3 + Na_2CO_3 xrightarrow{100^oC} 2NaAsO_2 + CO_2uparrow } }[/math]
Физические свойства
Метаарсенит натрия образует бесцветные кристаллы в котором анионы AsO2— образуют бесконечные цепочки.
Хорошо растворяется в холодной воде с частичным гидролизом по аниону.
Химические свойства
- При нагревании разлагается (диспропорционирует):
-
- [math]displaystyle{ mathsf{5NaAsO_2 xrightarrow{300-550^oC} Na_3AsO_4 + 2NaAsO_3 + 2As } }[/math]
- Разлагается горячей водой с образованием дигидроарсенита натрия:
-
- [math]displaystyle{ mathsf{NaAsO_2 + H_2O xrightarrow{100^oC} NaH_2AsO_3 } }[/math]
- Медленно окисляется кислородом воздуха:
-
- [math]displaystyle{ mathsf{2NaAsO_2 + O_2 xrightarrow{} 2NaAsO_3 } }[/math]
- В щелочных растворах окисление идёт иначе:
-
- [math]displaystyle{ mathsf{2NaAsO_2 + O_2 + 2NaOH xrightarrow{CuSO_4} 2Na_2HAsO_4 } }[/math]
- Реагирует в разбавленными кислотами:
-
- [math]displaystyle{ mathsf{2NaAsO_2 + 2HCl xrightarrow{} As_2O_3downarrow + 2NaCl + H_2O } }[/math]
- и концентрированными:
-
- [math]displaystyle{ mathsf{NaAsO_2 + 4HCl xrightarrow{} AsCl_3 + NaCl + 2H_2O } }[/math]
- Реагирует с щелочами с образованием гидроарсенита натрия:
-
- [math]displaystyle{ mathsf{NaAsO_2 + NaOH xrightarrow{} Na_2HAsO_3 } }[/math]
- Может окисляться:
-
- [math]displaystyle{ mathsf{NaAsO_2 + NaClO + 2NaOH xrightarrow{} Na_3AsO_4 + NaCl + H_2O } }[/math]
- и восстанавливаться:
-
- [math]displaystyle{ mathsf{2NaAsO_2 + 3SnCl_2 + 14HCl xrightarrow{} 2Asdownarrow + 3H_2[SnCl_6] + 2NaCl + 4H_2O } }[/math]
- Вступает в обменные реакции:
-
- [math]displaystyle{ mathsf{NaAsO_2 + AgNO_3 xrightarrow{} AgAsO_2downarrow + NaNO_3 } }[/math]
Литература
- Химическая энциклопедия / Редкол.: Кнунянц И.Л. и др.. — М.: Советская энциклопедия, 1988. — Т. 1. — 623 с.
- Справочник химика / Редкол.: Никольский Б.П. и др.. — 3-е изд., испр. — Л.: Химия, 1971. — Т. 2. — 1168 с.
- Лидин Р.А. и др. Химические свойства неорганических веществ: Учеб. пособие для вузов. — 3-е изд., испр. — М.: Химия, 2000. — 480 с. — ISBN 5-7245-1163-0.

Метаарсенит натрия — неорганическое соединение, соль щелочного металла натрия и метамышьяковистой кислоты с формулой NaAsO2, бесцветные кристаллы, растворимые в воде.
| Метаарсенит натрия | |
|---|---|
| Общие | |
| Систематическое наименование |
Метаарсенит натрия |
| Традиционные названия | Метаарсенат(III) натрия, мышьяковистокислый (мета) натрий |
| Хим. формула | NaAsO2 |
| Физические свойства | |
| Молярная масса | 129,90 г/моль |
| Плотность | 1,87 г/см³ |
| Термические свойства | |
| Температура | |
| • плавления | разл. 550 °C |
| Химические свойства | |
| Растворимость | |
| • в воде | 15625 г/100 мл |
| Классификация | |
| Рег. номер CAS | 7784-46-5 |
| PubChem | 443495 |
| Рег. номер EINECS | 232-070-5 |
| SMILES |
[O-][As]=O.[Na+] |
| InChI |
1S/AsHO2.Na/c2-1-3;/h(H,2,3);/q;+1/p-1 PTLRDCMBXHILCL-UHFFFAOYSA-M |
| RTECS | CG3675000 |
| ChEBI | 29678 |
| ChemSpider | 22980 |
| Безопасность | |
| ЛД50 | 40 мг/кг |
| NFPA 704 |
Получение
- Растворение мышьяка в кипящем растворе едкого натра:
- Медленно окисляется кислородом воздуха:
- В щелочных растворах окисление идёт иначе:
- Реагирует в разбавленными кислотами:
- Может окисляться:
- и восстанавливаться:
Метаарсенит натрия
Другие названия: .Метаарсенат(III) натрия, мышьяковистокислый (мета) натрий
Метаарсенит натрия — неорганическое соединение с химической формулой NaAsO2.
Физические свойства
| Молярная масса | 129,911 г/моль |
| Температура кипения, tкип. | 550 разл.°C |
| Плотность, ρ | 1,87 г/см3 |
Химические свойства и методы получения
Список использованной литературы
- Волков, А.И., Жарский, И.М. Большой химический справочник / А.И. Волков, И.М. Жарский. — Мн.: Современная школа, 2005. — 608 с ISBN 985-6751-04-7. [c. 139]
Справочник содержит названия веществ и описания химических формул (в т.ч. структурные формулы и скелетные формулы).
Введите часть названия или формулу для поиска:
Общее число найденных записей: 1.
Показано записей: 1.
Метаарсенит натрия
Брутто-формула:
AsNaO2
CAS# 7784-46-5
Названия
Русский:
- Метаарсенат(III) натрия
- Метаарсенит натрия [Wiki]
- мышьяковистокислый (мета) натрий
- соль натрия и метамышьяковистой кислоты
English:
- EINECS:232-070-5
- Prodaluminol Double
- Sodium arsenite [Wiki]
- Sodium m-arsenite
- sodium meta-arsenite
- sodium;oxoarsinite(IUPAC)
Варианты формулы:
Реакции, в которых участвует Метаарсенит натрия
-
5NaAsO2 «300-550^oC»—> Na3AsO4 + 2NaAsO3 + 2As
-
NaAsO2 + NaClO + 2NaOH -> Na3AsO4 + NaCl + H2O
-
2As + 2NaOH + 2H2O «100^oC»—> 2NaAsO2 + 3H2″|^»
-
As2O3 + 2NaOH -> 2NaAsO2 + H2O
-
As2O3 + Na2CO3 «100^oC»—> 2NaAsO2 + CO2″|^»













![mathsf{2NaAsO_2 + 3SnCl_2 + 14HCl xrightarrow{} 2Asdownarrow + 3H_2[SnCl_6] + 2NaCl + 4H_2O }](https://dic.academic.ru/dic.nsf/ruwiki/bd2ce0b870de4cccdd72d52d6ae0e18d.png)
