Альфинал®
Таб., покр. пленочной оболочкой, 5 мг: 30 шт.
рег. №: Р N002468/01
от 06.05.08
Дата перерегистрации: 02.11.20
Пенестер®
Таб., покр. пленочной оболочкой, 5 мг: 30, 60 или 90 шт.
рег. №: ЛС-000133
от 30.03.10
Дата перерегистрации: 13.07.20
Произведено:
ZENTIVA
(Чешская Республика)
Сонирид Дуо
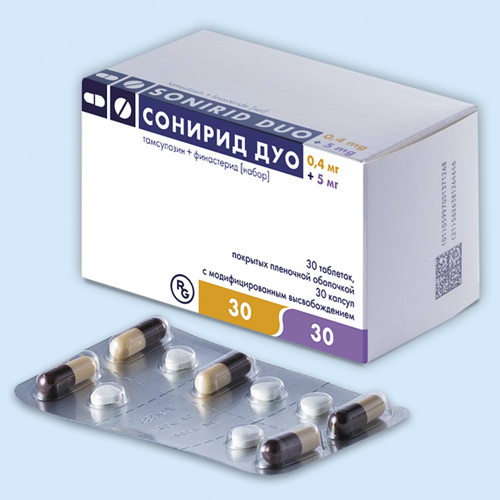
Таблеток и капсул набор / в наборе: капс. с модиф. высвобождением 400 мкг: 30 шт. в пачке; таб., покр. пленочной оболочкой, 5 мг: 30 шт. в пачке
рег. №: ЛП-(000183)-(РГ-RU )
от 01.04.21
Предыдущий рег. №: ЛП-001488
Финаст®
Таб., покр. пленочной оболочкой, 5 мг: 28 или 30 шт.
рег. №: ЛП-(000835)-(РГ-RU )
от 25.05.22
Предыдущий рег. №: П N014580/01
Финастерид-OBL
Таб., покр. пленочной оболочкой, 5 мг: 7, 10, 14, 15, 20, 21, 28, 30, 40, 42, 45, 56, 60, 80, 90 или 120 шт.
рег. №: ЛП-(000502)-(РГ-RU )
от 13.01.22
Предыдущий рег. №: ЛС-002040
Финастерид-Тева
Таб., покр. пленочной оболочкой, 5 мг: 20, 28, 30, 60, 90 или 100 шт.
рег. №: ЛП-(000933)-(РГ-RU )
от 24.06.22
Предыдущий рег. №: ЛП-001187
контакты:
ТЕВА
(Израиль)
Алфузозин
Таб. пролонгир. действия 10 мг: 10, 14, 28, 30, 50, 56 или 60 шт.
рег. №: ЛП-000665
от 28.09.11
Дата перерегистрации: 29.09.16
Алфузозин
Таб. пролонгир. действия 5 мг: 10, 14, 28, 30, 50, 56 или 60 шт.
рег. №: ЛП-000665
от 28.09.11
Дата перерегистрации: 29.09.16
Алфупрост® МР
Таб. пролонгированного действия 10 мг: 10, 20, 30 или 60 шт.
рег. №: ЛП-001176
от 11.11.11
Дата перерегистрации: 27.04.17
Альфузозин
Таб. с контролир. высвоб., покр. оболочкой, 5 мг: 60 шт.
рег. №: ЛСР-000174/08
от 23.01.08
Афала®
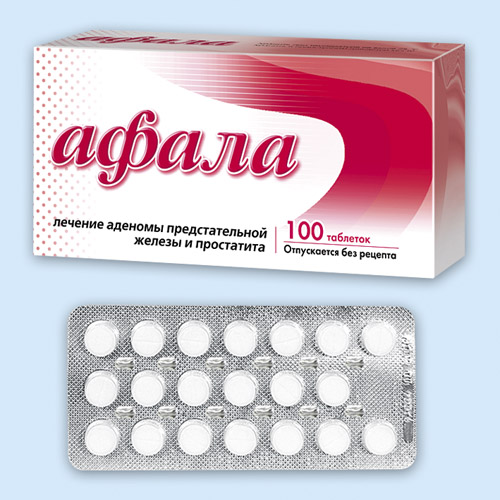
Таб. д/рассасывания: 100 шт.
рег. №: ЛП-(000020)-(РГ-RU )
от 12.12.19
Дата перерегистрации: 23.06.22
Афалаза®

Таб. д/рассасывания: 100 шт.
рег. №: ЛП-(000021)-(РГ-RU )
от 12.12.19
Дата перерегистрации: 26.04.22
Биопрост®
Супп. ректальные 500 мг+100 мг: 10 шт.
рег. №: Р N003058/01
от 27.10.08
Дата перерегистрации: 19.09.19
Гиперпрост
Капс. пролонгир. действия 400 мкг: 10 или 30 шт.
рег. №: ЛС-001345
от 20.06.11
Упаковка и выпускающий контроль качества:
МАКИЗ-ФАРМА
(Россия)
или
СКОПИНФАРМ
(Россия)
контакты:
ШТАДА
(Россия)
Глансин
Капс. с модифицированным высвобождением 0.2 мг: 10, 30, 60 или 90 шт.
рег. №: ЛП-003820
от 05.09.16
Дата перерегистрации: 06.09.21
Глансин
Капс. с модифицированным высвобождением 0.4 мг: 10, 30, 60 или 90 шт.
рег. №: ЛП-003820
от 05.09.16
Дата перерегистрации: 06.09.21
Дальфаз® Ретард
Таб. пролонгир. действия, покр. оболочкой, 5 мг: 56 шт.
рег. №: П N013809/01
от 19.11.07
Дальфаз® СР
Таб. пролонгир. действия 10 мг: 10 или 30 шт.
рег. №: П N013178/01
от 17.04.07
Дуодарт
Капс. с модифицированным высвобождением 500 мкг+400 мкг: 30 или 90 шт.
рег. №: ЛП-(000392)-(РГ-RU )
от 15.10.21
Предыдущий рег. №: ЛП-002650
Корнам®
Таб. 2 мг: 20 или 30 шт.
рег. №: П N015973/01
от 03.11.09
Корнам®
Таб. 5 мг: 20 или 30 шт.
рег. №: П N015973/01
от 03.11.09
Омник Окас
Таб. с контролир. высвобождением, покр. оболочкой, 400 мкг: 10 или 30 шт.
рег. №: ЛС-000849
от 24.02.11
Дата перерегистрации: 13.05.15
Или упаковка и выпускающий контроль качества:
ЗиО-ЗДОРОВЬЕ
(Россия)
Омник®
Капс. с модифицированным высвобождением 400 мкг: 10, 30 или 100 шт.
рег. №: П N013915/01
от 21.05.08
Дата перерегистрации: 11.10.16
Или упаковка и выпускающий контроль качества:
ЗиО-ЗДОРОВЬЕ
(Россия)
Омсулозин
Капс. пролонгир. действия 400 мкг: 10 шт.
рег. №: ЛСР-001955/07
от 07.08.07
Пальмапрост
Капс. 320 мг: 30, 60 или 90 шт.
рег. №: ЛП-007529
от 21.10.21
Пермиксон
Капс. 160 мг: 30 шт.
рег. №: ЛП-(000340)-(РГ-RU )
от 30.08.21
Предыдущий рег. №: П N012687/02
Простагерб Н
Таб., покр. оболочкой, 230 мг: 40 или 100 шт.
рег. №: П N010251
от 19.10.11
Простагут Форте
Капс. 160 мг+120 мг: 60 или 120 шт.
рег. №: П N014145/01
от 31.07.08
Простамол® УНО
Капс. 320 мг: 15, 30 или 60 шт.
рег. №: П N012255/01
от 29.12.10
Простаплант
Капс. 320 мг: 30, 60 или 120 шт.
рег. №: П N014621/01
от 18.09.08
Простатофф
Капс. 160 мг: 30, 40, 45, 60 или 90 шт.
рег. №: ЛП-004420
от 16.08.17
Простатофф
Капс. 320 мг: 30, 40, 45, 60 или 90 шт.
рег. №: ЛП-004420
от 16.08.17
Профлосин®
Капс. кишечнорастворимые пролонгир. действ. 400 мкг: 10 или 30 или 100 шт.
рег. №: ЛП-000832
от 10.10.11
Профлосин®
Капс. кишечнорастворимые пролонгир. действ. 400 мкг: 10, 30 или 100 шт.
рег. №: ЛП-000832
от 10.10.11
Фасовка, упаковка и выпускающий контроль качества:
MENARINI-VON HEYDEN
(Германия)
Сетегис®
Таб. 1 мг: 30 шт.
рег. №: П N012256/01
от 23.08.10
Дата перерегистрации: 16.02.18
Сетегис®
Таб. 10 мг: 30 шт.
рег. №: П N012256/01
от 23.08.10
Дата перерегистрации: 16.02.18
Сетегис®
Таб. 2 мг: 30 шт.
рег. №: П N012256/01
от 23.08.10
Дата перерегистрации: 16.02.18
Сетегис®
Таб. 5 мг: 30 шт.
рег. №: П N012256/01
от 23.08.10
Дата перерегистрации: 16.02.18
Сонизин®
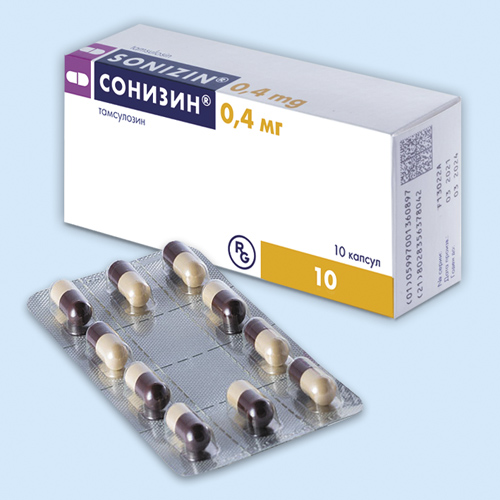
Капс. с модифицированным высвобождением 0.4 мг: 10 или 30 шт.
рег. №: ЛП-(000753)-(РГ-RU )
от 04.05.22
Предыдущий рег. №: ЛСР-002155/07
Тадимакс®
Таб., покр. пленочной оболочкой: 42 или 63 шт.
рег. №: ЛП-002170
от 02.08.13
Дата перерегистрации: 29.08.18
Тамзелин®
Капс. с пролонгир. высвобождением 0.4 мг: 10 или 30 шт.
рег. №: ЛП-000620
от 21.09.11
Дата перерегистрации: 18.05.20
Тамсувел
Капс. с пролонгир. высвобождением 0.4 мг: 10, 20, 30, 40, 50, 60, 70, 80, 90 или 100 шт.
рег. №: ЛП-007658
от 02.12.21
Произведено:
ВЕЛФАРМ
(Россия)
Тамсулозин
Капс. кишечнорастворимые с пролонгир. высвобождением 400 мкг: 10, 20, 30, 50, 60, 90 или 100 шт.
рег. №: ЛП-003636
от 17.05.16
Тамсулозин
Капс. кишечнорастворимые с пролонгированным высвобождением 0.4 мг: 10, 30 или 100 шт.
рег. №: ЛП-(000663)-(РГ-RU )
от 05.04.22
Фасовка, упаковка и выпускающий контроль качества:
ФармФирма Сотекс
(Россия)
Тамсулозин
Капс. с пролонгир. высвобождением 0.4 мг: 10, 20, 30, 40, 50, 60, 70, 80, 90 или 100 шт.
рег. №: ЛП-008006
от 01.04.22
Тамсулозин
Капс. с пролонгир. высвобождением 0.4 мг: 7, 10, 14, 20, 21, 30, 35, 42, 50, 60, 63, 70, 90 или 100 шт.
рег. №: ЛП-007900
от 18.02.22
Производитель:
ОЗОН
(Россия)
Тамсулозин
Капсулы кишечнорастворим. с пролонг. высвобождением 0.4 мг
рег. №: ЛП-008088
от 25.04.22
Тамсулозин Канон
Капс. кишечнорастворимые с пролонгир. высвобождением 0.4 мг: 10, 30, 60, 70 или 90 шт.
рег. №: ЛП-003936
от 07.11.16
Дата перерегистрации: 10.04.20
Тамсулозин Канон
Таб. с пролонгир. высвобождением, покр. пленочной оболочкой 0.4 мг: 10 или 30 шт.
рег. №: ЛП-004253
от 19.04.17
Тамсулозин Реневал
Капс. кишечнораств. с пролонгир. высвобождением 0.4 мг: 30 или 90 шт.
рег. №: ЛП-007703
от 21.12.21
Тамсулозин ретард
Таб. с пролонгир. высвобождением, покр. пленочной оболочкой, 400 мкг: 10, 14, 15, 20, 28, 30, 40, 42, 45 или 60 шт.
рег. №: ЛП-000283
от 17.02.11
Дата перерегистрации: 28.08.18
Тамсулозин-OBL
Капс. с модифицированным высвобождением 0.4 мг: 10, 14, 15, 20, 28, 30, 40, 42, 45 или 60 шт.
рег. №: ЛП-001422
от 12.01.12
Дата перерегистрации: 24.03.22
Тамсулозин-Бинергия
Капс. кишечнорастворимые с пролонгир. высвобождением 0.4 мг: 10, 30, 60, 90 или 100 шт.
рег. №: ЛП-005765
от 03.09.19
Тамсулозин-Вертекс
Капс. с пролонгир. высвобождением 400 мкг: 10, 20, 30, 60 или 90 шт.
рег. №: ЛП-002820
от 14.01.15
Тамсулозин-Вертекс
Таб. с пролонгир. высвобождением, покр. пленочной оболочкой, 0.4 мг: 30, 60 или 90 шт.
рег. №: ЛП-005271
от 20.12.18
Тамсулозин-Розлекс
Капс. с модифицированным высвобождением 0.4 мг: 10 30, 60 или 90 шт.
рег. №: ЛП-005444
от 04.04.19
Дата перерегистрации: 03.06.19
Тамсулозин-Эдвансд
Капс. кишечнорастворимые с пролонгир. высвобождением 0.4 мг: 10, 30, 60 или 90 шт.
рег. №: ЛП-006922
от 13.04.21
Тамсулон®
Капс. пролонгированного действия 400 мкг: 10, 30 или 90 шт.
рег. №: ЛС-000859
от 15.06.11
Дата перерегистрации: 27.03.17
Произведено и упаковано:
ФАРМПРОЕКТ
(Россия)
Выпускающий контроль качества:
ФАРМ-СИНТЕЗ
(Россия)
Таниз®-К
Капс. с пролонгир. высвобождением 400 мкг: 10, 20, 30, 60, 90 или 200 шт.
рег. №: ЛСР-007250/08
от 10.09.08
Дата перерегистрации: 24.07.20
Фасовка, упаковка и выпускающий контроль качества:
KRKA
(Словения)
Теразозин
Таб. 2 мг: 100, 500 или 1000 шт., 5 кг, 8 кг или 10 кг
рег. №: П N014281/01
от 22.10.08
Теразозин
Таб. 2 мг: 20 или 1000 шт.
рег. №: ЛСР-003526/09
от 13.05.09
Теразозин
Таб. 5 мг: 100, 500 или 1000 шт., 5 кг, 8 кг или 10 кг
рег. №: П N014281/01
от 22.10.08
Теразозин
Таб. 5 мг: 20 или 1000 шт.
рег. №: ЛСР-003526/09
от 13.05.09
Тыквеол®
Капс. 450 мг: 10, 20, 30, 50, 84, 90 или 180 шт.
рег. №: Р N002321/01
от 25.06.08
Масло д/приема внутрь: фл.100 мл
рег. №: Р N002321/03
от 01.07.08
Супп. ректальные 500 мг: 10 шт.
рег. №: Р N002321/02
от 25.06.08
Дата перерегистрации: 28.06.19
Урорек

Капс. 4 мг: 5, 10, 15, 20, 25, 30, 40, 45, 50, 60, 75, 90, 100, 135 или 150 шт.
рег. №: ЛСР-005971/10
от 25.06.10
Дата перерегистрации: 04.02.22
Капс. 8 мг: 5, 10, 15, 20, 25, 30, 40, 45, 50, 60, 75, 90, 100, 135 или 150 шт.
рег. №: ЛСР-005971/10
от 25.06.10
Дата перерегистрации: 04.02.22
Фокусин®
Капс. с модиф. высвобождением 400 мкг: 30, 60, 90 или 100 шт.
рег. №: ЛС-001633
от 01.04.11
Дата перерегистрации: 12.02.20
Капс. с модиф. высвобождением 400 мкг: 30, 90 или 100 шт.
рег. №: ЛС-001633
от 01.04.11
Дата перерегистрации: 12.02.20
Цернилтон®
Таб., покр. пленочной оболочкой, 311.5 мг: 100, 200 или 5000 шт.
рег. №: ЛП-001301
от 29.11.11
Цернилтон®
Таб.: 100 или 200 шт.
рег. №: П N014227/01
от 06.06.08
Дата перерегистрации: 07.04.17
Цернилтон® Форте
Капс.: 50 шт.
рег. №: ЛП-000453
от 01.03.11
Дата перерегистрации: 07.04.17
МНН: дутастерид — аналоги
Важно: аналоги содержат действующее вещество дутастерид, но не являются эквивалентной заменой друг другу
Уточнить
Дутастерид селективно и необратимо ингибирует I и II изоформу 5α-редуктазы. Этот фермент превращает тестостерон в дигидротестостерон — , первичный гормональный медиатор, участвующий в гиперплазии предстательной железы. Препарат применяется как в виде монотерапии, так и в комбинации с тамсулозином для усиления терапевтического ответа при ДГПЖ.
Дуодарт
Дуодарт (дутастерид + тамсулозин, капсулы с модифицированным высвобождением). Оригинальный комбинированный препарат для лечения и профилактики доброкачественной гиперплазии предстательной железы. Производитель: «ГлаксоСмитКляйн» (Великобритания).
Дутастерид Канон
Дутастерид. 5-альфа редуктазы двойной ингибитор. ЗАО «Канонфарма продакшн» (Россия)
Аводарт
Аводарт (оригинальный дутастерид, капсулы). Препарат для лечения и профилактики доброкачественной гиперплазии предстательной железы. Производитель: «ГлаксоСмитКляйн» (Великобритания).
Гардиум
Дутастерид. 5-альфа редуктазы двойной ингибитор. Тева Фармасьютикал Воркс Прайвэт Лимитед Компани (Венгрия)
Дутастерон
Дутастерон (дутастерид, капсулы). Препарат для лечения и профилактики доброкачественной гиперплазии предстательной железы. Производитель: «Фарм-Синтез» (Россия).
Рак
предстательной железы (РПЖ)
В
4-летнем исследовании участвовали более 8000 мужчин в возрасте от 50 до 75 лет,
характеризующихся отрицательным результатом биопсии на наличие РПЖ и
концентрацией ПСА между 2,5 нг/мл и 10,0 нг/мл (исследование REDUCE)
при первичном обследовании, при этом у 1517 из них был диагностирован РПЖ.
Зарегистрировано
больше случаев РПЖ с оценкой 8–10 баллов по шкале Глисона в группе дутастерида
(n = 29; 0,9%) по сравнению с группой
плацебо (n = 19; 0,6%). Не
отмечалось увеличения количества случаев РПЖ с оценкой 5–6 и 7–10 баллов по
шкале Глисона. Причинно-следственная связь между приемом дутастерида и
развитием РПЖ высокой степени градации не установлена. Клиническое значение
количественного дисбаланса неизвестно. Мужчины, принимающие дутастерид, должны
регулярно проходить обследования в отношении оценки риска развития РПЖ, включая
определение концентрации ПСА.
В
дополнительном 2-летнем исследовании, направленном на последующее наблюдение
пациентов из исследования REDUCE
по химиопрофилактике, новые случаи РПЖ диагностировались редко (дутастерид
(n = 14, 1,22%) и плацебо (n = 7, 0,7%)). новые случаи РПЖ
с оценкой 8–10 баллов по шкале Глисона отсутствовали.
Долгосрочные
наблюдения (до 18 лет) в исследовании по химиопрофилактике с помощью другого
ингибитора 5α‑редуктазы (финастерид) не выявили статистически
значимое различие в применении финастерида и плацебо по показателям общей
выживаемости (ОР 1,02, 95% ДИ 0,97–1,08) или выживаемости после подтверждения
диагноза РПЖ (ОР 1,01, 95% ДИ 0,85–1,20).
Простат-специфический
антиген (ПСА)
Определение
концентрации ПСА является важным компонентом скрининга, направленного на
выявление РПЖ. После 6-месячной терапии дутастеридом средняя концентрация ПСА в
сыворотке крови снижается примерно на 50%.
Для
пациентов, принимающих дутастерид, должна быть установлена новая базовая
концентрация ПСА после 6 месяцев терапии. После этого рекомендуется регулярное
мониторирование концентрации ПСА. Любое подтвержденное повышение концентрации
ПСА относительно наименьшего его значения при лечении дутастеридом может
свидетельствовать о развитии РПЖ или о несоблюдении режима терапии препаратом и
должно подвергаться тщательной оценке, даже если эти концентрации ПСА остаются
в пределах нормальных значений для мужчин, не принимающих ингибиторы 5α‑редуктазы.
При
интерпретации значений концентрации ПСА у пациентов, принимающих дутастерид,
необходимо использовать для сравнения предыдущие результаты оценки концентрации
ПСА.
Применение
дутастерида не влияет на диагностическую ценность определения концентрации ПСА
как маркера РПЖ после того, как установлена новая базовая концентрация ПСА.
Концентрация
общего ПСА в сыворотке крови возвращается к исходному значению в течение 6
месяцев после отмены дутастерида.
Отношение
концентрации свободного ПСА к общему остается постоянным даже на фоне терапии
дутастеридом. Если для выявления РПЖ у мужчин, получающих дутастерид,
дополнительно используется определение процентного содержания свободной фракции
ПСА не требуется проводить коррекцию этого показателя.
У
пациентов необходимо проводить пальцевое ректальное исследование и использовать
другие методы диагностики РПЖ до начала лечения дутастеридом, а также регулярно
повторять обследование пациента в процессе лечения.
Побочные
явления со стороны сердечно-сосудистой системы
В
двух 4-летних клинических исследованиях частота развития сердечной
недостаточности (обобщенный термин для наблюдавшихся событий, представленных в
основном сердечной недостаточностью и застойной сердечной недостаточностью)
была выше у пациентов, получавших комбинацию дутастерида и си-адреноблокатора,
главным образом тамсулозина, чем у пациентов, не получавших комбинированного
лечения. В этих двух клинических исследованиях частота развития сердечной
недостаточности оставалась низкой ( ДИ 0,71, 1,57), острого инфаркта миокарда
(ОР 1,00, 95% ДИ 0,77, 1,30) или инсульта (ОР 1,20, 95% ДИ 0,88, 1,64).
Рак
грудной железы
При
проведении клинических исследований и в пострегистрационном периоде
зарегистрированы редкие сообщения о развитии рака грудной железы у мужчин,
принимающих дутастерид. Тем не менее, данные эпидемиологических исследований не
свидетельствуют о повышении риска развития рака грудной железы у мужчин при
применении ингибиторов 5α‑редуктазы. Специалисты должны
проинструктировать пациентов о необходимости немедленно сообщать о любых
изменениях со стороны грудных желез, таких как уплотнения в железе или
выделения из соска.
Утечка
содержимого капсул
Дутастерид
всасывается через кожу, поэтому женщины и дети должны избегать контакта с капсулами,
у которых наблюдается утечка содержимого. В случае контакта с такими капсулами
затронутую область следует немедленно промыть водой с мылом.
Нарушения
функции печени
Влияние
нарушений функции печени на фармакокинетику дутастерида не исследовалось.
Поскольку дутастерид интенсивно
метаболизируется и его период полувыведения составляет от 3 до 5 недель,
следует с осторожностью назначать дутастерид пациентам с нарушением функции
печени.
Влияние на способность
управлять транспортными средствами и механизмами
Прием
дутастерида не влияет на управление транспортными средствами и работу с
механизмами.
Dutasteridum (род. Dutasteridi)
(4aR,4bS,6aS,7S,9aS,9bS,11aR)-N-[2,5-Бис(трифторметил)фенил]-2,4a,4b,5,6,6a,7,8,9,9a,9b,10,11,11a-тетрадекагидро-4a,6a-диметил-2-оксо-1H-инден[5,4-f]хинолин-7-карбоксамид
Дутастерид представляет собой порошок от белого до бледно-желтого цвета с температурой плавления от 242 до 250 °C. Он растворим в этаноле (44 мг/мл), метаноле (64 мг/мл) и ПЭГ 400 (3 мг/мл), но не растворяется в воде. Молекулярная масса 528,5 Да.
Синтетическое 4-азастероидное соединение, являющееся селективным ингибитором изоформ как 1-го, так и 2-го типов стероидной 5-альфа-редуктазы, внутриклеточного фермента, превращающего тестостерон в дигидротестостерон (ДГТ).
Механизм действия
Дутастерид ингибирует превращение тестостерона в ДГТ. ДГТ — это андроген, который в основном отвечает за начальное развитие и последующее увеличение предстательной железы. Тестостерон превращается в ДГТ с помощью фермента 5-альфа-редуктазы, который существует в виде изоформ типа 1 и типа 2. Изофермент типа 2 в основном активен в репродуктивных тканях, в то время как изофермент типа 1, кроме того, отвечает за преобразование тестостерона в коже и печени.
Дутастерид является конкурентным и специфическим ингибитором изоферментов 5-альфа-редуктазы как 1-го, так и 2-го типов, с которыми он образует стабильный ферментный комплекс. Диссоциация этого комплекса была оценена в условиях in vitro и in vivo и происходит очень медленно. Дутастерид не связывается с андрогенными рецепторами человека.
Фармакодинамика
Влияние на 5-альфа-дигидротестостерон и тестостерон
Максимальный эффект дутастерида на снижение уровня ДГТ зависит от дозы и наблюдается в течение 1–2 нед. Через 1 и 2 нед ежедневного приема 0,5 мг дутастерида медиана концентрацияи ДГТ в сыворотке крови снижалась на 85 и 90% соответственно. У пациентов с ДГПЖ, получавших дутастерид в дозе 0,5 мг/сут в течение 4 лет, медиана снижения сывороточного уровня ДГТ составило 94% через 1 год, 93% через 2 года и 95% как через 3, так и через 4 года. Среднее повышение уровня тестостерона в сыворотке крови составило 19% через 1 и 2 года, 26% через 3 года и 22% через 4 года, но средние и медианные значения оставались в пределах физиологического диапазона. У пациентов с ДГПЖ, получавших 5 мг/сут дутастерида или плацебо в течение 12 нед до трансуретральной резекции простаты, средняя концентрация ДГТ в ткани предстательной железы была значительно ниже в группе получавших дутастерид по сравнению с плацебо (784 и 5793 пг/г соответственно, p<0,001). Средняя концентрация тестостерона в ткани предстательной железы была значительно выше в группе получавших дутастерид по сравнению с плацебо (2073 и 93 пг/г соответственно, p<0,001).
У взрослых мужчин с генетически унаследованной недостаточностью 5-альфа-редуктазы 2-го типа также наблюдается снижение уровня ДГТ. Эти мужчины с дефицитом 5-альфа-редуктазы на протяжении всей жизни имеют небольшую предстательную железу и не заболевают ДГПЖ. За исключением связанных с этой недостаточностью урогенитальных дефектов, присутствующих при рождении, у этих людей не наблюдалось никаких других клинических отклонений, связанных с дефицитом 5-альфа-редуктазы.
Влияние на другие гормоны
У здоровых добровольцев 52 нед лечения дутастеридом в дозе 0,5 мг/сут (n=26) не привели к клинически значимым изменениям по сравнению с плацебо (n=23) в отношении ГСПГ, эстрадиола, ЛГ, ФСГ, тироксина (свободный Т4) и дегидроэпиандростерона. Статистически значимое, скорректированное по исходному уровню среднее увеличение по сравнению с плацебо наблюдалось для общего тестостерона через 8 нед (97,1 нг/дл, p<0,003) и ТТГ через 52 нед (0,4 мкМЕ/мл, p<0,05). Медиана процентных изменений относительно исходного уровня в группе дутастерида составила 17,9% для тестостерона через 8 нед и 12,4% для ТТГ через 52 нед. После прекращения приема дутастерида в течение 24 нед средние уровни тестостерона и ТТГ вернулись к исходному уровню в группе субъектов, данные которой были доступны во время визита. У пациентов с ДГПЖ, получавших дутастерид в большом рандомизированном двойном слепом плацебо-контролируемом исследовании, средний процент увеличения уровня ЛГ составлял 12% через 6 мес и 19% как через 12, так и через 24 мес.
Прочие эффекты
Липидный профиль в плазме крови и МПКТ оценивали после 52 нед приема дутастерида в дозе 0,5 мг 1 раз в день у здоровых добровольцев. По данным двухэнергетической рентгеновской абсорбциометрии, изменений в МПКТ по сравнению с плацебо или исходным уровнем не наблюдалось. Кроме того, дутастерид не влиял на липидный профиль плазмы (т.е. общий Хс, ЛПНП, ЛПВП, триглицериды). Клинически значимых изменений в ответах гормонов надпочечников на стимуляцию АКТГ не наблюдалось в субпопуляции (n=13) в течение 1-летнего исследования с участием здоровых добровольцев.
Фармакокинетика
Абсорбция
После перорального приема дутастерида в однократной дозе 0,5 мг Tmax в сыворотке крови составляла 2–3 ч. Абсолютная биодоступность у 5 здоровых добровольцев — приблизительно 60% (в диапазоне от 40 до 94%). При приеме во время еды Cmax в сыворотке крови снижалась на 10–15%. Это уменьшение не имеет клинического значения.
Распределение
Фармакокинетические данные после однократных и повторных пероральных доз показывают, что дутастерид имеет большой Vd (от 300 до 500 л). Дутастерид сильно связывается с альбумином плазмы (99%) и альфа1-кислым гликопротеином (96,6%).
В исследовании с участием здоровых добровольцев (n=26), получавших дутастерид в дозе 0,5 мг/сут в течение 12 мес, концентрация дутастерида в сперме составляла в среднем 3,4 нг/мл (диапазон от 0,4 до 14 нг/мл) через 12 мес и, как и в сыворотке крови, достигала равновесных значений через 6 мес. В среднем через 12 мес в сперму распределяется 11,5% от сывороточной концентрации дутастерида.
Метаболизм и выведение
Дутастерид экстенсивно метаболизируется в организме человека. Исследования in vitro показали, что дутастерид метаболизируется с участием изоферментов CYP3A4 и CYP3A5. Оба этих изофермента катализировали образование 4′-гидроксидутастерид, 6-гидроксидутастерида и 6,4′-дигидроксидутастерида. Кроме того, с участием CYP3A4 образуется 15-гидроксидутастеридный метаболит. Дутастерид не метаболизируется изоферментами CYP1A2, CYP2A6, CYP2B6, CYP2C8, CYP2C9, CYP2C19, CYP2D6 и CYP2E1. В сыворотке крови человека после достижения равновесного состояния, по результатам масс-спектрометрического анализа, обнаруживаются неизмененный дутастерид, 3 основных метаболита (4′-гидроксидутастерид, 1,2-дигидродутастерид и 6-гидроксидутастерид) и 2 второстепенных метаболита (6,4′-дигидроксидутастерид и 15-гидроксидутастерид). Абсолютная стереохимия гидроксильных групп в положениях 6 и 15 неизвестна. In vitro метаболиты 4′-гидроксидутастерид и 1,2-дигидродутастерид гораздо менее эффективны, чем дутастерид, в отношении обеих изоформ 5-альфа-редуктазы человека. Активность 6β-гидроксидутастерида сопоставима с активностью дутастерида.
Дутастерид и его метаболиты экскретируются преимущественно с калом, в т.ч. приблизительно 5% в виде неизмененного дутастерида (от ~1 до ~15%) и 40% в виде его метаболитов (от ~2 до ~90%). В моче обнаруживались только следовые количества неизмененного дутастерида (<1%).
Конечный T1/2 дутастерида составляет примерно 5 нед в равновесном состоянии. Средняя Css дутастерида в сыворотке крови составила 40 нг/мл после приема в дозе 0,5 мг/сут в течение 1 года. После ежедневного приема концентрация дутастерида в сыворотке крови достигает 65% от Css через 1 мес и примерно 90% через 3 мес. Из-за длительного T1/2 дутастерида его сывороточные концентрации остаются определяемыми (более 0,1 нг/мл) в течение 4–6 мес после прекращения лечения.
Особые группы пациентов
Дети. Фармакокинетика дутастерида не изучалась у субъектов моложе 18 лет.
Пожилой возраст. У пожилых людей коррекция дозы не требуется. Фармакокинетика и фармакодинамика дутастерида были оценены у 36 здоровых мужчин от 24 до 87 лет после введения однократной дозы дутастерида 5 мг. В этом исследовании T1/2 дутастерида увеличивался с возрастом (примерно 170 ч у мужчин от 20 до 49 лет, примерно 260 ч у мужчин от 50 до 69 лет и примерно 300 ч у мужчин старше 70 лет). Из 2167 мужчин, получавших дутастерид в трех базовых исследованиях, 60% были в возрасте 65 лет и старше и 15% — в возрасте 75 лет и старше. В целом не наблюдалось различий в безопасности или эффективности между пожилыми и более молодыми пациентами.
Пол. Дутастерид противопоказан при беременности и не показан для использования женщинами (см. «Противопоказания»). Фармакокинетика дутастерида у женщин не изучалась.
Раса. Влияние расы на фармакокинетику дутастерида не изучалось.
Почечная недостаточность. Влияние почечной недостаточности на фармакокинетику дутастерида не изучалось. Однако менее 0,1% дозы дутастерида 0,5 мг в равновесном состоянии выводится с мочой человека, поэтому для пациентов с почечной недостаточностью корректировки дозировки не требуется.
Печеночная недостаточность. Влияние печеночной недостаточности на фармакокинетику дутастерида не изучалось. Поскольку дутастерид интенсивно метаболизируется, его экспозиция может быть выше у пациентов с печеночной недостаточностью.
Исследования лекарственных взаимодействий
Ингибиторы CYP450
Не проводились клинические исследования лекарственного взаимодействия для оценки влияния ингибиторов изофермента CYP3A на фармакокинетику дутастерида. Однако, основываясь на данных in vitro, концентрация дутастерида в крови может увеличиваться в присутствии ингибиторов CYP3A4/5, таких как ритонавир, кетоконазол, верапамил, дилтиазем, циметидин, тролеандомицин и ципрофлоксацин.
Дутастерид не подавляет метаболизм in vitro модельных субстратов основных изоферментов CYP450 человека (CYP1A2, CYP2C9, CYP2C19, CYP2D6 и CYP3A4) в концентрации 1000 нг/мл, что в 25 раз выше Css в сыворотке крови человека.
Альфа-адреноблокаторы
В перекрестном исследовании с одной последовательностью с участием здоровых добровольцев введение тамсулозина или теразозина в комбинации с дутастеридом не влияло на стационарную фармакокинетику любого альфа-адреноблокатора. Хотя влияние введения тамсулозина или теразозина на фармакокинетические параметры дутастерида не оценивалось, процентное изменение концентрации ДГТ было аналогичным при применении дутастерида в виде монотерапии и при комбинированной терапии.
БКК
В популяционном фармакокинетическом анализе было отмечено снижение клиренса дутастерида при одновременном назначении с ингибиторами CYP3A4 верапамилом (−37%, n=6) и дилтиаземом (−44%, n=5). Напротив, уменьшение клиренса не наблюдалось при одновременном применении амлодипина, другого БКК, который не является ингибитором CYP3A4, с дутастеридом (+7%, n=4).
Уменьшение клиренса и последующее увеличение воздействия дутастерида в присутствии верапамила и дилтиазема не считается клинически значимым. Коррекция дозы не рекомендуется.
Колестирамин
Однократное применение 5 мг дутастерида с последующим приемом 12 г колестирамина через 1 ч не повлияло на относительную биодоступность дутастерида у 12 здоровых добровольцев.
Дигоксин
В исследовании с участием 20 здоровых добровольцев дутастерид при одновременном приеме в дозе 0,5 мг/сут в течение 3 нед не изменял фармакокинетику дигоксина в равновесном состоянии.
Варфарин
В исследовании с участием 23 здоровых добровольцев трехнедельный курс лечения дутастеридом в дозе 0,5 мг/сут не повлиял на фармакокинетику в равновесном состоянии изомеров S- или R-варфарина и не изменял влияние варфарина на ПВ при одновременном применении.
Другая сопутствующая терапия
Хотя исследования специфического взаимодействия с другими ЛС не проводились, примерно 90% субъектов в 3 рандомизированных двойных слепых плацебо-контролируемых исследованиях безопасности и эффективности, получавших дутастерид, одновременно принимали другие ЛС. Не выявлено клинически значимого неблагоприятного взаимодействия комбинации дутастерида и сопутствующей терапии при одновременном применении гиполипидемических ЛС, ингибиторов АПФ, бета-адреноблокаторов, БКК, ГКС, диуретиков, НПВС, ингибиторов ФДЭ-5 и хинолоновых антибактериальных средств.
Канцерогенность, мутагенность, влияние на фертильность
Канцерогенность
Было проведено двухлетнее исследование канцерогенности на мышах линии B6C3F1 при дозах 3, 35, 250 и 500 мг/кг/сут для самцов и 3, 35 и 250 мг/кг/сут для самок, повышенная частота развития доброкачественных гепатоцеллюлярных аденом была отмечена при введении 250 мг/кг/сут (кратно 290 МРДЧ, составляющей 0,5 мг/сут) только у самок мышей. Два из трех основных метаболитов человека были обнаружены у мышей. Воздействие этих метаболитов у мышей либо ниже, чем у людей, либо неизвестно.
В двухлетнем исследовании канцерогенности на крысах линии Han Wistar при дозах 1,5; 7,5 и 53 мг/кг/сут у самцов и 0,8; 6,3 и 15 мг/кг/сут у самок наблюдалась повышенная частота аденомы из лейдиговских клеток в яичках при дозе, в 135 раз превышающей МРДЧ (53 мг/кг/сут и больше). Повышенная частота гиперплазии клеток Лейдига отмечалась при дозах, в 52 раза превышающих МРДЧ (дозы у самцов крыс 7,5 мг/кг/сут и выше). Положительная корреляция между пролиферативными изменениями в клетках Лейдига и повышением уровня циркулирующего ЛГ отмечалась при действии ингибиторов 5-альфа-редуктазы и согласуется с влиянием этого ингибирования на гипоталамо-гипофизарно-яичниковую ось. В туморогеных дозах уровень ЛГ у крыс увеличивался на 167%. В этом исследовании основные метаболиты человека были проверены на канцерогенность при экспозиции, примерно в 1–3 раза превышающей ее ожидаемый уровень в клинике.
Мутагенность
Дутастерид был протестирован на генотоксичность в бактериальном тесте Эймса, в анализе хромосомных аберраций в клетках яичников китайского хомячка и микроядерном тесте на клетках крыс. Не обнаружено генотоксического потенциала у исходного соединения. Два основных метаболита у человека также показали отрицательные результаты в тесте Эймса, либо в сокращенном тесте Эймса.
Влияние на фертильность
Введение дутастерида половозрелым самцам крыс в дозе, составляющей 0,1 МРДЧ (дозы у животных, составляющие 0,05 мг/кг/сут или более в течение до 31 нед) из расчета средней концентрации в сыворотке крови, приводило к зависимому от дозы и времени снижению фертильности при всех дозах; снижение количества сперматозоидов в хвостовой части придатка яичка (абсолютное), но не концентрации сперматозоидов (при дозах 50 и 500 мг/кг/сут), уменьшению веса придатка яичка, простаты и семенных пузырьков и микроскопическим изменениям (цитоплазматическая вакуолизация канальцевого эпителия в придатках яичка и/или снижение цитоплазматического содержания эпителия, что соответствует снижению секреторной активности в предстательной железе и семенных пузырьках) в репродуктивных органах при всех дозах при отсутствии токсичности для самцов. Эти эффекты устранялись к 6-й неделе периода реабилитации при всех дозах, и количество сперматозоидов было нормальным в конце 14-недельного периода реабилитации. Микроскопические изменения больше не обнаруживались на 14-й нед восстановления при дозах, состаляющих 0,1 МРДЧ, и частично восстановились в других группах введения. Низкий уровень дутастерида (от 0,6 до 17 нг/мл) был обнаружен в сыворотке самок крыс без введения препарата, скрещенных с леченными самцами (от 10 до 500 мг/кг/сут в течение 29–30 нед), что в 16–110 раз превышало МРДЧ из расчета средней концентрации в сыворотке крови. У потомства самцов самок крыс без введения препарата, скрещенных с леченными самцами, не происходило феминизации, хотя у самок крыс наблюдались определяемые уровни дутастерида в крови.
В исследовании фертильности у самок крыс, получавших дутастерид в период за 4 нед до спаривания и на ранних сроках гестации, пероральное введение дутастерида в дозах 0,05; 2,5; 12,5 и 30 мг/кг/сут приводило к уменьшению размера помета из-за увеличения резорбции и феминизации плодов мужского пола (уменьшение аногенитального расстояния) при дозах, в 2–10 раз превышающих МРДЧ (дозы у животных 2,5 мг/кг/сут или больше) из расчета средней концентрации в сыворотке крови, при наличии материнской токсичности (уменьшение прироста массы тела). Масса тела плода также была снижена при дозах, примерно составляющих 0,02 МРДЧ (доза для крыс 0,05 мг/кг/сут или больше) из расчета средней концентрации в сыворотке крови, при отсутствии материнской токсичности.
Клинические исследования
Монотерапия
В трех 2-летних многоцентровых плацебо-контролируемых двойных слепых исследованиях, каждое из них с 2-летним периодом дополнительного открытого лечения (n=2340), сравнивали применение дутастерида в дозе 0,5 мг/сут (n=2167) или плацебо (n=2158) у мужчин с ДГПЖ. Более 90% исследуемой популяции были представителями европеоидной расы. Возраст субъектов составлял как минимум 50 лет, уровень ПСА в сыворотке крови — ≥1,5 и <10 нг/мл, и ДГПЖ была диагностирована на основании истории болезни и физикального обследования, включая увеличение простаты (≥30 см3) и симптомы ДГПЖ от умеренных до тяжелых при оценке с помощью индекса симптомов американской урологической ассоциации (AUA-SI). Большинство из 4325 субъектов, рандомизированных для получения дутастерида или плацебо, прошли 2 года двойного слепого лечения (70 и 67% соответственно). Большинство из 2340 субъектов в период дополнительного открытого лечения завершили 2 дополнительных года открытого лечения (71%).
Влияние на оценку симптомов
Симптомы оценивали количественно с помощью опросника AUA-SI, который оценивает симптомы мочеиспускания (неполное опорожнение, частота, прерывистость, позывы, слабый поток, напряжение и никтурия) по шкале от 0 до 5 с общим возможным баллом 35, более высокая числовая оценка симптомов соответствует более серьезной тяжести симптомов. Исходный показатель AUA-SI в трех исследованиях составлял примерно 17 единиц в обеих группах лечения.
Пациенты, получавшие дутастерид, показали статистически значимое улучшение симптомов по сравнению с получавшими плацебо к 3-му мес в одном исследовании и к 12-му мес в двух других базовых исследованиях. К 12-му мес среднее снижение по сравнению с исходным уровнем общей оценки по шкале AUA-SI в пуле из трех исследований составило −3,3 единицы для дутастерида и −2 единицы для плацебо со средней разницей между двумя группами лечения −1,3 (диапазон от −1,1 до −1,5 в каждом из трех исследований, p<0,001) и было постоянным во всех трех исследованиях. К 24-му мес среднее снижение по сравнению с исходным уровнем составило −3,8 у получавших дутастерид и −1,7 у получавших плацебо со средней разницей −2,1 (диапазон от −1,9 до −2,2 в каждом из трех исследований, p<0,001). Улучшение симптомов ДГПЖ, наблюдаемое в течение первых 2 лет двойного слепого лечения, сохранялось и в течение дополнительных 2 лет открытого лечения.
Проспективный дизайн этих исследований предусматривал оценку воздействия на симптомы, основанную на исходном размере предстательной железы. У мужчин с объемом предстательной железы ≥40 см3 среднее снижение составило −3,8 единицы для получавших дутастерид и −1,6 единицы для получавших плацебо, при этом средняя разница между двумя группами лечения составила −2,2 к 24-му мес. У мужчин с объемом простаты <40 см3 среднее снижение составило −3,7 единицы для дутастерида и −2,2 единицы для плацебо, при средней разнице между двумя группами лечения −1,5 к 24-му мес.
Влияние на острую задержку мочи и необходимость хирургического вмешательства по поводу аденомы предстательной железы
Эффективность применения дутастерида также оценивали после 2 лет лечения по частоте возникновения острой задержки мочи, требующей катетеризации и связанного с ДГПЖ урологического хирургического вмешательства. По сравнению с плацебо, применение дутастерида было связано со статистически значимо более низкой частотой равития острой задержки мочи (1,8 по сравнению с 4,2%, p<0,001; снижение риска на 57% (95% ДИ: от 38 до 71%) и меньшей частотой хирургических вмешательств (2,2 по сравнению с 4,1%, p<0,001; снижение риска на 48% (95% ДИ: от 26 до 63%).
Влияние на объем предстательной железы
Для включения в исследование требовался объем простаты у пациентов не менее 30 см3, измеренный методом трансректального УЗИ. Средний объем простаты на момент включения в исследование был приблизительно 54 см3.
Статистически значимые различия (дутастерид по сравнению с плацебо) были отмечены при самом раннем измерении объема простаты после лечения в каждом испытании (месяц 1, месяц 3 или месяц 6) и сохранялись до 24 мес. На 12-й мес среднее изменение объема простаты по объединенным данным трех исследований составило −24,7% для дутастерида и −3,4% для плацебо; средняя разница (дутастерид минус плацебо) составила −21,3% (диапазон: от −21 до −21,6% в каждом из 3 исследований, p<0,001). К 24-му месяцу среднее изменение объема простаты по объединенным данным трех исследований составило −26,7% для получавших дутастерид и −2,2% для получавших плацебо со средней разницей −24,5% (диапазон от −24 до −25,1% в каждом из трех исследований, p<0,001). Уменьшение объема простаты, наблюдаемое в течение первых 2 лет двойного слепого лечения, сохранялось и в течение дополнительных 2 лет открытого лечения.
Влияние на максимальную скорость потока мочи
Для включения в исследование требовалась средняя пиковая скорость потока мочи у пациента (Qmax) ≤15 мл/с. Qmax в трех базовых испытаниях составлял приблизительно 10 мл/с на исходном уровне. Различия между двумя группами лечения были статистически значимыми по сравнению с исходным уровнем к 3-му мес во всех трех исследованиях и сохранялись до 12 мес. К 12-му мес среднее увеличение Qmax в объединенных данных трех исследований составило 1,6 мл/с для получавших дутастерид и 0,7 мл/с для получавших плацебо, средняя разница (дутастерид минус плацебо) составляла 0,8 мл/с (диапазон 0,7–1 мл/с в каждом из трех исследований, p<0,001). К 24-му мес среднее увеличение Qmax составило 1,8 мл/с для дутастерида и 0,7 мл/с для плацебо при средней разнице 1,1 мл/с (диапазон от 1 до 1,2 мл/с в каждом из трех исследований, p<0,001). Увеличение Qmax, наблюдаемое в течение первых 2 лет двойного слепого лечения, сохранялось в течение дополнительных 2 лет открытого лечения.
Резюме по результатам клинических исследований
Данные трех крупных, хорошо контролируемых исследований эффективности показывают, что применение дутастерида (0,5 мг 1 раз в день) снижает риск развития острой задержки мочи и хирургического вмешательства, связанного с ДГПЖ, по сравнению с плацебо, улучшает симптомы, связанные с ДГПЖ, уменьшает объем простаты и увеличивает Qmax. Эти данные позволяют предположить, что дутастерид останавливает развитие ДГПЖ у мужчин с увеличенной простатой.
Комбинированная терапия альфа-адреноблокаторами (CombAT)
Эффективность комбинированной терапии (дутастерид в дозе 0,5 мг/сут плюс тамсулозин в дозе 0,4 мг/сут, n=1610) сравнивалась с монотерапией дутастеридом (n=1623) или тамсулозином (n=1611) в 4-летнем многоцентровом рандомизированном двойном слепом исследовании. Критерии включения в исследование были аналогичны таковым в двойных слепых плацебо-контролируемых исследованиях эффективности монотерапии. Популяция, включенная в исследование, на 88% состояла из представителей европеоидной расы. Примерно 52% субъектов ранее получали лечение ингибитором 5-альфа-редуктазы или альфа-адреноблокатором. Из 4844 пациентов, рандомизированных для получения лечения, 69% пациентов в группе комбинированной терапии, 67% в группе, получавшей дутастерид, и 61% в группе получавшей тамсулозин завершили 4 года двойного слепого лечения.
Влияние на оценку симптомов
Симптомы количественно оценивались с использованием первых 7 вопросов Международной шкалы симптомов простаты (IPSS) (идентична AUA-SI). Исходный балл составлял приблизительно 16,4 единицы для каждой группы лечения. Комбинированная терапия статистически превосходила каждый из видов монотерапии в снижении количества симптомов к 24-му мес, основной временной точке для этой конечной точки. К 24-му мес средние изменения по сравнению с исходным уровнем (± стандартное отклонение) общих баллов по шкале IPSS составили −6,2 (±7,14) для комбинированной терапии, −4,9 (±6,81) для монотерапии дутастеридом и −4,3 (±7,01) для монотерапии тамсулозином при средней разнице между комбинированной терапией и монотерапией дутастеридом −1,3 (p<0,001, 95% ДИ: −1,69; −0,86) и между комбинированной терапией и монотерапией тамсулозином −1,8 (p<0,001, 95% ДИ: −2,23; −1,4). Существенная разница наблюдалась к 9-му мес и сохранялась до 48 мес. На 48-м мес средние изменения по сравнению с исходным уровнем (± стандартное отклонение) общих оценок симптомов по IPSS составили −6,3 (±7,4) для комбинированной терапии, −5,3 (±7,14) для монотерапии дутастеридом и −3,8 (±7,74) для монотерапии тамсулозином при средней разнице между комбинированной терапией и монотерапией дутастеридом −0,96 (p<0,001, 95% ДИ: −1,4; −0,52) и между комбинированной терапией и монотерапией тамсулозином −2,5 (p< 0,001, 95% ДИ: −2,96; −2,07).
После 4 лет лечения комбинированная терапия с применением дутастерида и тамсулозина не давала преимущества по сравнению с монотерапией дутастеридом в отношении снижения частоты случаев развития острой задержки мочи или необходимости хирургического вмешательств, связанного с ДГПЖ.
Влияние на Qmax
Исходный Qmax составлял приблизительно 10,7 мл/с в каждой группе лечения. Комбинированная терапия статистически превосходила каждый вид монотерапии в отношении увеличения Qmax к 24-му мес, основной временной точке для этой конечной точки. Через 24 мес среднее увеличение Qmax по сравнению с исходным уровнем (± стандартное отклонение) составило 2,4 (±5,26) мл/с для комбинированной терапии, 1,9 (±5,1) мл/с для монотерапии дутастеридом и 0,9 (±4,57) мл/с для монотерапии тамсулозином при средней разнице между комбинированной терапией и монотерапией дутастеридом 0,5 мл/с (p= 0,003, 95% ДИ: 0,17; 0,84) и комбинированной терапией и монотерапией тамсулозином 1,5 мл/с (p<0,001, 95% ДИ: 1,19; 1,86). Эта разница отмечалась к 6-му мес и сохранялась до 24 мес. Дополнительное улучшение Qmax при комбинированной терапии по сравнению с монотерапией дутастеридом не было статистически значимым через 48 мес.
Влияние на объем предстательной железы
Средний объем простаты на момент включения в исследование был приблизительно 55 см3. К 24 мес, основной временной точке для этой конечной точки, среднее изменение объема простаты от исходного уровня (± стандартное отклонение) составило −26,9% (±22,57) для комбинированной терапии, −28% (±24,88) для монотерапии дутастеридом и 0% (±31,14) для монотерапии тамсулозином при средней разнице между комбинированной терапией и монотерапией дутастеридом 1,1% (p=результат недостоверен, 95% ДИ: −0,6; 2,8) и комбинированной терапией и монотерапией тамсулозином −26,9% (p<0,001, 95% ДИ: −28,9; −24,9). Аналогичные изменения наблюдались и на 48-м мес: −27,3% (±24,91), −28% (±25,74) и +4,6% (±35,45).
ДГПЖ с клиническими проявлениями у мужчин с увеличенной предстательной железой (монотерапия и в сочетании с альфа-адреноблокатором) в целях улучшения симптоматики, снижения риска острой задержки мочи и необходимости хирургического вмешательства по поводу аденомы предстательной железы. Дутастерид не предназначен для профилактики рака простаты.
Клинически значимая гиперчувствительность (например, серьезные кожные реакции, ангионевротический отек) к дутастериду или другим ингибиторам 5-альфа-редуктазы в анамнезе.
Результаты клинических исследований
Поскольку клинические исследования проводятся в различных условиях, частота побочных реакций, наблюдаемая в одном исследовании, не может напрямую сравниваться с показателями другого клинического исследования и может не отражать частоту, наблюдаемую на практике.
Данные клинических исследований с применением дутастерида в качестве монотерапии или в комбинации с тамсулозином
Наиболее частыми побочными реакциями, о которых сообщалось у пациентов, получавших дутастерид, были импотенция, снижение либидо, патология молочной железы (включая увеличение и болезненность) и нарушения эякуляции. При комбинированной терапии (дутастерид + тамсулозин) наиболее часто отмечались такие побочные реакции, как импотенция, снижение либидо, патология молочной железы (включая увеличение и болезненность), нарушения эякуляции и головокружение. Нарушения эякуляции значительно чаще встречались у пациентов, получавших комбинированную терапию (11%), по сравнению с применением дутастерида или тамсулозина в качестве монотерапии (соответственно 2 и 4%).
В плацебо-контролируемых исследованиях с применением дутастерида отмена лечения из-за побочных реакций наблюдалась у 4% пациентов, получавших дутастерид, и у 3% пациентов, получавших плацебо. Наиболее частой причиной отмены лечения была импотенция (1%).
В клиническом исследовании по оценке комбинированной терапии отмена лечения из-за побочных реакций наблюдалась у 6% пациентов, получавших дутастерид в комбинации с тамсулозином, и у 4% пациентов, получавших дутастерид или тамсулозин в качестве монотерапии. Наиболее частой причиной отмены лечения была эректильная дисфункция (от 1 до 1,5%).
Монотерапия
В трех идентичных 2-летних плацебо-контролируемых двойных слепых исследованиях III стадии с последующим 2-летним открытым периодом более 4300 пациентов мужского пола с ДГПЖ были рандомизировны для получения плацебо или дутастерида в суточной дозе 0,5 мг. В течение двойного слепого исследования 2167 мужчин получали дутастерид, из них 1772 человека в течение 1 года и 1510 человек в течение 2 лет. С учетом открытого периода исследований 1009 пациентов получали дутастерид в течение 3 лет, а 812 — в течение 4 лет. Возраст популяции составлял от 47 до 94 лет (средний возраст 66 лет), более 90% из них были представителями европеоидной расы. В таблице 1 приведены клинические побочные реакции, о которых сообщалось как минимум у 1% субъектов, получавших дутастерид, и чаще, чем у пациентов, получавших плацебо.
Таблица 1
Побочные реакции, отмеченные у ≥1% субъектов в течение 24 мес и чаще в группах получавших дутастерид, чем в группах плацебо (объединенные данные рандомизированных двойных слепых плацебо-контролируемых исследований), по времени их возникновения
| Побочная реакция | Частота побочных реакций (%) по времени их возникновения (в скобках число участников в группах дутастерид/плацебо) | |||
| Месяцы 0–6 (2167/2158) | Месяцы 7–12 (1901/1922) | Месяцы 13–18 (1725/1714) | Месяцы 19–24 (1605/1555) | |
| Импотенция1 | ||||
| Дутастерид | 4,7 | 1,4 | 1 | 0,8 |
| Плацебо | 1,7 | 1,5 | 0,5 | 0,9 |
| Снижение либидо1 | ||||
| Дутастерид | 3 | 0,7 | 0,3 | 0,3 |
| Плацебо | 1,4 | 0,6 | 0,2 | 0,1 |
| Нарушения эякуляции1 | ||||
| Дутастерид | 1,4 | 0,5 | 0,5 | 0,1 |
| Плацебо | 0,5 | 0,3 | 0,1 | 0 |
| Патология молочной железы2 | ||||
| Дутастерид | 0,5 | 0,8 | 1,1 | 0,6 |
| Плацебо | 0,2 | 0,3 | 0,3 | 0,1 |
1 Эти побочные реакции сексуального характера связаны с лечением дутастеридом (включая монотерапию и комбинацию с тамсулозином). Эти побочные реакции могут сохраняться после прекращения лечения. Роль дутастерида в их сохранении неизвестна.
2 Включая болезненность и увеличение молочной железы.
Длительное лечение (до 4 лет)
Рак предстательной железы высокой степени злокачественности
В рандомизированном двойном слепом плацебо-контролируемом исследовании REDUCE участвовали мужчины (n=8231) от 50 до 75 лет с сывороточным уровнем ПСА от 2,5 до 10 нг/мл и отрицательным результатом биопсии простаты в течение предыдущих 6 мес. Они были рандомизированы для получения плацебо (n=4126) или дутастерида (n=4105) в суточной дозе 0,5 мг с продолжительностью до 4 лет. Средний возраст составлял 63 года, 91% из них были представителями европеоидной расы. Проводилась плановая биопсия простаты в соответствии с протоколом через 2 и 4 года лечения или внеплановая биопсия, если это было клинически показано. У пациентов, получавших дутастерид, наблюдалась более высокая частота развития рака предстательной железы с оценкой по шкале Глисона 8–10 (1%), по сравнению с получавшими плацебо (0,5%) (см. «Показания» и «Меры предосторожности»). В 7-летнем плацебо-контролируемом клиническом исследовании с другим ингибитором 5-альфа-редуктазы (финастерид в дозе 5 мг) наблюдались аналогичные результаты развития рака простаты с оценкой по шкале Глисона 8–10 (финастерид — 1,8%, плацебо — 1,1%). Не обнаружено клинической эффективности применения дутастерида у пациентов с раком предстательной железы.
Нарушения репродуктивной системы и патология молочной железы
В трех базовых плацебо-контролируемых исследованиях ДГПЖ с применением дутастерида, каждое из которых было продолжительностью 4 года, не выявлено доказательств возрастания числа случаев сексуальных побочных реакций (импотенция, снижение либидо и нарушение эякуляции) или патологии молочной железы с увеличением продолжительности лечения. В ходе этих трех исследований отмечен 1 случай рака молочной железы в группе получавших дутастерид и 1 случай в группе получавших плацебо. Ни в одной группе лечения в 4-летнем исследовании CombAT или 4-летнем исследовании REDUCE не сообщалось о случаях рака молочной железы.
Взаимосвязь между длительным применением дутастерида и новообразованием молочной железы у мужчин в настоящее время неизвестна.
Комбинированная терапия с альфа-адреноблокатором (CombAT)
В 4-летнем двойном слепом исследовании более 4800 субъектов мужского пола с ДГПЖ были рандомизированы для получения 0,5 мг дутастерида, 0,4 мг тамсулозина или комбинированной терапии (0,5 мг дутастерида плюс 0,4 мг тамсулозина) 1 раз в день. В целом 1623 пациента получали монотерапию дутастеридом, 1611 — монотерапию тамсулозином и 1610 — комбинированную терапию. Возраст популяции составлял от 49 до 88 лет (средний возраст 66 лет), из них 88% были представителями европеоидной расы. В таблице 2 суммированы побочные реакции, о которых сообщалось как минимум у 1% пациентов, получавших комбинированную терапию, и чаще, чем у пациентов, получавших монотерапию дутастеридом или тамсулозином.
Таблица 2
Побочные реакции, отмеченные в течение 48-месячного периода у ≥1% субъектов и чаще у получавших комбинированную терапию, чем в группах, получавших монотерапию, по времени их возникновения
| Число участников (n) по группам лечения и побочные реакции | Частота побочных реакций (%) по времени их возникновения | ||||
| 1-й год | 2-й год | 3-й год | 4-й год | ||
| Месяцы 0–6 | Месяцы 7–12 | ||||
| Число участников: | |||||
| Комбинированная терапия1 | 1610 | 1527 | 1428 | 1238 | 1200 |
| Дутастерид | 1623 | 1548 | 1464 | 1325 | 1200 |
| Тамсулозин | 1611 | 1545 | 1468 | 1281 | 1112 |
| Нарушения эякуляции2,3 | |||||
| Комбинированная терапия | 7,8 | 1,6 | 1 | 0,5 | <0,1 |
| Дутастерид | 1 | 0,5 | 0,5 | 0,2 | 0,3 |
| Тамсулозин | 2,2 | 0,5 | 0,5 | 0,2 | 0,3 |
| Импотенция3,4 | |||||
| Комбинированная терапия | 5,4 | 1,1 | 1,8 | 0,9 | 0,4 |
| Дутастерид | 4 | 1,1 | 1,6 | 0,6 | 0,3 |
| Тамсулозин | 2,6 | 0,8 | 1 | 0,6 | 1,1 |
| Снижение либидо3,5 | |||||
| Комбинированная терапия | 4,5 | 0,9 | 0,8 | 0,2 | 0 |
| Дутастерид | 3,1 | 0,7 | 1 | 0,2 | 0 |
| Тамсулозин | 2 | 0,6 | 0,7 | 0,2 | <0,1 |
| Патология молочной железы6 | |||||
| Комбинированная терапия | 1,1 | 1,1 | 0,8 | 0,9 | 0,6 |
| Дутастерид | 0,9 | 0,9 | 1,2 | 0,5 | 0,7 |
| Тамсулозин | 0,4 | 0,4 | 0,4 | 0,2 | 0 |
| Головокружение | |||||
| Комбинированная терапия | 1,1 | 0,4 | 0,1 | <0,1 | 0,2 |
| Дутастерид | 0,5 | 0,3 | 0,1 | <0,1 | <0,1 |
| Тамсулозин | 0,9 | 0,5 | 0,4 | <0,1 | 0 |
1 Комбинированная терапия: дутастерид 0,5 мг 1 раз в сутки плюс тамсулозин 0,4 мг 1 раз в сутки.
2 Включает аноргазмию, ретроградную эякуляцию, уменьшение объема семенной жидкости, снижение оргазмических ощущений, аномальный оргазм, задержку эякуляции, расстройство эякуляции, неспособность к эякуляции и преждевременную эякуляцию.
3 Эти побочные реакции сексуального характера связаны с лечением дутастеридом (включая монотерапию и комбинацию с тамсулозином). Эти побочные реакции могут сохраняться после прекращения лечения. Роль дутастерида в сохранении этих реакций неизвестна.
4 Включает эректильную дисфункцию и нарушение сексуального возбуждения.
5 Включает снижение либидо, расстройство либидо, потерю либидо, сексуальную дисфункцию и мужскую сексуальную дисфункцию.
6 Включает увеличение молочной железы, гинекомастию, набухание молочной железы, боль в груди, болезненность молочной железы, боль в сосках и набухание сосков.
Сердечная недостаточность
В исследовании CombAT после 4 лет лечения частота применения собирательного термина «сердечная недостаточность» у получавших комбинированную терапию (12 из 1610 пациентов, 0,7%) была выше, чем в любой группе получавших монотерапию: дутастерид — 2 из 1623 (0,1%) и тамсулозин — 9 из 1611 (0,6%). Комбинированная сердечная недостаточность также изучалась в отдельном 4-летнем плацебо-контролируемом исследовании, оценивавшем применение дутастерида у мужчин с риском развития рака предстательной железы. Частота развития сердечной недостаточности у пациентов, принимавших дутастерид, составила 0,6% (26 из 4105) по сравнению с 0,4% (15 из 4126) у пациентов, получавших плацебо. Большинство пациентов с сердечной недостаточностью в обоих исследованиях имели сопутствующие заболевания, связанные с повышенным риском развития сердечной недостаточности. Таким образом, клиническое значение численного дисбаланса по случаям сердечной недостаточности неизвестно. Причинно-следственной связи между применением дутастерида в монотерапии или в комбинации с тамсулозином и сердечной недостаточностью не установлено. Ни в одном исследовании не наблюдалось дисбаланса в частоте общих сердечно-сосудистых побочных эффектов.
Результаты пострегистрационных наблюдений
Побочные реакции, выявленные при применении дутастерида после регистрации, приведены ниже. Поскольку сообщения об этих реакциях поступали в добровольном порядке от популяции неустановленного размера, не всегда возможно надежно оценить их частоту или установить причинно-следственную связь с действием дутастерида. Эти реакции были выбраны для включения из-за сочетания их серьезности, частоты сообщений или потенциальной причинной связи с применением дутастерида.
Со стороны иммунной системы: реакции гиперчувствительности, включая сыпь, зуд, крапивницу, локализованный отек, серьезные кожные реакции и ангионевротический отек.
Новообразования: рак молочной железы у мужчин.
Нарушения психики: депрессивное настроение.
Со стороны репродуктивной системы и молочной железы: боль в яичках и отек яичек.
Перорально, 1 раз в день, независимо от приема пищи.
www.rxlist.com, 2021.
