Описание
Блокаторы кальциевых каналов (антагонисты кальция) — гетерогенная группа ЛС, имеющих одинаковый механизм действия, но различающихся по ряду свойств, в т.ч. по фармакокинетике, тканевой селективности, влиянии на ЧСС и др.
Ионы кальция играют важную роль в регуляции различных процессов жизнедеятельности организма. Проникая в клетки, они активируют биоэнергетические процессы (превращение АТФ в цАМФ, фосфорилирование белков и др.), обеспечивающие реализацию физиологических функций клеток. В повышенной концентрации (в т.ч. при ишемии, гипоксии и других патологических состояниях) они могут чрезмерно усиливать процессы клеточного метаболизма, увеличивать потребность тканей в кислороде и вызывать различные деструктивные изменения. Трансмембранный перенос ионов кальция осуществляется через специальные, т.н. кальциевые каналы. Каналы для ионов Са2+ достаточно разнообразны и сложны. Они расположены в синоатриальных, атриовентрикулярных путях, волокнах Пуркинье, миофибриллах миокарда, гладкомышечных клетках сосудов, скелетных мышцах и др.
Историческая справка. Первый клинически важный представитель антагонистов кальция — верапамил, был получен в 1961 г. в результате попыток синтезировать более активные аналоги папаверина, обладающего вазодилатирующим действием. В 1966 г. был синтезирован нифедипин, в 1971 г. — дилтиазем. Верапамил, нифедипин и дилтиазем — наиболее изученные представители антагонистов кальция, их считают препаратами-прототипами и характеристику новых ЛС этого класса принято давать в сравнении с ними.
В 1962 г. Хасс и Хартфелдер обнаружили, что верапамил не только расширяет кровеносные сосуды, но и обладает отрицательным инотропным и хронотропным эффектами (в отличие от других вазодилататоров, например нитроглицерина). В конце 60-х годов А. Флекенштейн предположил, что действие верапамила обусловлено снижением входа ионов Ca2+ в кардиомиоциты. При изучении действия верапамила на изолированных полосках сосочковой мышцы сердца животных он обнаружил, что препарат вызывает такой же эффект, как и удаление ионов Ca2+ из перфузионной среды, при добавлении ионов Ca2+ кардиодепрессивное действие верапамила снимается. Примерно в то же время было предложено называть препараты, близкие к верапамилу (прениламин, галлопамил и др.), антагонистами кальция.
В последующем выяснилось, что некоторые препараты из разных фармакологических групп также обладают способностью умеренно влиять на ток Ca2+ внутрь клетки (фенитоин, пропранолол, индометацин).
В 1963 г. верапамил был разрешен для клинического применения в качестве антиангинального средства (антиангинальные (анти + angina pectoris)/ антиишемические средства — лекарственные средства, увеличивающие приток крови к сердцу или снижающие его потребность в кислороде, применяемые для профилактики или купирования приступов стенокардии). Немного раньше с этой же целью было предложено другое производное фенилалкиламина — прениламин (Дифрил). В дальнейшем верапамил нашел широкое применение в клинической практике. Прениламин оказался менее эффективным и перестал использоваться как лекарственное средство.
Кальциевые каналы — это трансмембранные белки сложного строения, состоящие из нескольких субъединиц. Через эти каналы поступают также ионы натрия, бария и водорода. Различают потенциал-зависимые и рецептор-зависимые кальциевые каналы. Через потенциал-зависимые каналы ионы Са2+ проходят сквозь мембрану, как только ее потенциал снижается ниже определенного критического уровня. Во втором случае поток ионов кальция через мембраны регулируется специфическими агонистами (ацетилхолин, катехоламины, серотонин, гистамин и др.) при их взаимодействии с рецепторами клетки.
В настоящее время выделяют несколько типов кальциевых каналов (L, T, N, P, Q, R), обладающих разными свойствами (в т.ч. проводимость, длительность открытия) и имеющих разную тканевую локализацию.
Каналы L-типа (long-lаsting large-capacitance, от англ. long-lаsting — долгоживущий, large — большой; имеется в виду проводимость канала) медленно активируются при деполяризации клеточной мембраны и обусловливают медленный вход ионов Са2+ в клетку и формирование медленного кальциевого потенциала, например в кардиомиоцитах. Каналы L-типа локализованы в кардиомиоцитах, в клетках проводящей системы сердца (синоаурикулярном и AV узлах), гладкомышечных клетках артериальных сосудов, бронхов, матки, мочеточников, желчного пузыря, ЖКТ, в клетках скелетных мышц, тромбоцитах.
Медленные кальциевые каналы образованы крупной α1-субъединицей, формирующей собственно канал, а также более мелкими дополнительными субъединицами — α2, β, γ, δ. Альфа1-субъединица (молекулярная масса 200–250 тыс.) соединена с комплексом субъединиц α2β (молекулярная масса около 140 тыс.) и внутриклеточной β-субъединицей (молекулярная масса 55–72 тыс.). Каждая α1-субъединица состоит из 4-х гомологичных доменов (I, II, III, IV), а каждый домен — из 6 трансмембранных сегментов (S1–S6). Комплекс субъединиц α2β, и β-субъединица могут влиять на свойства α1-субъединицы.
Каналы T-типа — транзиторные (от англ. transient — скоротечный, кратковременный; имеется в виду время открытия канала), быстро инактивируются. Каналы Т-типа называют низкопороговыми, т.к. они открываются при разности потенциалов 40 мВ, тогда как каналы L-типа относят к высокопороговым — они открываются при 20 мВ. Каналы Т-типа играют важную роль в генерации сердечных сокращений; кроме того, они принимают участие в регуляции проводимости в предсердно-желудочковом узле. Кальциевые каналы Т-типа обнаружены в сердце, нейронах, а также в таламусе, различных секреторных клетках и др. Каналы N-типа (от англ. neuronal — имеется в виду преимущественное распределение каналов) обнаружены в нейронах. N-каналы активируются при переходе от очень отрицательных значений мембранного потенциала к сильной деполяризации и регулируют секрецию нейромедиаторов. Ток ионов Са2+ через них в пресинаптических окончаниях ингибируется норадреналином через α-рецепторы. Каналы P-типа, выявленные первоначально в клетках Пуркинье мозжечка (отсюда и происходит их название), обнаружены в гранулярных клетках и в гигантских аксонах кальмара. Каналы N-, P-, Q- и недавно описанного R-типов, видимо, регулируют секрецию нейромедиаторов.
В клетках сердечно-сосудистой системы расположены преимущественно медленные кальциевые каналы L-типа, а также T- и R-типов, причем в гладкомышечных клетках сосудов содержатся каналы трех типов (L, T, R), в клетках миокарда — в основном L-типа, а в клетках синусного узла и нейрогормональных клетках — каналы Т-типа.
Классификация антагонистов кальция
Существует много классификаций БКК — в зависимости от химического строения, тканевой специфичности, продолжительности действия и др.
Наиболее широко используется классификация, отражающая химическую гетерогенность антагонистов кальция.
Исходя из химической структуры обычно антагонисты кальция L-типа подразделяют на следующие группы:
— фенилалкиламины (верапамил, галлопамил и др.);
— 1,4-дигидропиридины (нифедипин, нитрендипин, нимодипин, амлодипин, лацидипин, фелодипин, никардипин, исрадипин, лерканидипин и др.);
— бензотиазепины (дилтиазем, клентиазем и др.);
— дифенилпиперазины (циннаризин, флунаризин);
— диариламинопропиламины (бепридил).
С практической точки зрения в зависимости от влияния на тонус симпатической нервной системы и ЧСС, антагонисты кальция делят на две подгруппы — рефлекторно увеличивающие (производные дигидропиридина) и уменьшающие (верапамил и дилтиазем, по действию во многом сходны с бета-адреноблокаторами) ЧСС.
В отличие от дигидропиридинов (обладающих незначительным отрицательным инотропным эффектом) фенилалкиламины и бензотиазепины обладают отрицательным инотропным (снижение сократительной способности миокарда) и отрицательным хронотропным (замедление ритма сердца) действием.
Согласно классификации, приведенной И.Б. Михайловым (2001 г.), БКК делят на три поколения:
Первое поколение:
а) верапамил (Изоптин, Финоптин) — производные фенилалкиламина;
б) нифедипин (Фенигидин, Адалат, Коринфар, Кордафен, Кордипин) — производные дигидропиридина;
в) дилтиазем (Диазем, Дилтиазем) — производные бензотиазепина.
Второе поколение:
a) группа верапамила: галлопамил, анипамил, фалипамил;
б) группа нифедипина: исрадипин (Ломир), амлодипин (Норваск), фелодипин (Плендил), нитрендипин (Октидипин), нимодипин (Нимотоп), никардипин, лацидипин (Лаципил), риодипин (Форидон);
в) группа дилтиазема: клентиазем.
По сравнению с БКК первого поколения, БКК второго поколения имеют бóльшую продолжительность действия, более высокую тканевую специфичность и меньше побочных эффектов.
У представителей БКК третьего поколения (нафтопидил, эмопамил, лерканидипин), имеется ряд дополнительных свойств, например альфа-адренолитическая (нафтопидил) и симпатолитическая активность (эмопамил).
Фармакологические свойства
Фармакокинетика. БКК вводят парентерально, принимают перорально и сублингвально. Большинство антагонистов кальция назначают внутрь. Формы для парентерального введения существуют у верапамила, дилтиазема, нифедипина, нимодипина. Сублингвально применяют нифедипин (например при гипертоническом кризе; таблетку рекомендуют разжевать).
Будучи липофильными соединениями, при приеме внутрь большинство БКК быстро абсорбируются, но в связи с эффектом «первого прохождения» через печень биодоступность очень вариабельна. Исключение составляют амлодипин, исрадипин и фелодипин, которые медленно всасываются. Связывание с белками крови, преимущественно с альбумином, высокое (70–98%). Tmax составляет 1–2 ч для ЛС I поколения и 3–12 ч для БКК II–III поколения и зависит также от лекформы. При сублингвальном приеме Cmax достигается в течение 5–10 мин. В среднем T1/2 из крови для БКК I поколения — 3–7 ч, для БКК II поколения — 5–11 ч. БКК хорошо проникают в органы и ткани, объем распределения — 5–6 л/кг. БКК практически полностью биотрансформируются в печени, метаболиты обычно неактивны. Однако у некоторых антагонистов кальция имеются активные производные — норверапамил (T1/2 около 10 ч, обладает примерно 20% гипотензивной активности верапамила), дезацетилдиазем (25–50% коронарорасширяющей активности исходного соединения — дилтиазема). Выводятся преимущественно почками (80–90%), частично через печень. При многократном приеме внутрь биодоступность может увеличиваться, а выведение — замедляться (из-за насыщения печеночных ферментов). Такие же изменения фармакокинетических параметров отмечаются при циррозе печени. Элиминация замедляется также у пожилых пациентов. Длительность действия БКК I поколения — 4–6 ч, II поколения — в среднем 12 ч.
Основной механизм действия антагонистов кальция заключается в том, что они тормозят проникновение ионов кальция из экстрацеллюлярного пространства в мышечные клетки сердца и сосудов через медленные кальциевые каналы L-типа. Снижая концентрацию ионов Ca2+ в кардиомиоцитах и клетках гладкой мускулатуры сосудов, они расширяют коронарные артерии и периферические артерии и артериолы, оказывают выраженное сосудорасширяющее действие.
Спектр фармакологической активности антагонистов кальция включает влияние на сократимость миокарда, активность синусного узла и AV проводимость, тонус сосудов и сосудистое сопротивление, функцию бронхов, органов желудочно-кишечного тракта и мочевыводящих путей. Эти препараты обладают способностью тормозить агрегацию тромбоцитов и модулировать выделение нейромедиаторов из пресинаптических окончаний.
Влияние на сердечно-сосудистую систему
Сосуды. Для сокращения гладкомышечных клеток сосудов необходим кальций, который, поступая в цитоплазму клетки, образует комплекс с кальмодулином. Образующийся комплекс активирует киназу легких цепей миозина, что приводит к их фосфорилированию и возможности образования поперечных мостиков между актином и миозином, результатом чего является сокращение гладкомышечных волокон.
Антагонисты кальция, блокируя L-каналы, нормализуют трансмембранный ток ионов Ca2+, нарушенный при ряде патологических состояний, прежде всего при артериальной гипертензии. Все антагонисты кальция вызывают расслабление артерий и почти не влияют на тонус вен (не меняют преднагрузку).
Сердце. Нормальная функция сердечной мышцы зависит от потоков ионов кальция. Для сопряжения возбуждения и сокращения во всех клетках сердца требуется вход ионов кальция. В миокарде, поступая внутрь кардиомиоцита, Ca2+связывается с белковым комплексом — так называемым тропонином, при этом изменяется конформация тропонина, устраняется блокирующий эффект комплекса тропонин-тропомиозин, образуются актомиозиновые мостики, вследствие чего происходит сокращение кардиомиоцита.
Уменьшая ток внеклеточных ионов кальция, БКК вызывают отрицательный инотропный эффект. Отличительной чертой дигидропиридинов является то, что они преимущественно расширяют периферические сосуды, что приводит к выраженному барорефлекторному повышению тонуса симпатической нервной системы и их отрицательный инотропный эффект нивелируется.
В клетках синусного и AV узлов деполяризация обусловлена главным образом входящим кальциевым током. Влияние нифедипина на автоматизм и AV проведение обусловлено уменьшением количества функционирующих кальциевых каналов при отсутствии воздействия на время их активации, инактивации и восстановления.
При повышении ЧСС степень блокады каналов, вызванной нифедипином и другими дигидропиридинами, практически не меняется. В терапевтических дозах дигидропиридины не угнетают проведение по AV узлу. Напротив, верапамил не только снижает ток кальция, но и тормозит деинактивацию каналов. При этом чем выше ЧСС, тем больше степень блокады, вызванной верапамилом, а также дилтиаземом (в меньшей степени) — это явление называют частотозависимостью. Верапамил и дилтиазем снижают автоматизм, замедляют AV проведение.
Бепридил блокирует не только медленные кальциевые, но и быстрые натриевые каналы. Он оказывает прямой отрицательный инотропный эффект, уменьшает ЧСС, вызывает удлинение интервала QT и может провоцировать развитие полиформной желудочковой тахикардии.
В регуляции деятельности сердечно-сосудистой системы принимают участие также кальциевые каналы Т-типа, которые в сердце локализуются в синусно-предсердном и предсердно-желудочковом узлах, а также в волокнах Пуркинье. Был создан антагонист кальция — мибефрадил, который блокирует каналы L- и Т-типа. При этом чувствительность к нему каналов L-типа в 20–30 меньше, чем чувствительность Т-каналов. Практическое использование этого препарата для лечения артериальной гипертензии и хронической стабильной стенокардии было приостановлено в связи с серьезными побочными эффектами, обусловленными, по-видимому, ингибированием Р-гликопротеина и изофермента CYP3A4 цитохрома Р450, а также из-за нежелательного взаимодействия со многими кардиотропными препаратами.
Тканевая селективность. В наиболее общем виде различия в действии БКК на сердечно-сосудистую систему заключаются в том, что верапамил и другие фенилалкиламины действуют преимущественно на миокард, в т.ч. на AV проводимость и в меньшей степени на сосуды, нифедипин и другие дигидропиридины, в большей степени — на мышцы сосудов и меньше — на проводящую систему сердца, причем у некоторых имеется избирательная тропность к коронарным (нисолдипин — в России не зарегистрирован) или мозговым (нимодипин) сосудам; дилтиазем занимает промежуточное положение и примерно в равной степени влияет на сосуды и проводящую систему сердца, но слабее, чем предыдущие.
Эффекты БКК. Тканевая селективность БКК обусловливает различие их эффектов. Так, верапамил вызывает умеренную вазодилатацию, нифедипин — выраженное расширение сосудов.
Фармакологические эффекты ЛС группы верапамила и дилтиазема сходны: они обладают отрицательным ино-, хроно- и дромотропным действием — могут снижать сократительную способность миокарда, уменьшать ЧСС, замедлять предсердно-желудочковую проводимость. В литературе их иногда называют «кардиоселективными» или «брадикардическими» БКК. Созданы антагонисты кальция (преимущественно дигидропиридины), отличающиеся высокоспецифическим влиянием на отдельные органы и сосудистые регионы. Нифедипин и другие дигидропиридины называют «вазоселективными» или «вазодилатирующими» БКК. Нимодипин, обладающий высокой липофильностью, был разработан как препарат, действующий на мозговые сосуды для снятия их спазма. При этом дигидропиридины не оказывают клинически значимого влияния на функцию синусного узла и предсердно-желудочковую проводимость, обычно не влияют на ЧСС (однако ЧСС может увеличиваться в результате рефлекторной активации симпато-адреналовой системы в ответ на резкое расширение системных артерий).
Антагонисты кальция оказывают выраженное сосудорасширяющее действие и обладают следующими эффектами: антиангинальный/антиишемический, гипотензивный, органопротективный (кардиопротективный, нефропротективный), антиатерогенный, антиаритмический, снижение давления в легочной артерии и дилатация бронхов — характерно для некоторых БКК (дигидропиридины), снижение агрегации тромбоцитов.
Антиангинальный/антиишемический эффект обусловлен как прямым действием на миокард и коронарные сосуды, так и влиянием на периферическую гемодинамику. Блокируя поступление ионов кальция в кардиомиоциты, БКК снижают механическую работу сердца и уменьшают потребление кислорода миокардом. Расширение периферических артерий вызывает снижение периферического сопротивления и АД (снижение постнагрузки), что приводит к уменьшению напряжения стенки миокарда и потребности миокарда в кислороде.
Гипотензивный эффект связан с периферической вазодилатацией, при этом снижается ОПСС, понижается АД, повышается приток крови к жизненно важным органам — сердцу, головному мозгу, почкам. Гипотензивный эффект антагонистов кальция сочетается с умеренным диуретическим и натрийуретическим действием, что приводит к дополнительному снижению ОПСС и ОЦК.
Кардиопротективный эффект связан с тем, что вызываемая БКК вазодилатация приводит в снижению ОПСС и АД и, соответственно, к уменьшению постнагрузки, что уменьшает работу сердца и потребность миокарда в кислороде и может приводить к регрессу гипертрофии миокарда левого желудочка и улучшению диастолической функции миокарда.
Нефропротективный эффект обусловлен устранением вазоконстрикции почечных сосудов и повышением почечного кровотока. Кроме того, БКК увеличивают скорость клубочковой фильтрации. Увеличивается натрийурез, дополняющий гипотензивное действие.
Имеются данные об антиатерогенном (антисклеротическом) эффекте, полученные в исследованиях в культуре ткани аорты человека, у животных, а также в ряде клинических исследований.
Антиаритмический эффект. К БКК, обладающим выраженной антиаритмической активностью, относятся верапамил, дилтиазем. Антагонисты кальция дигидропиридиновой природы антиаритмической активностью не обладают. Антиаритмический эффект связан с угнетением деполяризации и замедлением проведения в AV узле, что отражается на ЭКГ удлинением интервала QT. Антагонисты кальция могут угнетать фазу спонтанной диастолической деполяризации и подавлять тем самым автоматизм, прежде всего синоатриального узла.
Уменьшение агрегации тромбоцитов связано с нарушением синтеза проагрегантных простагландинов.
Основное применение антагонистов ионов кальция обусловлено их влиянием на сердечно-сосудистую систему. Вызывая расширение сосудов и уменьшая ОПСС, они понижают АД, улучшают коронарный кровоток и редуцируют кислородный запрос миокарда. Эти препараты понижают АД пропорционально дозе, в терапевтических дозах незначительно влияют на нормальное АД, не вызывают ортостатических явлений.
Общими показаниями к назначению всех БКК являются артериальная гипертензия, стенокардия напряжения, вазоспастическая стенокардия (Принцметала), однако фармакологические особенности различных представителей этой группы определяют дополнительные показания (а также и противопоказания) к их применению.
Препараты этой группы, влияющие на возбудимость и проводимость сердечной мышцы, находят применение в качестве антиаритмиков, их выделяют в отдельную группу (IV класс антиаритмических средств). Антагонисты кальция применяются при наджелудочковой (синусовой) тахикардии, тахиаритмии, экстрасистолии, трепетании и мерцании предсердий.
Эффективность БКК при стенокардии напряжения обусловлена тем, что они расширяют коронарные артерии и снижают потребность миокарда в кислороде (вследствие понижения АД, ЧСС и сократимости миокарда). В плацебо-контролируемых исследованиях показано, что БКК снижают частоту приступов стенокардии и уменьшают депрессию сегмента ST при физической нагрузке.
Развитие вазоспастической стенокардии определено снижением коронарного кровотока, а не повышением потребности миокарда в кислороде. Действие БКК в данном случае, вероятно, опосредовано расширением коронарных артерий, а не влиянием на периферическую гемодинамику. Предпосылкой для применения БКК при нестабильной стенокардии являлась гипотеза, согласно которой ведущую роль в ее развитии играет спазм коронарных артерий.
Если стенокардия сопровождается суправентрикулярными (наджелудочковыми) нарушениями ритма, тахикардией — применяют препараты группы верапамила или дилтиазема. Если стенокардия сочетается с брадикардией, нарушениями AV проводимости и артериальной гипертензией — предпочтительными являются препараты группы нифедипина.
Дигидропиридины (нифедипин в лекарственной форме с медленным высвобождением, лацидипин, амлодипин) являются препаратами выбора при лечении артериальной гипертензии у пациентов с поражением сонных артерий.
При гипертрофической кардиомиопатии, сопровождающейся нарушением процесса расслабления сердца в диастолу, используют препараты группы верапамила второго поколения.
До настоящего времени не получено доказательств эффективности БКК на ранней стадии инфаркта миокарда или для его вторичной профилактики. Есть данные, свидетельствующие, что дилтиазем и верапамил могут снижать риск повторного инфаркта у пациентов после первого инфаркта без патологического зубца Q, которым противопоказаны бета-адреноблокаторы.
БКК используют для симптоматического лечения болезни и синдрома Рейно. Показано, что нифедипин, дилтиазем и нимодипин уменьшают симптомы болезни Рейно. Следует отметить, что БКК первого поколения — верапамил, нифедипин, дилтиазем характеризуются короткой продолжительностью действия, обусловливающей необходимость 3–4 кратного приема в течение суток и сопровождающейся колебаниями вазодилатирующего и гипотензивного эффекта. Лекарственные формы с замедленным высвобождением антагонистов кальция второго поколения обеспечивают постоянство терапевтической концентрации и увеличивают продолжительность действия препарата.
Клиническими критериями эффективности применения антагонистов кальция являются нормализация АД, уменьшение частоты болевых приступов за грудиной и в области сердца, возрастание толерантности к физической нагрузке.
БКК используются также в комплексной терапии заболеваний ЦНС, в т.ч. болезни Альцгеймера, сенильной деменции, хореи Гентингтона, алкоголизма, вестибулярных расстройств. При неврологических расстройствах, связанных с субарахноидальным кровоизлиянием, применяют нимодипин и никардипин. БКК назначают для предупреждения холодового шока, для устранения заикания (за счет подавления спастического сокращения мышц диафрагмы).
В ряде случаев целесообразность назначения антагонистов кальция обусловлена не столько их эффективностью, сколько наличием противопоказаний для назначения ЛС других групп. Например, при ХОБЛ, перемежающейся хромоте, сахарном диабете типа 1 может быть противопоказан или нежелателен прием бета-адреноблокаторов.
Ряд особенностей фармакологического действия БКК дает им ряд преимуществ в сравнении с другими сердечно-сосудистыми средствами. Так, антагонисты кальция метаболически нейтральны — для них характерно отсутствие неблагоприятного влияния на обмен липидов, углеводов; они не повышают тонус бронхов (в отличие от бета-адреноблокаторов); не снижают физическую и умственную активность, не вызывают импотенции (как бета-адреноблокаторы и диуретики), не вызывают депрессию (как, например, препараты резерпина, клонидин). БКК не влияют на электролитный баланс, в т.ч. на уровень калия в крови (как диуретики и ингибиторы АПФ).
Противопоказаниями к назначению антагонистов кальция являются выраженная артериальная гипотензия (сАД ниже 90 мм рт. ст.), синдром слабости синусного узла, острый период инфаркта миокарда, кардиогенный шок; для группы верапамила и дилтиазема — AV блокада различной степени, выраженная брадикардия,WPW-синдром; для группы нифедипина — выраженная тахикардия, аортальный и субаортальный стеноз.
При сердечной недостаточности следует избегать применения БКК. С осторожностью назначают БКК больным с выраженным стенозом митрального клапана, тяжелыми нарушениями мозгового кровообращения, непроходимостью ЖКТ.
Побочные эффекты разных подгрупп антагонистов кальция сильно различаются. Неблагоприятные эффекты БКК, особенно дигидропиридинов, обусловлены чрезмерным расширением сосудов — возможны головная боль (очень часто), головокружение, артериальная гипотензия, отеки (в т.ч. стоп и лодыжек ног, локтей); при применении нифедипина — приливы (покраснение кожи лица, ощущение жара), рефлекторная тахикардия (иногда); нарушения проводимости — AV блокада. В то же время при применении дилтиазема и, особенно, верапамила, возрастает риск проявления присущих каждому препарату эффектов — угнетение функции синусного узла, AV проводимости, отрицательный инотропный эффект. В/в введение верапамила у пациентов, принимавших до этого бета-адреноблокаторы (и наоборот), может вызвать асистолию.
Возможны диспептические явления, запор (чаще при использовании верапамила). Редко возникают сыпь, сонливость, кашель, одышка, повышение активности печеночных трансаминаз. Редкими побочными явлениями являются сердечная недостаточность и лекарственный паркинсонизм.
Применение при беременности. В соответствии с рекомендациями FDA (Food and Drug Administration), определяющими возможность применения ЛС при беременности, препараты из группы блокаторов кальциевых каналов по действию на плод относятся к категории C FDA (Изучение репродукции на животных выявило неблагоприятное действие на плод, а адекватных и строго контролируемых исследований у беременных женщин не проведено, однако потенциальная польза, связанная с применением ЛС у беременных, может оправдывать их использование, несмотря на возможный риск).
Применение в период грудного вскармливания. Хотя осложнений у человека не зарегистрировано, дилтиазем, нифедипин, верапамил и, возможно, другие БКК проникают в грудное молоко. Относительно нимодипина неизвестно, проникает ли он в женское грудное молоко, однако нимодипин и/или его метаболиты обнаруживаются в молоке крыс в более высоких концентрациях, чем таковые в крови. Верапамил проникает в грудное молоко, проходит через плаценту и определяется в крови пупочной вены в родах. Быстрое в/в введение вызывает гипотензию у матери, приводящую к дистрессу плода.
Нарушение функции печени и почек. При заболеваниях печени необходимо снижение дозы БКК. При почечной недостаточности корректировка дозы необходима только при применении верапамила и дилтиазема вследствие возможности их кумуляции.
Педиатрия. БКК следует применять с осторожностью у детей до 18 лет, т.к. их эффективность и безопасность не установлены. Однако специфических педиатрических проблем, которые ограничивали бы применении БКК в этой возрастной группе, не предполагают. В редких случаях после в/в введения верапамила у новорожденных и грудных детей были отмечены тяжелые побочные гемодинамические эффекты.
Гериатрия. У пожилых людей БКК следует применять в низких дозах, т.к. у этой категории пациентов метаболизм в печени снижен. При изолированной систолической гипертонии и склонности к брадикардии предпочтительнее назначать производные дигидропиридина пролонгированного действия.
Взаимодействие антагонистов кальция с другими ЛС. Нитраты, бета-адреноблокаторы, ингибиторы АПФ, диуретики, трициклические антидепрессанты, фентанил, алкоголь усиливают гипотензивный эффект. При одновременном применении НПВС, сульфаниламидов, лидокаина, диазепама, непрямых антикоагулянтов возможно изменение связывания с белками плазмы, значительное увеличение свободной фракции БКК и, соответственно, увеличение риска побочных эффектов и передозировки. Верапамил усиливает токсическое действие карбамазепина на ЦНС.
Опасно вводить БКК (особенно группы верапамила и дилтиазема) с хинидином, прокаинамидом и сердечными гликозидами, т.к. возможно чрезмерное снижение ЧСС. Сок грейпфрута (большое количество) увеличивает биодоступность.
Антагонисты кальция могут применяться в комбинированной терапии. Особенно эффективно сочетание производных дигидропиридина с бета-адреноблокаторами. При этом происходит потенцирование гемодинамических эффектов каждого из препаратов и усиление гипотензивного действия. Бета-адреноблокаторы препятствуют активации симпато-адреналовой системы и развитию тахикардии, возможной в начале лечения БКК, а также снижают вероятность развития периферических отеков.
В заключение можно отметить, что антагонисты кальция являются эффективными средствами для лечения сердечно-сосудистых заболеваний. Для оценки эффективности и своевременного выявления нежелательного действия БКК во время лечения необходимо проводить мониторинг АД, ЧСС, AV проводимости, важно также контролировать наличие и степень выраженности сердечной недостаточности (появление сердечной недостаточности может служить причиной отмены БКК).
Блокаторы медленных кальциевых каналов (БКК; синонимы: блокаторы кальциевых каналов, антагонисты кальция) относятся к одному из основных классов лекарственных средств, применяющихся при артериальной гипертонии (АГ). В практической деятельности врачу часто приходится выбирать, какому препарату следует отдать предпочтение при назначении терапии. При этом выбор оказывается достаточно широким. Выраженность их основного действия, особенности фармакодинамики, преимущества или, наоборот, негативный профиль воздействия в тех или иных клинических ситуациях, а также взаимодействие с препаратами других групп – все это имеет большое значение, и знание этих моментов позволяет решить проблему выбора.
Неоднократно описанные в литературе негативные последствия применения БКК первого поколения, в основном у больных ИБС и СН, по–видимому, до сих пор препятствуют более широкому применению современных БКК, имеющих отличный от них фармакодинамический профиль и доказавших свою эффективность во многих исследованиях. Этому мешает и рутинное назначение больным АГ комбинированной терапии из препаратов других групп, без сомнения эффективных, но иногда уступающих БКК по набору так называемых плейотропных эффектов.
БКК – довольно разнородная группа лекарственных препаратов. Они отличаются друг от друга по химической структуре, фармакодинамике, клиническим и возможным побочным эффектам. Основной механизм их действия – уменьшение поступления Са2+ через кальциевые L–каналы, чувствительные к БКК. Строго говоря, БКК не вступают в какой–либо антагонизм с ионами кальция и не блокируют кальциевые каналы, но влияют на их модуляцию, увеличивая и/или уменьшая продолжительность разных фаз состояния (фаза 0 – закрытые каналы, N1 и N2 – открытые каналы), и изменяя, таким образом, кальциевый ток. Как известно, сокращение гладкомышечных клеток сосудов зависит от концентрации Са2+ в цитоплазме, и если подавить трансмембранный вход Са2+, его количество в цитоплазме клетки и ее готовность к сокращению уменьшатся. Все БКК, расслабляя гладкие мышцы артериол, снижают АД и общее периферическое сопротивление сосудов (ОПСС).
Из особенностей фармакокинетики БКК следует отметить то, что они метаболизируются в печени и выводятся в основном с мочой. При заболеваниях почек фармакокинетика БКК мало изменяется, тогда как при болезнях печени их период полужизни и биодоступность увеличиваются [1]. В литературе не отмечается эффекта привыкания к БКК. Это, по–видимому, объясняется тем, что длительное введение БКК не оказывает существенного влияния на плотность и чувствительность рецепторов к ним в кальциевых каналах. При длительном применении верапамила и дилтиазема наблюдается их кумуляция. При этом время полужизни верапамила и его активного метаболита норверапамила увеличивается в два раза (до 10 ч), хотя активность последнего составляет 1/8 активности верапамила [1].
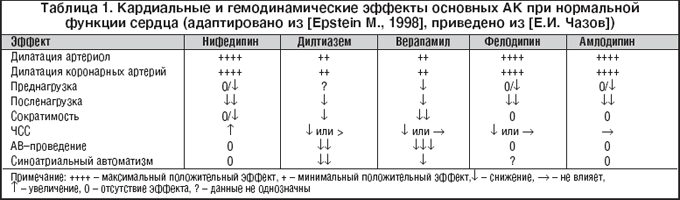
В клинической практике применяются препараты 3 подгрупп: фенилалкиламины (верапамил), дигидропиридины (нифедипин, амлодипин, исрадипин и др.) и бензодиазепины (дилтиазем). Поскольку верапамил и дилтиазем проявляют определенное сходство между собой, их часто объединяют в одну условную подгруппу «недигидропиридиновые». По одной из классификаций с учетом органоспецифичности (Singh, 1986) препараты этой объединенной группы относятся к БКК I типа, которые проявляют свое действие на сердце, сосуды и проводящую систему сердца. Дигидропиридиновые препараты относятся к БКК II типа с преимущественно сосудистым эффектом (всего по этой классификации различают 4 типа БКК). Между препаратами этих двух подгрупп действительно имеются существенные фармакодинамические различия и, в частности, в характере влияния на сердечно–сосудистую систему (табл. 1). Так, дигидропиридиновые БКК в отличие от верапамила и дилтиазема (проявляя свою сосудистую селективность) значительно снижают ОПСС, практически не влияют на проводимость сердца и очень слабо влияют на его сократительную функцию.
В подгруппе дигидропиридинов по своим улучшенным (по сравнению с нифедипином) характеристикам выделяются препараты длительного действия, в частности, амлодипин (Нормодипин). Главной его особенностью с точки зрения клинического применения является большая продолжительность действия (Т1/2 равен 35–50 ч). Его сывороточная концентрация и эффект нарастают в течение 5–7 дней лечения [2]. Действие амлодипина проявляется медленно, так как растворимость в жирах в 3–4 раза ниже, чем у нифедипина. Кроме того, он обладает в небольшой степени также свойствами дилтиазема, поскольку частично связывается с его рецепторами [1].
Антигипертензивная эффективность
Монотерапия БКК в равной степени эффективна при мягкой и умеренной АГ [2]. В многочисленных плацебо–контролируемых и сравнительных исследованиях была показана хорошая эффективность БКК при лечении АГ. Антигипертензивный эффект БКК дозозависимый. Так, в ранних исследованиях при использовании средних и высоких доз разных препаратов (верапамил, дилтиазем, нифедипин, риодипин) систолическое АД (САД) снижалось приблизительно на 20–30 (до 40) мм рт.ст., диастолическое (ДАД) – на 10–20 мм рт.ст. При этом разница в эффективности этих препаратов между собой либо не достигала уровня достоверности, в том числе при длительном лечении [3], либо снижение АД было более выраженным при лечении нифедипином [4,5]. По данным сравнительных исследований, БКК снижают АД, по крайней мере, столь же эффективно, как b–блокаторы и диуретики, а также иАПФ [6–8]. В недавнем крупном исследовании ALLHAT (33357 больных) амлодипин продемонстрировал равную антигипертензивную активность при сравнении с хлорталидоном и лизиноприлом. Разница состояла лишь в том, что хлорталидон лучше снижал систолическое давление, а амлодипин – диастолическое. Вместе с тем профиль снижения АД в качестве результата лечения в группе амлодипина оказался более приемлемым, т.е. число случаев повышения или чрезмерного снижения АД в этой группе было меньше, чем в других [8].
Влияние на сердечно–сосудистую
систему
Все БКК вызывают расширение артериол и коронарных артерий. В большей степени это свойство присуще препаратам подгруппы дигидропиридинов. Характерным для них, если они применяются в терапевтических дозах, является отсутствие или слабое влияние на сократимость и функцию проводимости сердца. Особенного внимания в этом отношении заслуживают долгодействующие препараты амлодипин и фелодипин. По гемодинамическому эффекту амлодипин (Нормодипин) близок другим дигидропиридинам – никардипину и нисольдипину и отличается от верапамила и дилтиазема. Препарат снижает АД, ОПСС и увеличивает сердечный индекс и ЧСС. При длительном применении реакция ЧСС уменьшается. Отрицательный инотропный эффект при применении амлодипина менее выражен и наступает позже, чем у нифедипина [1].
Рефлекторное повышение симпатического тонуса в большей степени выражено при лечении дигидропиридиновыми БКК, особенно нифедипином. Недигидропиридиновые БКК, напротив, замедляют ЧСС. Они также вызывают снижение сократимости миокарда (отрицательный инотропный эффект) и замедление проводимости сердца.
Расширяя периферические сосуды, БКК могут увеличить венозный возврат и сердечный выброс, т.е. увеличивать преднагрузку. Этот эффект необходимо учитывать у больных АГ, у которых имеется гипертрофия миокарда и диастолическая дисфункция ЛЖ. Показано, что БКК не улучшают диастолическую функцию. Однако их влияние на скорость расслабления ЛЖ сложное. Расслабление желудочков регулируется на разных уровнях, поэтому даже один и тот же препарат может влиять на него по–разному [2]. Например, у больных АГ и ИБС наполнение и опорожнение ЛЖ могут улучшаться за счет уменьшения зон дискинезии вследствие антиишемического действия и снижения постнагрузки, как это наблюдается при лечении дигидропиридинами длительного действия (амлодипин (Нормодипин), фелодипин и др.). Так, показано, что никардипин способен уменьшать степень диастолической дисфункции [9], и данное свойство может быть присуще другим дигидропиридинам, которые сходны с ним по гемодинамическому эффекту.
Влияние на сердечно–сосудистые осложнения
По данным нескольких крупных сравнительных исследований с применением недигидропиридинов – верапамила и дилтиазема (INVEST, NORDIL, CONVINCE, VHAS) с общим числом 51473 пациента и в трех сравнительных исследованиях с применением дигидропиридинов длительного действия, а именно, нифедипина ГИТС, амлодипина, фелодипина и исрадипина (STOP–2, ALLHAT, INSIGHT) с общим числом пациентов 37238, было показано, что БКК в сравнении с другими антигипертензивными препаратами основных классов (диуретики, иАПФ и b–адреноблокаторы), приблизительно в одинаковой степени снижали АД и частоту возникновения «больших сердечно–сосудистых осложнений» (ССО), включая ИМ, мозговой инсульт (МИ) и смерть от сердечно–сосудистых причин [10].
Профиль воздействия амлодипина на сердечно–сосудистую систему сравнительно с БКК первого поколения имеет существенные отличия (табл. 1).
Установлено, что дигидропиридины длительного действия снижают смертность от сердечно–сосудистых заболеваний у пожилых больных [11]. В шведском исследовании STOP (Swedish Trial in Old Patients with Hypertension), в котором участвовало 6614 пациентов, было продемонстрировано, что лечение фелодипином или исрадипином по эффективности и влиянию на смертность не отличалось от схемы лечения, включавшей диуретик и/или b–блокатор, либо ингибитор АПФ (эналаприл или лизиноприл). Однако в группе БКК риск развития ИМ и СН был выше, чем у больных, принимавших иАПФ [12]. В свою очередь, в исследовании THOM (1993 г.) у непожилых больных АГ (средний возраст 55 лет) была продемонстрирована хорошая переносимость и безопасность длительного (средний период наблюдения 4,4 года) лечения амлодипином.
В крупном исследовании INVEST на 22576 больных, страдающих АГ и ИБС, сравнивалось лечение верапамилом и атенололом. Результаты исследования показали, что лечение верапамилом SR также эффективно уменьшает смертность и риск ССО, как и атенолол. Однако при оценке суррогатных клинических точек в группе верапамила отмечалось более выраженное снижение частоты приступов стенокардии и достоверно реже регистрировались новые случаи сахарного диабета [7].
Как известно, применение БКК короткого действия при ИМ увеличивает смертность. Кроме того, как показали В.М. Psaty и соавт. (1995), применение дигидропиридинов короткого действия увеличивает риск развития ИМ у больных АГ по сравнению с терапией диуретиками и b–блокаторами. С другой стороны, по данным другого исследования дилтиазем и верапамил могут снижать риск повторного инфаркта у больных с впервые возникшим ИМ без зубцов Q, которым противопоказаны b–блокаторы [Ryan и соавт., 1999]. В настоящее время признано, что БКК не улучшают общую выживаемость после ИМ [2]. Вместе с тем признается, что нужны дальнейшие исследования с новыми длительнодействующими БКК.
На основании приведенных данных можно сделать вывод, что у больных АГ и ИБС стабильного течения применение длительно действующих БКК уступает по своему влиянию на ССО ингибиторам АПФ, но в определенной части случаев, в особенности, если учитывать их адекватный антигипертензивный и антиангинальный эффекты, а также метаболическую нейтральность, может иметь преимущество перед препаратами других групп.
Влияние на толерантность
к физической нагрузке
При АГ наблюдается снижение физической работоспособности. Это очень важный вопрос, поскольку переносимость физической нагрузки существенно влияет на самочувствие больных АГ, их активность в повседневной деятельности и качество жизни.
Улучшение переносимости физической нагрузки на фоне применения БКК в основном связывают с положительными гемодинамическими эффектами. При однократном приеме и в условиях длительного лечения препаратами этой группы отмечаются следующие эффекты: относительное уменьшение ЧСС, систолического АД, ДП и сосудистого периферического сопротивления. Снижение темпа прироста показателей нагрузки сердечно–сосудистой системы и потребности в кислороде при физической работе обеспечивает увеличение толерантности к ней. В свое время, в частности, на примере лечения больных АГ нифедипином и верапамилом это убедительно продемонстрировал Lund–Johansen в 1987 г. [13]. Подобные результаты при изучении эффективности БКК были получены в работах многих других авторов. Так, существенное увеличение времени нагрузки до достижения субмаксимальной ЧСС при пробе с физической нагрузкой отмечено на фоне как однократного, так и длительного приема риодипина, нифедипина, верапамила и дилтиазема [3].
БКК уменьшают ДП при данной физической нагрузке, хотя ДП при максимальной нагрузке не меняется. Это говорит о том, что при стабильной стенокардии они главным образом снижают потребность миокарда в кислороде, а не повышают коронарный кровоток. Именно этим объясняется их антиишемический эффект. Многочисленные плацебо–контролируемые исследования показали, что БКК снижают частоту приступов стенокардии и уменьшают депрессию сегмента ST при физической нагрузке [2].
Влияние на гипертрофию
левого желудочка
Гипертрофия миокарда является независимым фактором риска при АГ. Поэтому способность антигипертензивного препарата при длительном применении уменьшать гипертрофию левого желудочка (ГЛЖ) – важный признак его эффективности. Наблюдающаяся регрессия ГЛЖ при лечении БКК, как полагают, объясняется не только вазодилатацией, но и влиянием на процессы «ремоделирования» в тканях. Так, по экспериментальным данным при длительном применении БКК уменьшалась выраженность гипертрофии миокарда и средней оболочки артерий. При применении нифедипина регрессия ГЛЖ сопровождается снижением содержания коллагена в миокарде [14]. Доказано, что регрессия гипертрофии левого желудочка наблюдается при длительном лечении БКК и, в частности, амлодипином [15]. J.D. Neaton и соавт. (1999), по результатам исследования THOM, показали, что на фоне продолжительного лечения больных с мягкой АГ амлодипин уменьшал ГЛЖ в такой же степени, как при лечении b–адреноблокатором (ацебутолол), b–адреноблокатором (доксазозин) и ингибитором АПФ (эналаприл). Обзор всех проведенных исследований показал, что БКК вызывают обратное развитие ГЛЖ в большей степени, чем диуретики, но в меньшей степени, чем ингибиторы АПФ и метилдофа [16].
Влияние на эндотелиальную
функцию, структуру сосудов
и микроциркуляторное русло при АГ
При АГ, как одно из звеньев патогенеза, развивается ремоделирование сосудов с изменением их структуры, механических свойств и местной регуляторной (эндотелиальной) функции. Наблюдается также перестройка микрососудистого русла с уменьшением числа или плотности капилляров. Поражение органов–мишеней при АГ во многом обусловлено именно этими процессами. Предупреждение или замедление их в определенной степени должно влиять на клиническое течение болезни и прогноз. БКК в этом отношении демонстрируют положительные качества. По результатам исследований VHAS [17] и INSIGHT [18], верапамил длительного действия и нифедипин, соответственно, превосходили диуретики по скорости замедления увеличения толщины интима–медиа сонных артерий при том, что не отличались от них по антигипертензивной активности и влиянию на ССО. БКК благотворно влияют на микроциркуляторное русло при АГ, уменьшая величину отношения «толщина стенки/ диаметр просвета» и увеличивая плотность капилляров, препятствуя таким образом ремоделированию сосудов. Применение дигидропиридиновых БКК у больных АГ сопровождается значительным снижением жесткости сосудистой стенки [19, 20]. Кроме того, дигидропиридины длительного действия (в частности, амлодипин) улучшают эндотелий–зависимую вазодилатацию за счет увеличения выработки NO [21, 22, 23].
Влияние на функцию почек
Ценными свойствами БКК являются диуретический и натрийуретический эффекты, которые связаны с увеличением почечного плазмотока и непосредственным воздействием препаратов на канальцевую экскрецию натрия [1]. Микроальбуминурия (МАУ) расценивается, как один из ранних неблагоприятных прогностических признаков и факторов риска поражения органов–мишеней при АГ и сахарном диабете. Снижение АД до целевых уровней и уменьшение МАУ, если таковая имеется, следует, по–видимому, считать одними из главных промежуточных критериев эффективности антигипертензивной терапии и профилактики почечной недостаточности.
По результатам разных исследований антигипертензивное лечение дигидропиридиновыми БКК (нифедипин, фелодипин, амлодипин) у больных мягкой и умеренной АГ сопровождалось достоверным снижением МАУ, сравнимым с аналогичным эффектом при лечении иАПФ и b–блокаторами. По другим данным, амлодипин не проявлял данного свойства в сравнении с иАПФ [24]. Ингибиторы АПФ и блокаторы рецепторов АТ1 более эффективно снижают МАУ [25] и являются препаратами первого ряда при АГ и нарушении функции почек [26]. Однако в таких случаях (при наличии признаков поражения органов–мишеней) всегда применяется комбинированная антигипертензивная терапия. По мнению Е.И. Чазовой (2001 г.) наиболее заметным ренопротективным эффектом обладают комбинации иАПФ и недигидропиридиновых анатагонистов кальция. При этом, как показали E. Kushnir и соавт. (1996 г.), G. Bakris и соавт. (1998 г.) снижение экскреция альбумина было более существенным при их комбинации, в частности с верапамилом, нежели при раздельном применении.
С клинической точки зрения полезно обратить внимание на то, что применение БКК позволяет избежать назначения мочегонных препаратов, которые оказывают неблагоприятное воздействие на липидный спектр плазмы крови, показатели электролитного и углеводного обмена. Вместе с тем они не влияют на экскрецию калия, что позволяет их комбинировать с иАПФ.
Применение
Общим показанием для назначения БКК является стойкая АГ обусловленная повышением ОПСС (табл. 2) [2]. По Российским рекомендациям (второй пересмотр) комитета экспертов ВНОК (2004) [26] показания для применения БКК при АГ выглядят следующим образом:
• БКК дигидропиридиновые длительного действия: ИСАГ, АГ у пожилых больных, стенокардия, атеросклероз периферических артерий, атеросклероз сонных артерий, беременность.
• БКК недигидропиридиновые (верапамил, дилтиазем): стенокардия, атеросклероз сонных артерий, суправетрикулярная тахикардия.
По другим источникам особыми показаниями для назначения БКК при АГ являются также мерцательная аритмия, мигрень и АГ, индуцированнная циклоспорином.
Побочные эффекты и переносимость при длительной терапии
Побочные эффекты при применении БКК достаточно подробно описаны в соответствующих руководствах. Хотелось бы обратить внимание лишь на некоторые аспекты этой темы. Побочные эффекты чаще встречаются при применении короткодействующих БКК первого поколения и при использовании препаратов в больших дозах. Дигидропиридины короткого действия, особенно нифедипин, часто вызывают побочные эффекты. Полагают, что это связано с резким расширением сосудов (головная боль, приливы, отеки лодыжек) и последующим рефлекторным повышением симпатического тонуса (тахикардия) [2,27]. При приеме нифедипина побочные эффекты наблюдаются в 10% случаев, и реже бывают при лечении длительнодействующими дигидропиридинами (амлодипин, фелодипин). Для недигидропиридинов (верапамил) из побочных эффектов чаще наблюдаются запоры, брадикардия и нарушения проводимости.
В настоящее время для постоянной терапии при АГ рекомендуются длительно действующие БКК (амлодипин (Нормодипин), фелодипин, верапамил SR и др.). С другой стороны, увеличение дозы любого антигипертензивного препарата при монотерапии выше средней терапевтической дозы не считается целесообразным, и в таких случаях показана комбинированная терапия. Длительнодействующие БКК второго поколения в указанной дозировке переносятся, как правило, хорошо. В частности, амлодипин в меньшей степени вызывает побочные реакции, например, рефлекторную тахикардию. Как считают, это связано с большим Т1/2 амлодипина и относительно постоянной его сывороточной концентрацией [2]. Хорошая переносимость и безопасность терапии амлодипином была продемонстрирована в исследовании TНOM (1993), в котором применялись также препараты других групп: ацебутолол, доксазозин и эналаприл.
По данным упоминавшегося выше исследования ALLHAT, через 5 лет от начала исследования осталось 80,4% больных, изначально получавших амлодипин, 80,5% – хлорталидон и 72,6% – лизиноприл. При этом побочные симптомы в группах отмечались приблизительно в равной степени (16,4 – 15 – 18,1% соответственно). Однако среди основных причин несоблюдения схемы I этапа (монотерапия основным препаратом) по своим отличиям выделяются: повышение АД (3,5 – 4,5 – 9%), чрезмерное снижение АД (1,4 – 3,8 – 2,3%) и ухудшение лабораторных показателей (1,6 – 3,8 – 2,3%). В группе хлорталидона достоверно чаще, чем в группе амлодипина, была зафиксирована гипокалиемия (8,5% против 1,9%). По влиянию на все биохимические показатели (уровень холестерина, гликемический профиль, калиемия) хлорталидон оказался хуже лизиноприла, в то время как амлодипин был с ним вполне сравним [8]. По этим результатам складывается впечатление, что при равной безопасности приведенных схем лечения в целом амлодипин является стабильным по влиянию на гемодинамику и метаболически нейтральным препаратом.
Комбинированная терапия БКК
В клинической практике врачи чаще сталкиваются со случаями, когда необходимо применение комбинированной терапии. Отчасти это связано с относительно поздней обращаемостью больных АГ к врачу, когда уже имеются стабильное повышение АД, а также симптомы поражения органов–мишеней. С другой стороны, монотерапия не всегда позволяет добиться эффективного снижения АД.
Комбинированная антигипертензивная терапия (АГТ) показана при умеренной и тяжелой АГ, а также при мягкой АГ, если имеются факторы риска, ухудшающие ее прогноз. При назначении терапии необходимо рассчитывать не только на выраженный антигипертензивный эффект, но и снижение риска ССО. Выбор препаратов при этом зависит также от их взаимного влияния на факторы риска и возможности подавления побочных эффектов, наблюдающихся при монотерапии. Эффективность БКК возрастает при одновременном приеме иАПФ, метилдофы или b–адреноблокаторов. Для сочетания с b–блокатором используют БКК с преимущественно избирательным действием на сосуды (амлодипин, исрадипин, никардипин). Диуретики тоже могут повышать эффективность БКК, но данных об этом пока недостаточно [2].
Эффективные комбинации
• БКК + иАПФ. Полезные свойства: усиление гипотензивного эффекта, метаболическая нейтральность, подавление активации ренин–ангиотензиновой и симпатоадреналовой систем. Комбинация эффективна при тяжелой, как высоко– так и низкорениновой АГ.
• БКК (дигидропиридиновые) + b–блокаторы. Полезные свойства: b–блокаторы препятствуют развитию выраженных сосудистых эффектов и рефлекторной тахикардии (БКК), которая, с одной стороны, снижает гипотензивный эффект, а с другой – увеличивает потребность миокарда в кислороде. БКК нивелируют негативное действие b–блокаторов на обмен липидов и глюкозы, а также на периферическое сопротивление сосудов. Данная комбинация эффективна при АГ в сочетании с ИБС, а также при АГ, рефрактерной к монотерапии.
• БКК (дигидропиридины) + АИР (агонисты имидазолиновых рецепторов). Полезные свойства: предупреждение повышения симпатического тонуса, метаболическая нейтральность, и те и другие препараты не замедляют скорость психических реакций. Применение данной комбинации может оказаться полезным у больных АГ с метаболическим синдромом и для водителей автотранспорта.
• БКК + диуретики. Указывается, что в сочетании амлодипин + гидрохлортиазид отмечается аддитивный гипотензивный эффект [14]. Сочетание БКК с диуретиками относят как к эффективным [26], так и к нерациональным комбинациям [14,28]. Нерациональной считается комбинация нифедипина короткого действия с диуретиком.
Заключение
Подводя итог, в целом можно заключить, что БКК эффективно снижают АД. При этом их антигипертензивная активность сравнима с таковой препаратов других основных групп, применяющихся для лечения АГ. При длительном применении у больных АГ они уменьшают ГЛЖ, препятствуют процессам ремоделирования сосудов и микрососудистого русла, а также положительно влияют на функцию эндотелия. БКК проявляют диуретический и натрийуретический эффекты, не влияя при этом на экскрецию калия, и уменьшают микроальбуминурию. Препараты этой группы не влияют на липидный обмен и гликемический профиль. БКК длительного действия снижают смертность и риск сердечно–сосудистых осложнений, а также частоту приступов стенокардии у больных АГ и ИБС стабильного течения. Они повышают толерантность к физической нагрузке за счет снижения энергозатрат и потребности миокарда в кислороде.
Сравнимое с препаратами других групп небольшое количество побочных эффектов и хорошая переносимость при длительной терапии отличает длительнодействующие БКК, в особенности второго поколения, такие как амлодипин. Их преимущества (гемодинамический профиль, метаболическая нейтральность и др.) становятся очевидными при назначении комбинированной терапии. Пожалуй, единственным абсолютным противопоказанием для назначения БКК является выраженная СН. Однако применение амлодипина (в комбинации с иАПФ, диуретиками и b–блокаторами) при СН считается оправданным.
Литературы
1. Андреев Н.А., Моисеев В.С. Антагонисты кальция в клинической медицине. М. ФАРМЕДИНФО,1995; 161 с.
2. Гилман А.Г. Клиническая фармакология по Гудману и Гилману. М. Практика 2006; 1648 стр.
3. Андреева Т.Н. Исследование возможностей лечения больных гипертонической болезнью посредством форидона, нифедипина, верапамила и дилтиазема. Автореф. дис. канд. мед. наук; Минск, 1989; 27 с.
4. Midtbo K, Heds O, Von der Meer. Verapamile compared in the treatment of essential hypertension. J. Cardiovasc. Pharmacol., 1982; 4, Suppl.3: S363–S368.
5. Muiesan G, Agabiti–Rosei E, Castellano M, et al. Antihypertensive and humoral effects of verapamile and nifedipine in essential hypertension. J. Cardiovasc. Pharmacol., 1982; 4, N3: 325–329.
6. Inouye IK, Massie BM, Benowitz N, Simpson P, and Loge D. Antihypertensive therapy with diltiazem and comparison with hydrochlorothiazide. Am. J. Cardiol., 1984, 53: 1588–1592.
7. Pepine CJ, Handberg EM, Rhonda M. Cooper, et al. A Calcium Antagonist vs a Non–Calcium Antagonist Hypertension Treatment Strategy for Patients With Coronary Artery Disease The International Verepamil SR/Trandolapril Study (INVEST): A Randomized Controlled Trial. JAMA December 3, 2003; 21 (Vol 290): 2805–61.
8. Mayor Outcomes in High–Risk Hypertensive Patients Randomized to Angiotensin–Converting Enzyme Inhibitor or Calcium Channel Blocer vs Diuretic. The Antihypertensive and Lipid–Lowering Treatment to Prevent Heart Attack Trial (ALLHAT). JAMA 2002; 288: 2981–97.
9. Hanet C, Rousseau MF, van Eyll C, and Pouleur H. Effects of nicardipine on regional diastolic left ventricular function in patients with angina pectoris. Circulation, 1990; 81: III48–III54.
10. Чазов Е.И., Чазова И.Е. (под ред.). Руководство по артериальной гипертонии. Медиа Медика 2005; 734 стр.
11. Staessen JA, Fagard R, Thijs L, Celis H, et al. Randomized double–blind comparison of placebo and active treatment for older patients with isolated systolic hypertension. The Systolic Hypertension in Europe (Syst–Eur) Trial Investigators. Lancet, 1997, 350: 757–764.
12. Hansson L, Lindholm L,EkbomT, et al. randomized trial of old and new antihypertensive drugs in elderly patients: cardiovascular morbidity and mortality. The Swedish Trial in Old Patients with Hypertension–II Study. Lancet 1999; 354: 1751–6.
13. Lund–Johansen P. Exercise and antihypertensive therapy. Am. J. Cardiol. 1987; 59: 98a–107a.
14. Метелица В.И. Справочник по клинической фармакологии сердечно–сосудистых лекарственных средств. М. Медпрактика, 1996; 778 с.
15. Nayler W. G. Calcium antagonists. London: Academic press, 1988; 347 p.
16. Dalhof B, Pennert K end Hansson L. Reversal of left ventricular hypertrophy in hypertensive patients. A metaanalysis of 109 treatment studies. Am. J. Hypertens., 1992, 5: 95–110
17. Zancetti A, Rosei EA, Palu CD, et al. The Verapamil in Hypertension and Atherosclerosis Study (VHAS): Results of long–term randomized treatment with either verapamil or chlorthalidone on carotid intima–media thickness. J Hypertens 1998; 16: 1667–76.
18. Brown MJ, Palmer CR, Castaigne A, et al. Morbidity and mortality in patients randomized to double–blind treatment with a long–acting calcium–blocker or diuretic in the international Niferdipine GITS Study: Intervention as a Goal in Hypertension Treatment (INSIGHT). Lancet 2000; 356: 366–72.
19. Dusseau J, Hutchins PM. Calcium entry blokers stimulate vasoproliferation on the chick chorioallantoic membrane. Int J Microcirc Clin Exp 1993; 13: 219–31.
20. Rakusan K, Cicutti N, Kazda S, et al. Effekt of nifedipine on coronary capillary geometry in normotensive and hypertensive rats. Hypertension 1994; 24: 205–11.
21. Muiesan L, Salvetti M, Monteduro C. Effect of Treatment on Flow Depended Vasodilatation of the Brachial Artery in Essential Hypertension. 1999; 33: 575–80.
22. Schiffrin B, Pu Q, Park JB. Effect of amlodiopine compared to atenolol on small arteries of previously untreated essential hypertensive patients. Am. J. Hypertens. 2002; 15(2 Pt 1): 105–110.
23. Zhang X, Kichuk MR, Mital S, Michler R, et al. Amlodipine promotes kinin–mediated nitric oxide production in coronary vicrovessels of falling human hearts. Am. J. Cardiol. 1999; 84: 27L–33L.
24. Agodoa LY, Appel L, Bakris GL, et al. Effect of ramipril vs amlodipine on renal outcomes in hypertensive nephrosclerosis: a randomized controlled treal. JAMA 2001; 285: 2719–28.
25. Ruggeneti P, Schieppati A, Remuzzi G. Progression, remission, regression of chronic renal diseases. Lancet 2001; 357: 1601–8.
26. Профилактика, диагностика и лечение артериальной гипертензии. Российские рекомендации (второй пересмотр). Комитет экспертов Всероссийского научного общества кардиологов. Приложение к журналу «Кардиоваскулярная терапия и профилактика», 2004.
27. Opie LH, Yusuf S, Kubler W. Current status of safety end efficacy of calcium channel blockers in cardiovascular disease: a critical analysis based on 100 studies. Prog. Cardiovasc. Dis., 2000; 43: 171–196.
28. Чазова И.Е. Комбинированная терапия артериальной гипертензии. Cons. Med. 2001; 2: 22–6.
Антагонисты кальция (АК, синоним – блокаторы медленных кальциевых каналов) относятся к одному из основных классов препаратов, применяющихся для лечения артериальной гипертонии (АГ). Неоднократно описанные в литературе негативные последствия применения АК первого поколения, в основном, у больных с ишемической болезнью сердца (ИБС) и сердечной недостаточностью (СН), по-видимому, до сих пор препятствуют более широкому применению в клинической практике современных АК, имеющих отличный от них фармакодинамический профиль и доказавших свою эффективность во многих исследованиях.
АК – довольно разнородная группа лекарственных средств, отличающихся друг от друга по химической структуре, фармакодинамике, клиническим и возможным побочным эффектам. Основной механизм их действия – уменьшение поступления Са++ через кальциевые L-каналы, чувствительные к АК. Строго говоря, АК не вступают в какой-либо антагонизм с ионами Са++ и не блокируют кальциевые каналы, но влияют на их модуляцию, увеличивая и/или уменьшая продолжительность разных фаз состояния (фаза 0 – закрытые каналы, N1 и N2 – открытые каналы) и изменяя таким образом кальциевый ток.
Как известно, сокращение гладкомышечных клеток (ГМК) сосудов зависит от концентрации Са++ в цитоплазме, и если подавить трансмембранный вход Са++, его количество в цитоплазме клетки и ее готовность к сокращению уменьшатся. Все АК, расслабляя гладкие мышцы артериол, снижают уровень артериального давления (АД) и общее периферическое сопротивление сосудов (ОПСС).
Из особенностей фармакокинетики АК следует отметить то, что они метаболизируются в печени и выводятся, в основном, с мочой. При заболеваниях почек фармакокинетика АК мало изменяется, тогда как при болезнях печени их период полужизни и биодоступность увеличиваются [1].
В литературе не отмечается эффект привыкания к АК. Это, по-видимому, объясняется тем, что длительное введение АК не оказывает существенного влияния на плотность и чувствительность рецепторов к ним в кальциевых каналах. При длительном применении верапамила и дилтиазема наблюдается их кумуляция. При этом время полужизни верапамила и его активного метаболита норверапамила увеличивается в два раза (до 10 ч), хотя активность последнего составляет 1/8 активности верапамила [1].
В клинической практике применяются препараты 3 подгрупп: фенилалкиламины (верапамил), дигидропиридины (нифедипин, амлодипин, исрадипин и др.) и бензодиазепины (дилтиазем). Поскольку верапамил и дилтиазем проявляют определенное сходство между собой, их часто объединяют в одну условную подгруппу «недигидропиридиновые». По одной из классификаций с учетом органоспецифичности (Singh, 1986) препараты этой объединенной группы относятся к АК I типа, которые проявляют свое действие на сердце, сосуды и проводящую систему сердца. Дигидропиридиновые препараты относятся к АК II типа с преимущественно сосудистым эффектом (всего по этой классификации различают 4 типа АК). Между препаратами этих двух подгрупп действительно имеются существенные фармакодинамические различия и, в частности, в характере влияния на сердечно-сосудистую систему (табл. 1).
Так, дигидропиридиновые АК в отличие от верапамила и дилтиазема (проявляя свою высокую сосудистую селективность) значительно снижают ОПСС, практически не влияют на проводимость сердца и очень слабо влияют на его сократительную функцию.
В подгруппе дигидропиридинов по своим улучшенным (по сравнению нифедипином) характеристикам выделяются препараты длительного действия, в частности амлодипин. Главной его особенностью с точки зрения клинического применения является длительный период полувыведения (Т1/2 равен 35–50 ч) и большая продолжительность действия (72 ч), что позволяет принимать его 1 раз в сутки и не требует создания ретардных форм. Его сывороточная концентрация и эффект нарастают в течение 5–7 дней лечения [2]. Действие амлодипина проявляется медленно, так как растворимость в жирах в 3–4 раза ниже, чем у нифедипина. Кроме того, он обладает в небольшой степени также свойствами дилтиазема, поскольку частично связывается с его рецепторами [1].
Антигипертензивная эффективность
Монотерапия АК в равной степени эффективна при I и II степени АГ [2]. Хорошая эффективность АК при лечении АГ была показана в многочисленных плацебо-контролируемых и сравнительных исследованиях. Антигипертензивный эффект АК дозозависимый [3–5]. Так, амлодипин в дозе 5–10 мг/сут у больных АГ в течение первых 4 недель снижает уровни артериального давления (АД) на 16/12,5 мм рт. ст. Нормализация или терапевтически значимое снижение уровней АД наблюдается у 61–91% пациентов.
По данным сравнительных исследований, АК снижают уровни АД по крайней мере столь же эффективно, как β-блокаторы, диуретики и ингибиторы ангиотензин-превращающего фермента (ИАПФ) [6, 7, 8]. В завершенном крупном исследовании ALLHAT (33357 больных) амлодипин продемонстрировал равную антигипертензивную активность при сравнении с хлорталидоном и лизиноприлом [8]. Разница наблюдалась лишь в том, что хлорталидон лучше снижал систолическое АД (САД), а амлодипин – диастолическое АД (ДАД). Вместе с тем профиль снижения АД в качестве результата лечения в группе амлодипина оказался более приемлемым, поскольку число случаев повышения или чрезмерного снижения уровня давления в этой группе было меньше, чем в других. Основываясь на результатах многоцентровых рандомизированных исследований, сегодня можно полагать, что ни один из основных классов антигипертензивных средств (АГС) не имеет существенного преимущества в снижении уровня АД.
Влияние на сердечно-сосудистую систему
Все АК вызывают расширение артериол и коронарных артерий. В большей степени это свойство присуще препаратам подгруппы дигидропиридинов. Характерным для них является отсутствие или слабое влияние на сократимость и проводимость (если они применяются в терапевтических дозах). Особенного внимания в этом отношении заслуживают долгодействующие препараты амлодипин и фелодипин. По гемодинамическому эффекту амлодипин близок другим дигидропиридинам – никардипину и нисольдипину, и отличается от верапамила и дилтиазема. Препарат снижает АД и ОПСС, увеличивает сердечный индекс и частоту сердечных сокращений (ЧСС). Однако при длительном применении амлодипина реакция ЧСС уменьшается. Отрицательный инотропный эффект при применении амлодипина отсутствует или менее выражен, чем у нифедипина [1]. Профиль воздействия амлодипина на сердечно-сосудистую систему в сравнении с АК первого поколения имеет существенные отличия (см. табл. 1).
Рефлекторное повышение симпатического тонуса в большей степени выражено при лечении дигидропиридиновыми АК, особенно нифедипином. Недигидропиридиновые АК, наоборот, замедляют ЧСС. Они также вызывают снижение сократимости миокарда (отрицательный инотропный эффект) и замедление проводимости сердца.
Расширяя периферические сосуды, АК могут увеличить венозный возврат и сердечный выброс, т.е. преднагрузку. Этот эффект необходимо учитывать у больных АГ, у которых имеется гипертрофия миокарда левого желудочка (ЛЖ) и его диастолическая дисфункция. Влияние АК на скорость расслабления ЛЖ сложное. Так как расслабление желудочков регулируется на разных уровнях, поэтому даже один и тот же препарат может влиять на него по-разному [2]. Например, у больных АГ и ИБС наполнение и опорожнение ЛЖ могут улучшаться за счет уменьшения зон дискинезии вследствие антиишемического действия и снижения постнагрузки, как это наблюдается при лечении амлодипином. Напротив, никардипин способен уменьшать степень диастолической дисфункции, и данное свойство может быть присуще другим дигидропиридинам, которые сходны с ним по гемодинамическому эффекту [9].
АК оказывают ангиопротекторный эффект, обусловленный торможением агрегации тромбоцитов, уменьшением адгезии моноцитов и пролиферации ГМК, инактивацией ЭТ-I. В исследованиях VHAS (верапамил), PREVENT (амлодипин), INSIGHT (нифедипин) и ELSA (лацидипин) результаты оценки толщины интима-медиа показали, что АК замедляют развитие атеросклеротического поражения сонных артерий у больных АГ. Имеются сообщения о благоприятном влиянии, в частности, амлодипина на функцию эндотелия сосудов и их структуру, то есть предотвращение их ремоделирования. Так, в результатах проспективного плацебо-контролируемого исследования PREVENT (2000) отмечалось выраженное антиатеросклеротическое действие амлодипина в сонных артериях в виде регресса толщины комплекса интима-медиа на 0,046 мм против ее утолщения на 0,011 мм в группе контроля [10]. Это важный факт, поскольку в настоящее время доказана четкая корреляция степени утолщения комплекса интима-медиа сонных артерий с частотой развития инфаркта миокарда (ИМ) и мозгового инсульта (МИ).
Атеросклеротический эффект АК – их главный плейотропный эффект. Он связан со способностью высоколипофильных (амлодипина) АК уменьшать агрегацию липопротеидов низкой плотности с мембранными липидами клеток, что лежит в основе повреждения клеток, дисфункции эндотелия и деструктивного воспаления, ассоциируемых с атеросклерозом [11]. Так, антиокислительное действие амлодипина (ингибирование пероксидации липидов) было подтверждено в экспериментальных условиях [12]. В клиническом исследовании CAMELOT у больных ИБС изучалась динамика состояния атеросклеротической бляшки в коронарных артериях [13]. Только на фоне терапии амлодипином (в отличие от эналаприла и плацебо) показано достоверное замедление роста атеромы, что в свою очередь ассоциировалось со снижением сердечно-сосудистых осложнений на 31%.
Клинические и гемодинамические эффекты вазоселективных дигидропиридинов III поколения (амлодипин, фелодипин, лерканидипин и др.), связанные с их способностью расширять коронарные артерии и периферические сосуды, позволяют успешно применять их не только при АГ и легочной гипертензии, но и стенокардии, ИМ, сердечной недостаточности, синдроме Рейно [14]. В исследовании Chahine R.A. et al. (1993) пациенты с доказанной стенокардией вазоспастического характера показывали значительное уменьшение эпизодов стенокардии, частоты дополнительного приема нитроглицерина [15]. В многоцентровом исследовании САРЕ (1994) по данным 48-часового мониторирования ЭКГ амлодипин значительно снижал частоту эпизодов депрессии сегмента ST и общее время ишемии, а также частоту болевой ишемии и прием короткодействующих нитратов.
Влияние на сердечно-сосудистые осложнения
В последние годы целый ряд крупных клинических испытаний, таких как ALLHAT, VALUE, ASCOT и ACCOMPLISH, подтвердил клиническую пользу терапии, основанной на АК, в предотвращении сердечно-сосудистых осложнений и снижении сердечно-сосудистой смертности.
По данным нескольких крупных сравнительных исследований с применением недигидропиридинов – верапамила и дилтиазема (INVEST, NORDIL, CONVINCE, VHAS, n = 51473) и трех сравнительных исследований с применением дигидропиридинов длительного действия – нифедипина ГИТС, амлодипина, фелодипина и исрадипина (STOP-2, ALLHAT, INSIGHT, n = 37238) было показано, что АК в сравнении с другими АГС (диуретики, ИАПФ и β-блокаторы) приблизительно в одинаковой степени снижали уровень АД и частоту возникновения «больших сердечно-сосудистых осложнений», включая ИМ, МИ и смерть от сердечно-сосудистых причин [16].
В другом метаанализе (64 рандомизированных клинических исследования, 9417 клинических событий), сравнивающем эффект монотерапии с плацебо или контролем, также подтвердилась статистически значимая сопоставимость пяти основных классов АГС как в отношении предупреждения коронарных событий (тиазидный диуретик – 14%, β-блокаторы – 11%, ИАПФ – 17%, АК – 15%), так и в отношении предотвращения МИ (38%, 17%, 22%, 34% соответственно). В то же время у АК отмечался дополнительный эффект в отношении предупреждения развития МИ.
При анализе рандомизированных клинических исследований оказалось, что снижение САД на 10 мм рт. ст. или ДАД на 5 мм рт. ст. сопровождается сходной клинической эффективностью различных АГС, а именно на 22% (17–27%) снижается риск коронарных событий и на 41% (33–48%) риск инсульта. Полученные данные свидетельствуют о том, что профилактическая польза АГС обусловлена прежде всего их гипотензивным эффектом как таковым.
Использование любых АК при остром ИМ и наличии признаков СН считается противопоказанным. Также они противопоказаны и при хронической СН (ХСН). Однако в исследовании PRAISE выявлено, что добавление амлодипина к терапии больных с выраженной ХСН оказывало дополнительное положительное влияние на показатели смертности. В этом отношении амлодипин выгодно отличается от других известных АК.
Установлено, что дигидропиридины длительного действия снижают смертность от сердечно-сосудистых заболеваний (ССЗ) у пожилых больных [17]. В шведском исследовании STOP (Swedish Trial in Old Patients with Hypertension), в котором участвовало 6614 пациентов, было продемонстрировано, что лечение фелодипином или исрадипином по эффективности и влиянию на смертность не отличалось от схемы лечения, включавшей диуретик и/или β-блокатор, либо ИАПФ (эналаприл или лизиноприл). Однако в группе АК риск развития ИМ и СН был выше, чем у больных, принимавших ИАПФ [18]. В свою очередь, в исследовании THOM (1993) у не пожилых больных АГ (средний возраст 55 лет) была продемонстрирована хорошая переносимость и безопасность длительного (средний период наблюдения 4,4 года) лечения амлодипином.
В упоминавшемся выше исследовании PREVENT оценивалось влияние амлодипина на прогноз больных ИБС. У больных, получавших амлодипин, наблюдалось уменьшение числа госпитализаций вследствие прогрессирования или дестабилизации течения стенокардии и СН, операций реваскуляризации миокарда.
Как известно, применение АК короткого действия при ИМ увеличивает смертность. Кроме того, как показали В.М. Psaty и соавт. (1995), применение дигидропиридинов короткого действия увеличивает риск развития ИМ у больных АГ по сравнению с терапией диуретиками и β-блокаторами. В то же время, по данным другого исследования дилтиазем и верапамил могут снижать риск повторного ИМ у больных с впервые возникшим ИМ без зубцов Q, которым противопоказаны β-блокаторы (Ryan и соавт., 1999). В настоящее время признано, что АК не улучшают общую выживаемость после ИМ [2]. Вместе с тем признается, что нужны дальнейшие исследования с новыми длительно действующими АК.
На основании приведенных данных можно сделать вывод, что у больных АГ и ИБС стабильного течения применение длительно действующих АК может иметь преимущество перед препаратами в определенной части случаев, если учитывать их адекватный антигипертензивный и антиангинальный эффекты, а также метаболическую нейтральность.
Хорошие результаты дает комбинированное использование препаратов АК с ИАПФ. Так, в исследовании EUROPA у пациентов с ИБС на фоне лечения комбинацией амлодипина с периндоприлом (при сравнении с общей группой, к терапии которой был добавлен только периндоприл) отмечалось более выраженное снижение частоты первичной точки (сердечно-сосудистая смертность, ИМ, остановка сердца) и других исходов ИБС, отражающее синергизм в действии данных АГС [19].
Влияние на толерантность к физической нагрузке
При АГ и ИБС наблюдается снижение физической работоспособности. Это очень важный вопрос, поскольку переносимость физической нагрузки (ФН) существенно влияет на самочувствие больных, их активность в повседневной деятельности и качество жизни. Улучшение переносимости ФН на фоне применения АК, в основном, связывают с положительными гемодинамическими эффектами. При однократном приеме и в условиях длительного лечения препаратами данной группы отмечаются следующие эффекты: относительное уменьшение ЧСС, САД, двойного произведения (ДП) и ОПСС. Снижение темпа прироста показателей нагрузки сердечно-сосудистой системы и потребности в кислороде при физической работе обеспечивает увеличение толерантности к ней. В свое время, в частности, на примере лечения больных АГ нифедипином и верапамилом это убедительно продемонстрировал Lund-Johansen в 1987 г. [20]. Подобные результаты при изучении эффективности АК были получены в работах многих других авторов. Так, существенное увеличение времени нагрузки до достижения субмаксимальной ЧСС при пробе с ФН отмечено на фоне как однократного, так и длительного приема форидона, нифедипина, верапамила и дилтиазема [3].
Многочисленные плацебо-контролируемые исследования показали, что АК снижают частоту приступов стенокардии и уменьшают депрессию сегмента ST при ФН [2]. В исследовании J.A. Van Der Vring et al. (1999) при добавлении АК, в том числе амлодипина, к β-блокаторам значительно задерживалось появление ишемической депрессии сегмента ST во время пробы с ФН.
АК уменьшают ДП при ФН, хотя на пике нагрузки оно не меняется. Это говорит о том, что при стабильной стенокардии АК, главным образом, снижают потребность миокарда в кислороде, а не повышают коронарный кровоток. Именно этим объясняется их антиишемический эффект. Выгодным отличием амлодипина при ФН от более ранних АК считается отсутствие у него влияния на ЧСС, увеличение которого является одним из пусковых механизмов ишемии.
Влияние на гипертрофию левого желудочка
Гипертрофия левого желудочка (ГЛЖ) является независимым фактором риска при АГ. Поэтому способность АГС при длительном применении уменьшать гипертрофию миокарда – важный критерий его эффективности. Наблюдающаяся регрессия ГЛЖ при лечении АК, как полагают, объясняется не только вазодилатацией, но и влиянием на процессы ремоделирования в тканях. Так, по экспериментальным данным при длительном применении АК уменьшалась выраженность гипертрофии миокарда и средней оболочки артерий. При применении нифедипина регрессия ГЛЖ сопровождается снижением содержания коллагена в миокарде [21]. Доказано, что регрессия ГЛЖ наблюдается при длительном лечении АК и, в частности, амлодипином [22].
J.D. Neaton и соавт. (1999) по результатам исследования THOM показали, что на фоне продолжительного лечения больных с мягкой АГ амлодипин уменьшал ГЛЖ в такой же степени, как при лечении β-адреноблокатором (ацебутолол), ά-адреноблокатором (доксазозин) и ИАПФ (эналаприл). Обзор всех проведенных исследований показал, что АК вызывают обратное развитие ГЛЖ в большей степени, чем диуретики, но в меньшей степени, чем ИАПФ [23].
Влияние на стенку сосуда
При АГ как одно из звеньев патогенеза развивается ремоделирование сосудов с изменением их структуры, механических свойств и местной регуляторной (эндотелиальной) функции. Наблюдается также перестройка микрососудистого русла с уменьшением числа или плотности капилляров. Поражение органов-мишеней при АГ во многом обусловлено именно этими процессами. Предупреждение или замедление их в определенной степени должно влиять на клиническое течение болезни и прогноз. АК в этом отношении демонстрируют положительные качества.
По результатам исследований VHAS [24] и INSIGHT [25], верапамил длительного действия (Верапамил SR) и нифедипин, соответственно, превосходили диуретики по скорости замедления увеличения толщины комплекса интима-медиа сонных артерий, при том, что не отличались от них своей антигипертензивной активности и влиянием на сердечно-сосудистые осложнения.
АК благотворно влияют на микроциркуляторное русло при АГ, уменьшая величину отношения «толщина стенки / диаметр просвета» и увеличивая плотность капилляров, препятствуя, таким образом, ремоделированию сосудов. Применение дигидропиридиновых АК у больных АГ сопровождается значительным снижением жесткости сосудистой стенки [26, 27]. Кроме того, дигидропиридины длительного действия, в частности амлодипин, улучшают эндотелийзависимую вазодилатацию за счет увеличения выработки NO [28, 29, 30].
Влияние на функцию почек
Ценными свойствами АК являются диуретический и натрийуретический эффекты, которые связаны с увеличением почечного плазмотока и непосредственным воздействием препаратов на канальцевую экскрецию натрия [1]. Микроальбуминурия (МАУ) расценивается как один из ранних неблагоприятных прогностических признаков и факторов риска поражения органов-мишеней при АГ и сахарном диабете. Снижение АД до целевых уровней и уменьшение МАУ, если таковая имеется, следует считать одними из главных промежуточных критериев эффективности АГС и профилактики почечной недостаточности.
По результатам разных исследований антигипертензивное лечение дигидропиридиновыми АК (нифедипин, фелодипин, амлодипин) у больных мягкой и умеренной АГ сопровождалось достоверным снижением МАУ, сравнимым с аналогичным эффектом при лечении ИАПФ и β-блокаторами [31]. Конечно, ИАПФ и блокаторы рецепторов АТ1 более эффективно снижают МАУ и являются препаратами первого ряда при АГ и нарушении функции почек [32, 33]. Однако в таких случаях (при наличии признаков поражения органов-мишеней) всегда применяется комбинированная антигипертензивная терапия. По мнению Е.И. Чазовой (2001), наиболее заметным ренопротективным эффектом обладают комбинации ИАПФ и АК.
С клинической точки зрения полезно обратить внимание на то, что применение АК позволяет избежать назначения мочегонных препаратов, которые оказывают неблагоприятное воздействие на липидный спектр плазмы крови, показатели электролитного и углеводного обмена.
Применение в клинической практике
Общим показанием для назначения АК является АГ, в том числе и стойкая, обусловленная повышением ОПСС [2]. По современным международным и национальным рекомендациям ВНОК преимущественными показаниями для применения АК в клинической практике являются следующие состояния:
- АК дигидропиридиновые длительного действия (например, амлодипин) – изолированная систолическая АГ (пожилые больные), ИБС, стенокардия, атеросклероз сонных и коронарных артерий, беременность;
- АК недигидропиридиновые (верапамил, дилтиазем) – ИБС, стенокардия, атеросклероз сонных артерий, суправентрикулярная тахикардия.
Побочные эффекты при применении АК известны и достаточно подробно описаны в разных руководствах. Хотелось бы обратить внимание лишь на некоторые аспекты этой темы. Побочные эффекты чаще встречаются при применении короткодействующих АК первого поколения и при использовании препаратов в больших дозах. Дигидропиридины короткого действия, особенно нифедипин, часто вызывают побочные эффекты. Полагают, что это связано с резким расширением сосудов (головная боль, приливы, отеки лодыжек) и последующим рефлекторным повышением симпатического тонуса (тахикардия) [2, 34]. При приеме нифедипина побочные эффекты наблюдаются в 10% случаев и реже бывают при лечении длительно действующими дигидропиридинами (амлодипин, фелодипин). Для недигидропиридинов (верапамил) из побочных эффектов чаще наблюдаются запоры, брадикардия и нарушения проводимости.
В настоящее время для постоянной терапии при АГ рекомендуются длительно действующие АК (амлодипин, фелодипин, Верапамил SR и др.). В то же время увеличение дозы любого антигипертензивного препарата при монотерапии выше средней терапевтической дозы не считается целесообразным, и в таких случаях показана комбинированная терапия.
Длительно действующие АК второго поколения в указанной дозировке переносятся, как правило, хорошо. В частности, амлодипин в меньшей степени вызывает побочные реакции, например, рефлекторную тахикардию. Как считают, это связано с большим Т1/2 амлодипина и относительно постоянной его сывороточной концетрацией [2]. Хорошая переносимость, стабильное влияние на гемодинамику и метаболическая нейтральность и безопасность терапии амлодипином была продемонстрирована в ряде крупных исследований.
В исследовании ASCOT-BPLA впервые установлено, что терапия, основанная на применении современных АГС – амлодипина и периндоприла, по сравнению с комбинацией β-адреноблокатора (атенолола) и тиазидного диуретика приводила не только к снижению риска развития сердечно-сосудистых осложнений, предотвращала появление новых случаев СД (на 30%), но и к статистически значимому снижению общей смертности (на 11%) [35].
Генерики амлодипина
Выгодное сочетание эффективности, безопасности и благоприятных фармакокинетических свойств обуславливают важную роль амлодипина в органопротекции и профилактической терапии ССЗ. Однако в последние годы, наряду с эффективность и безопасностью, большое значение придается фармакоэкономическим показателям. В этой связи ведущие эксперты в области рационального применения лекарственных средств рекомендуют использование качественных генерических препаратов.
Мировой опыт показывает, что гарантией терапевтической эквивалентности (одинаковой степени эффективности и безопасности) генерика оригинальному препарату являются доказательства его фармацевтической эквивалентности и биоэквивалентности, полученные в корректно проведенных исследованиях. Генерик считается биоэквивалентным оригинальному препарату в том случае, если его фармакокинетическая кривая, определенная в исследовании здоровых добровольцев, не более чем на 15–20% отличается от таковой оригинального препарата.
Таким генериком, содержащим в качестве действующего вещества амлодипин, является Амлотоп® (ЗАО «Макиз-фарма).
Его биоэквивалентность оригинальному препарату амлодипина была установлена на здоровых добровольцах в адекватном исследовании, проведенным Ю.Б. Белоусовым и соавт. (на кафедре клинической фармакологии РГМУ) (рис. 1).
Фармакокинетическое исследование выявило практически одинаковый профиль концентрации в крови Амлотопа® в сравнении с оригинальным препаратом [36]. В настоящее время в ГНИЦ профилактической медицины Минздравсоцразвития РФ завершено рандомизированное перекрестное, сравнительное исследование, в которое было включено 30 больных, страдающих АГ (I и II степени) и ожирением. Дизайн исследования представлен на рисунке 2.
Первые результаты статистического анализа свидетельствуют о том, что Амлотоп® и оригинальный препарат (Норваск®, Pfizer) практически сходны по антигипертензивному действию. Не было также отмечено статистически значимых различий в переносимости препаратов.
Заключение
АК эффективно снижают уровни АД. При этом их антигипертензивная активность сравнима с таковой препаратов других основных групп, применяющихся для лечения АГ. При длительном применении у больных АГ выявляются четкий органопротективный эффект: они уменьшают ГЛЖ, препятствуют процессам ремоделирования сосудов и микрососудистого русла, а также положительно влияют на функцию эндотелия. АК проявляют диуретический и натрийуретический эффекты, не влияя при этом на экскрецию калия, и уменьшают микроальбуминурию. Препараты этой группы не ухудшают липидный обмен и гликемический профиль. Важным достоинством этого класса антигипертензивных средств является сердечно-сосудистое профилактическое действие: снижение смертности и риска сердечно-сосудистых осложнений, хороший антиишемический и антиангинальный эффекты.
Сравнимое с препаратами других групп небольшое количество побочных эффектов и хорошая переносимость при длительной терапии отличает длительнодействующие АК, такие как амлодипин. Их преимущества (гемодинамический профиль, метаболическая нейтральность и др.) становятся очевидными при назначении комбинированной терапии. Пожалуй, единственным абсолютным противопоказанием для назначения АК является выраженная СН. Однако применение амлодипина (в комбинации с ИАПФ, диуретиками и β-блокаторами) при СН считается оправданным (исследование PRAISE) ввиду позитивного влияние на показатели смертности в комбинации с базовой терапией больных ХСН [37].
Разнообразные эффекты блокаторов кальциевых каналов — место нифедипина
Статьи
Применение препаратов нифедипина и бета-блокаторов в кардиологической практике
Сборник докладов симпозиума
IКонгресс Ассоциации Кардиологов СНГ
К. В. Р. Редди
Отделение кардиологии, Лаборатория катетеризации сердца, Методистский госпиталь, Нью Йорк, США
Введение
Антагонисты кальция широко применяются в качестве антигипертензивных средств. Особенно большую популярность они приобрели в последнее десятилетие. Эти препараты привлекают внимание по многим причинам, прежде всего благодаря выраженной антигипертензивной активности, отсутствию действия на обменные процессы и благоприятному профилю побочных эффектов. Антагонисты кальция считаются идеальными средствами в тех случаях, когда единственной целью антигипертензивной терапии является контроль артериального давления. В большинстве случаев, когда следует избегать применения быстро высвобождающихся соединений (препаратов короткого действия), длительно действующие антагонисты кальция служат важными антигипертензивными средствами, причем показания к их применению можно расширить, включив в них сосудистый спазм, диастолическую дисфункцию, некоторые формы аритмии и ишемической болезни сердца, профилактику аигиопатий, идиопатическую легочную гипертензию, а также болезнь Рейно и другую не кардиологическую патологию.
Кроме того, в последних исследованиях уделяется большое внимание возможному защитному действию антагонистов кальция на такие органы-мишени, как сердце и почки, что может привести к еще большему расширению сферы их применения (1,2).
В данной статье рассматриваются разнообразные эффекты, показания к применению и использование антагонистов кальция при сердечно-сосудистых и иных заболеваниях. Обсуждаются также противоречивые мнения относительно целесообразности использования антагонистов кальция в целом и нифедипина в частности; пересматривается положение последнего в системе терапии.
Антагонисты кальция представляют собой весьма неоднородную группу лекарственных средств. Они отличаются по химической структуре, клиническому действию, терапевтической эффективности, фармакологическому профилю при сердечно-сосудистых заболеваниях, характеру побочного действия и противопоказаниям к применению (табл. 1-4). С функциональной точки зрения три типа блокаторов кальциевых каналов можно разделить на две группы: дигидропиридиновые и недигидропиридиновые блокаторы рецепторов. Дигидропиридины (нифедипин и сходные с ним препараты) характеризуются выраженным избирательным действием на сосуды, тогда как недигидропиридиновые средства сильнее влияют на миокард и обладают уникальным ингибирующим действием на ткань синусового и атриовентрикулярного узлов.
Таблица 1.
Кардиотропные эффекты антагонистов кальция
|
Нифедипин |
Дилтмазом |
Be рапа мил |
|
|
Коронарные сосуды |
|||
|
Тонус |
— |
— |
— |
|
Просвет |
+++ |
++ |
++ |
|
Дилатация периферических сосудов |
+++ |
+ |
++ |
|
Частота сердечных сокращений |
++ |
— |
— |
|
Сократимость |
0/+ |
0/- |
0/- |
|
Атриовентрикулярная проводимость |
0 |
— |
— |
|
Эффективный рефрактерный период атриовентрикулярного узла |
0 |
— |
— |
+ увеличение уменьшение
0 отсутствие влияния
Таблица 2
Основные показания к применению антагонистов кальция первого поколения
|
Bepaпамил |
Нифедипин |
Дилтиазем |
|
|
Стенокардия Принцметала |
+++ |
+++ |
+++ |
|
Вариантная стенокардия |
+++ |
+++ |
+++ |
|
Пароксизмальная суправентрикулярная тахикардия |
+++ |
— |
++ |
|
Мерцательная аритмия |
++ |
— |
++ |
|
Артериальная гипертония |
+++ |
+ |
Количество
(+) означает частоту применения;
(-) не используется
Таблица 3.
Противопоказания для антагонистов кальция первого поколения
|
Дилтиазем |
Нифедипин |
Верапамил |
|
|
Аортальный стеноз |
+ |
+ |
+ |
|
Нарушения атриовентрикулярной проводимости |
+ |
— |
+ |
|
Недостаточность кровообращ ения |
+ |
+ |
+ |
|
Гипотензия |
+ |
+ |
+ |
|
Синдром слабости синусового узла |
+ |
— |
+ |
|
Синусовая брадикардия |
+ |
— |
+ |
Таблица 4
Клинические эффекты антагонистов кальция
|
Острые эффекты |
Эффекты при длительной терапии |
||||
|
ЧСС |
Сократимость |
ЧСС |
Сократимость |
Уровень катехоламинов в плазме крови |
|
|
Верапамил |
↑ |
↓↓ |
↓↓ |
↓↓ |
↔ |
|
Дилтиазем |
↑ |
↓↓ |
↓ |
↓↓ |
↔ |
|
Галлопамил |
↑ |
↓↓ |
↓ |
↓↓ |
↔ |
|
Нифедипин |
↑↑ |
↓ |
↑ |
↓ |
↑(?) |
|
Нитрендипин |
↑↑ |
↓ |
↑ |
↓ |
↑(?) |
|
Никардипин |
↑↑ |
↔ |
↑ |
↓ |
↑(?) |
|
Исрадипин |
↑↑ |
↔ |
↔ |
↔ |
↔ |
|
Фелодипин |
↑ |
↔ |
↔ |
↔ |
↔ |
|
Амлодипин |
↑ |
↔ |
↔ |
↔ |
↔ |
Относительная избирательность дигидропиридинов в отношении сосудов обусловливает их сосудистые и сосудорасширяющие побочные эффекты, такие как приливы крови, головная боль, периферические отеки и рефлекторная тахикардия. Недигидропиридиновые средства, с их преимущественным действием на ткань синусового и атриовентрикулярного узлов, значительно реже индуцируют тахикардию в ответ на расширение сосудов, зато обладают гораздо более мощным отрицательным инотропным действием на функцию левого желудочка.
Дигидропиридины второго поколения (например, амлодипин и фелодипин) являются более мощными сосудорасширяющими средствами чем аналогичные препараты первого поколения и характеризуются высокой степенью избирательного действия на сосуды. Имеющиеся в настоящее время антагонисты кальция взаимодействуют только с потенциал-зависимыми каналами клеточных мембран L-типа. Новый препарат мибефрадил избирательно ингибирует потенциал-зависимые каналы клеточных мембран Т-типа и обладает уникальным профилем фармакологической активности. Хотя по своей химической структуре мибефрадил относится к группе не-дигидропиридиновых соединений, он, подобно дигидропиридинам, обладает избирательностью в отношении сосудов, но в то же время не оказывает отрицательного инотропного действия, характерного для верапамила.
Показания к применению антагонистов кальция при сердечно-сосудистых заболеваниях
Бессимптомная ишемия
Все антагонисты кальция оказывают благотворное терапевтическое действие, устраняя эпизоды бессимптомной ишемии миокарда при амбулаторном ЭКГ-мониторировании. Некоторые исследования продемонстрировали более высокую, чем у дигидропиридинов эффективность не-дигидропиридиновых препаратов или бета-блокаторов при лечении бессимптомной ишемии (3-6). Медленно высвобождающийся нифедипин оказался более мощным средством нежели препараты короткого действия при лечении бессимптомной ишемии (7). Он в меньшей степени индуцирует про ишемические явления, опосредуемые через рефлекторную тахикардию. В исследовании ACIP было установлено, что медленно высвобождающийся нифедипин с атенололом и дилтиазем с динитратом изосорбида подавляет бессимптомную ишемию (8). Точно также, хороший эффект при бессимптомной ишемии дают мибефрадил и амлодипин (3,9).
Вазоспастическая стенокардия
Все антагонисты кальция, в том числе нифедипин, имеют важное значение в терапии нарушений вазомоторной функции коронарных сосудов, особенно при вариантной стенокардии или стенокардии Принцметала (10). Все блокаторы кальциевых каналов первого поколения обладают сходным терапевтическим действием, снижая количество ишемических приступов при вариантной стенокардии (11,12). Дигидропиридиновые антагонисты кальция оказываются эффективными у больных с хронической стабильной стенокардией, в основе которой лежат вазомоторные нарушения (депрессия сегмента ST при гипервентиляции) (13,14). Кроме того, большинство кардиологов при проведении инвазивных методик используют блокаторы кальциевых каналов для предупреждения спазма сосудов до, во время и после коронарной ангиопластики. Все более широкое применение находит внутривенное введение верапамила при манипуляциях на коронарных сосудах, в частности при ротационной атерэктомии.
Стабильная стенокардия
Все антагонисты кальция, включая нифедипин, дают хороший эффект при назначении больным с хронической стабильной стенокардией. Они не только снижают тяжесть клинической симптоматики, но и улучшают объективные показатели ишемии при тестировании на бегущей дорожке, уменьшают изменения сегмента ST при ЭКГ-мониторировании, усиливают кровоток в коронарных артериях и улучшают нарушенную вследствие ишемии функцию желудочков (15-22), а при использовании не-дигидропиридиновых препаратов снижают частоту сердечных сокращений. Для устранения ишемических симптомов редко используется монотерапия. Обычно антагонисты кальция применяют в сочетании с другими лекарственными средствами, такими как бета-блокаторы и нитраты. Сравнительная эффективность антагонистов кальция при стабильной стенокардии оценивалась в исследованиях TIBET и APSIS (23,24). В исследовании TIBET проводилось сопоставление эффективности длительно действующей формы нифедипина и атенолола при терапии в течение 6 недель. В исследовании APSIS верапамил сравнивали с метопрололом при длительности наблюдения на протяжении более 3 лет. В обоих случаях эффективность, безопасность и переносимость блокаторов кальциевых каналов и бета-блокаторов оказались одинаковыми. В исследовании TIBET не наблюдалось сколько-нибудь выраженного синергетического действия использовавшихся препаратов. Ни одно из исследований по изучению блокаторов кальциевых каналов или бета-блокаторов в лечении стабильной стенокардии, не выявило их заметного влияния на смертность больных как и на другие оценивавшиеся конечные точки наблюдения, такие как бессимптомная ишемия, также как и не определило преимуществ той или иной формы медикаментозной терапии (23).
Нестабильная стенокардия
Недавно проведенные испытания антагонистов кальция при нестабильной стенокардии дали противоречивые результаты (25). Большинство антагонистов кальция, в том числе нифедипин, дилтиазем, верапамил, амлодипин и фелодипин, оказались эффективными средствами лечения нестабильной стенокардии (25). Muller с соавторами показали, что терапия нифедипином не имеет преимуществ перед другими обычными способами лечения нестабильной стенокардии (26). В исследовании методом двойного слепого контроля с использованием плацебо, которое проводилось Gersteinblith и соавт. (27), было отмечено меньше случаев внезапной смерти, инфаркта миокарда и хирургических операций аорто-коронарного шунтирования у больных с нестабильной стенокардией, которые получали нифедипин в сочетании с бета-блокаторами и нитратами (27).
Точно также, комбинация бета-блокатора и нифедипина уменьшала вероятность инфаркта миокарда и рецидивирующей ишемии в крупномасштабном исследовании больных, поступивших в клинику с диагнозом нестабильная стенокардия (28). В то же время есть сведения, что монотерапия нифедипином повышает риск острого инфаркта миокарда (28). Еще два небольших исследования показали, что монотерапия дилтиаземом или пропранололом оказывает одинаковое действие, проявляющееся в уменьшении частоты неприятных ощущений в области грудины у больных нестабильной стенокардией (29,30). Применение сочетанной терапии (бета-блокаторы с антагонистами кальция или нитратами) оказалось вполне оправданным, так как позволяет достигнуть желаемого терапевтического результата при нестабильной стенокардии, а именно: уменьшить тяжесть клинических симптомов и предотвратить дальнейшее прогрессирование ишемии миокарда.
Инфаркт миокарда
Результаты применения антагонистов кальция после перенесенного инфаркта миокарда зависят от типа того или иного препарата, сроков его введения и типа инфаркта. Кальциевые антагонисты относительно противопоказаны при остром инфаркте миокарда, и их следует назначать только при наличии совершенно определенных показаний к применению (например, для контроля частоты сердечных сокращений при мерцательной аритмии дилтиаземом).
Muller с соавт. (31) впервые установили, что применение нифедипина в капсулах не приводит к уменьшению размера инфаркта миокарда и не спасает больных с угрозой инфаркта от его возникновения (31). У больных, получавших эту коротко действующую лекарственную форму нифедипина по поводу острого инфаркта миокарда, смертность на протяжении 2 недель была выше чем среди больных в группе плацебо (соответственно 7,5 и 2,3%), хотя смертность на протяжении 6 месяцев среди больных, получавших нифедипин (10,8%) и в контрольной группе (11,4%) была примерно одинаковой. Другие исследования (TRENT, SPRINT и Norwegian Nifedipine Multicenter Trial) также показали повышение смертности среди получавших этот препарат больных независимо от состояния функции левого желудочка (32-34).
В исследованиях MDPIT и DAVIT II лечение больных, перенесших инфаркт миокарда при отсутствии сердечной недостаточности, не-дигидропиридиновыми препаратами (дилтиазем и верапамил) позволило снизить частоту смертности и не фатальных повторных инфарктов (35,36). Правда, терапия дилтиаземом повышала число сердечных расстройств и смерти у больных с нарушенной систолической функцией левого желудочка (35). В отличие от этого, верапамил не влиял на частоту возникновения кардиальных симптомов и смертности у больных с сердечной недостаточностью (36,37).
Gibson и соавт. установили, что раннее лечение дилтиаземом в течение трех дней после инфаркта миокарда без изменения зубца Q на 51% понижало частоту ранних инфарктов и на 50% — частоту постинфарктной стенокардии (38). В другом исследовании частота смерти и повторных не фатальных инфарктов в течение года после начала терапии дилтиаземом уменьшалась на 40% (39). Более целенаправленное исследование CRIS не выявило существенных различий в уровне общей смертности и частоте повторных инфарктов между контрольной группой и группой получавшей лечение верапамилом на протяжении, двухлетнего периода наблюдения (40).
Гипертония
Многочисленные исследования показали, что блокаторы кальциевых каналов обладают анти-гипертензивной активностью и не вызывают многие побочные эффекты, которыми сопровождается действие диуретиков и бета-блокаторов. Тесная связь между гипертонией и гипертрофией желудочков, а также последствия этих расстройств (инфаркт миокарда и сердечная недостаточность) объясняют упорные попытки снизить систолическое и диастолическое давление и заставляют рассматривать если не устранение, то стабилизацию гипертрофии левого желудочка как конечную цель терапии. Все используемые в настоящее время блокаторы кальциевых каналов понижают систолическое и диастолическое давление. Кроме того, при применении на протяжении достаточно длительного периода эти препараты уменьшают массу миокарда левого желудочка (51).
Заслуживает особого упоминания метаболическая инертность этих лекарственных средств, которые не влияют на липиды и не оказывают нежелательного действия на обмен электролитов. Существующие в настоящее время разногласия относительно терапевтической ценности антагонистов кальция в качестве антигипертензивных средств касаются преларатов короткого действия.
Все длительно действующие препараты, такие как дилтиазем, нифедипин, верапамил, амлодипин, фелодипин и мибефрадил успешно применяются для снижения артериального давления (38,52). Предназначенные для однократного приема, они всегда действуют лучше других антигипертензивных средств. Как дигидропиридиновые, так и не-дигидропиридиновые соединения превосходят диуретики, ингибиторы ангиотензин-превращающего фермента и бета-блокаторы по эффективности контроля кровяного давления, низкой частоте побочных эффектов и простоте выполнения больными предписанного режима терапии (53,54). Эти свойства способствовали расширению сферы их применения: они показаны пациентам с нарушенной функцией левого желудочка и с коронарными синдромами. В последнее время высказывались противоречивые мнения о целесообразности использования антагонистов кальция для лечения гипертонии и ишемической болезни сердца, которые вылились в бурную дискуссию в печати. Проводящиеся в настоящее время исследования призваны дать ответ на вопрос о безопасности этих лекарственных средств.
Атеросклеротический процесс
Применение нифедипина, верапамила, дилтиазема и фелодипина на холестериновой модели атеросклероза у лабораторных животных сопровождалось подавлением образования атеросклеротических бляшек (41-44). В исследовании INTACT было четко показано, что у больных с легкой формой ишемической болезни сердца (ИБС), получавших нифедипин, вероятность развития новых стенозов была ниже чем при использовании нитратов или бета-блокаторов (45). В ходе двухлетнего наблюдения за больными, перенесшими пересадку сердца, было установлено, что дилтиазем предотвращает развитие ИБС (46). С другой стороны, ни один из изученных антагонистов кальция не дал ожидаемого эффекта в условиях регрессивных испытаний, отчасти потому, что эти средства не обеспечивали поддержание устойчивого артериального давления на всем протяжении суток; кроме того, все эти препараты вызывали реактивную кардиоакселерацию на фоне кажущегося «steady-state» состояния (47).
Из сказанного выше следует, что разумным объяснением повышенной частоты нежелательных эффектов в регрессивных исследованиях служит тот факт, что лекарственные средства, провоцирующие контрарегуляторные реакции с кардиоакселерацией, могут индуцировать ишемию у больных с уже имеющейся ИБС. Напротив, препараты, обеспечивающие состояние «steady-state» (например, нифедипин GITS, амлодипин или лацидипин), не вызывают проишемических реакций и поэтому могут не провоцировать нежелательных эффектов (48). Для проверки данной гипотезы были предприняты два исследования (PREVENT и ELSA), в которых больные получали амлодипин и лацидипин.
Установлено также благотворное действие блокаторов кальциевых каналов при наличии процессов рестенозирования после хирургического вмешательства на коронарных сосудах. Обобщенные данные пяти испытаний с использованием плацебо (в трех из них применялся дилтиазем, в одном нифедипин и еще в одном верапамил) свидетельствуют о благоприятной тенденции в изменении состояния больных в четырех изученных группах (в одном из трех исследований с применением дилтиазема терапевтический эффект отсутствовал) (49).
Метаанализ пяти указанных работ свидетельствует о значительном уменьшении риска рестенозирования у больных, получавших блокаторы кальциевых каналов, по сравнению с пациентами контрольной группы (49). Сходные результаты были получены еще в одном исследовании, которое проводилось с целью оценки терапевтической эффективности никардипина (50).
Нарушение диастолической функции
Поток ионов кальция через клетки миокарда может играть роль в ухудшении наполнения в фазе диастолы, изменениях чувствительности и расслаблении левого желудочка у пациентов с ишемическим синдром (55). Наибольшей эффективностью при лечении нарушений диастолической функции обладает верапамил, благодаря его отрицательному инотропному и хронотропному действию (55). Дилтиазем, по-видимому, также может давать хороший эффект. Больные с тяжелыми формами диастолической дисфункции, которая имеет место, например, при гипертрофической кардиомиопатии, реагируют на терапию верапамилом в сочетании с дизопирамидом и бета-блокаторами (56). Верапамил в значительно большей степени чем никардипин улучшает показатели диастолического наполнения левого желудочка у больных с хронической стабильной стенокардией (55). Нисолдипин не оказал какого-либо значимого влияния на параметры диастолического наполнения (55).
Нарушения систолической функции
Дигидропиридины первого поколения не оказывают видимого благотворного действия при сердечной недостаточности. С другой стороны, больным с умеренной и тяжелой формами сердечной недостаточности противопоказаны не-дигидропиридиновые препараты, а дилтиазем усугубляет состояние больных с сердечной недостаточностью после перенесенного инфаркта миокарда (35). В то же время исследование DiDi показало, что терапия дилтиазвмом на протяжении 24 месяцев не оказывала отрицательного действия на выживаемость больных, одновременно улучшала функции сердца, переносимость физических нагрузок и субъективное состояние пациентов по сравнению с больными контрольной группы (57). В настоящее время проводится оценка терапевтической эффективности и влияния на смертность блокаторов кальциевых каналов второго поколения.
Результаты исследования PRAISE свидетельствует о том, что амлодипин уменьшает частоту внезапной смерти, а также частоту летальных исходов у больных с нарушением насосной функции сердца при неишемической кардиомиопатии, но не оказывает существенного положительного или отрицательного действия у больных с ИБС (58,59). Точно также, не наблюдался сколько-нибудь заметный положительный или отрицательный эффект терапии фелодипином на течение сердечной недостаточности в исследовании VHEFT III (60). Нейрогуморальная активация при сердечной недостаточности приводила к ухудшению клинического состояния больных.
Ни фелодипин, ни амлодипин не усиливали нейрогуморальную активацию (59,60). Из числа не-дигидропиридиновых препаратов, изучавшихся в исследовании DiDi, только дилтиазем не вызывал нежелательного усиления нейрогуморальной активации в сравнении с «плацебо» группой (57). Результаты достаточно продолжительных наблюдений свидетельствуют о безопасности применения дигидропиридинов второго поколения амлодипина и фелодипина у больных с хронической сердечной недостаточностью не ишемической этиологии. Однако, до сих пор не выработаны строгие показания к применению этих лекарственных средств для сердечной недостаточности per se.
Дополнительные показания к применению антагонистов кальция
Недостаточность аортального клапана
Показано, что коротко действующие формы нифедипина уменьшают частоту или позволяют отложить операцию протезирования аортального клапана у больных с тяжелой его недостаточностью, с минимальными симптомами и хорошо сохранившейся функцией левого желудочка (61).
Первичная легочная гипертензия
Терапия вазодилататорами с целью снижения давления в легочной артерии и уменьшения резистентности легочных сосудов составляет основу лечения первичной легочной гипертензии и служит подготовительным этапом к пересадке сердца и легких. Высокие дозы нифедипина или дилтиазема значительно уменьшают тяжесть клинической симптоматики и повышают выживаемость больных. У 26% больных, реагирующих на терапию высокими дозами этих лекарственных средств, вероятность выживания на протяжении 5 лет сосоставила 95% (62,63).
Недавно было установлено, что амлодипин оказывает положительное быстрое действие на состояние легочных сосудов (64). Однако необходимо провести длительное исследование терапевтической эффективности амлодипина для получения отдаленных результатов.
Болезнь Рейно
От 30 до 90% пациентов с этим заболеванием хорошо поддаются лечению при ежедневном приеме нифедипина в дозах 30-60 мг. При первичном заболевании эта реакция выражена сильнее чем при вторичном (65-67). В дополнение к сказанному следует упомянуть, что нифедипин, дилтиазем и верапамил применяются для лечения многих других некардиологических расстройств (табл. 5 и 6).
Таблица 5
Дополнительное и возможное применение антагонистов кальция при сердечнососудистых заболеваниях
Атеросклероз
Кардиоплегия
Ишемия мозга (локальная)
Ишемия мозга (глобальная)
Застойная сердечная недостаточность
Гипертрофическая кардиомиопатия
Мигрень
Инфаркт миокарда
Болезни периферических сосудов
Легочная гипертензия
Субарахноидальное кровотечение
Таблица 6
Дополнительное и возможное применение антагонистов кальция при некардиальной патологии
|
1 |
Ахалазия |
|
2 |
Резистентные формы астмы |
|
3 |
Дисменорея |
|
4 |
Эклампсия |
|
5 |
Спазм пищевода |
|
6 |
Гиперкинезия кишечника |
|
7 |
Обструктивные заболевания легких |
|
8 |
Преждевременные роды |
|
9 |
Недержание мочи |
|
10 |
Альдостеронизм |
|
11 |
Противомалярийный препарат |
|
12 |
Химиотерапия опухолей (резистентность к препаратам) |
|
13 |
Эпилепсия |
|
14 |
Глаукома |
|
15 |
Маниакальный синдром |
|
16 |
Укачивание |
|
17 |
Повреждения спинного мозга |
|
18 |
Шум в ушах |
|
19 |
Головокружение |
Разногласия по применению антагонистов кальция — место нифедипина сегодня
Введение
Год 1996 оказался очень беспокойным в истории лечения гипертонии и ишемической болезни сердца. Он был отмечен бурными дебатами о безопасности применения антагонистов кальция, особенно препаратов дигидропиридинового ряда — нифедипина. Широко освещавшееся исследование, включавшее контрольную группу больных, показало, что терапия гипертонии коротко действующими антагонистами кальция ассоциировалась с более высоким риском инфаркта миокарда, чем при лечении диуретиками и бета-блокаторами, причем этот эффект зависел от дозы (68). В другом исследовании основное внимание было сосредоточено на клинической оценке эффективности нифедипина у больных, у которых изначально имелись симптомы острой ишемии миокарда. Метаанализ полученных результатов выявил увеличение риска летального исхода, связанное с применением коротко действующих форм нифедипина в дозах 80 мг/день или выше (69,70). Наконец, еще одно обстоятельство добавило беспокойства по поводу потенциального риска применения нифедипина короткого действия. Pahor с соавторами показали, что среди пациентов в возрасте более 70 лет с повышенным артериальным давлением, которые получали коротко действующий нифедипин, уровень смертности был выше, чем при лечении бета-блокаторами (70).
Эти результаты были тотчас же широко распространены средствами массовой информации и вызвали панику среди больных, применявших указанные препараты. Публикации не сопровождались исчерпывающим анализом поднятой в них проблемы, и непроверенные отрывочные материалы, попавшие в руки журналистов, были сделаны достоянием общественности без малейшего представления о возможных последствиях такой акции. Это достойное сожаления и породившее панику событие привело к тому, что многие больные прекратили прием предписанных им лекарств и тем самым подвергли себя опасности рецидива исходного заболевания. Из-за недостатка информации в трудном положении оказалось и медицинское сообщество. В этой ситуации .средства массовой информации действовали безответственно, без должного внимания к интересам безопасности больных людей.
Научные данные
Данные за и против применения антагонистов кальция следует обсуждать исключительно на основании их научной ценности. В связи с этим, прежде чем делать какие-либо выводы, необходимо разъяснить целый ряд вопросов.
Безопасность антагонистов кальция при лечении гипертонии
Расхождения во мнениях относительно безопасности антагонистов кальция были вполне естественны, однако вызванная ими паника не имеет под собой никаких оснований. Несмотря на высокий уровень осведомленности и значительное увеличение числа больных, получающих лечение по поводу гипертонии, только у 24% больных в Соединенных Штатах и у 37% больных в Европе удалось добиться желаемого снижения артериального давления, тогда как у большинства остальных сохраняется некомпенсированная гипертония со всеми ее последствиями (71,72). Одним из многих объяснений этому поразительному факту служит недостаточно строгое выполнение больными врачебных предписаний; теперь к этому добавился необоснованный страх перед использованием антагонистов кальция, вызванный сообщениями средств массовой информации.
В то же время, наиболее часто больные тщательно выполняют предписанный им режим применения блокаторов кальциевых каналов благодаря хорошей переносимости этих лекарственных средств и отсутствию их побочного действия (54). В одном из исследований было установлено, что на протяжении 7 лет относительная вероятность прекращения антигипертензивной терапии была максимальной у больных, которым были предписаны бета-блокаторы, и минимальной при использовании блокаторов кальциевых каналов, включая нифедипин (73). Если удастся обеспечить контроль артериального давления у большего числа больных, мы сможем более успешно бороться с заболеваемостью и смертностью, связанными с такой важной проблемой общественного здравоохранения, какой является гипертония. Это диктует необходимость совместных усилий в деле разъяснения больным с высоким артериальным давлением важности выполнения врачебных предписаний и реализации этих рекомендаций на практике.
Коротко действующие и длительно действующие нифедипины
Все вышесказанное касалось нифедипинов короткого действия и не относится к его длительно действующим формам. Известно, что разные формы одного и того же химического соединения могут обладать совершенно различными гемодинамическими и нейро-гуморальным действиями. Прием короткодействующего нифедипина сопровождается быстрым увеличением его концентрации в крови на протяжении часа, после чего она также быстро понижается. В отличие от этого, концентрация в крови длительно действующих препаратов нифедипина (GITS) нарастает медленно и достигает максимальной величины примерно через 6 часов после введения, но затем сохраняется на относительно постоянном уровне в течение 24 часов и более. Стабильная концентрация нифедипина в крови позволяет избежать активации ренин-ангиотензиновой и симпатической нервной систем (47). В исследовании, в котором сравнивался гипотензивный эффект различных способов введения препаратов для достижения эффективной концентрации в плазме крови (от болюсного до постепенного повышения), было установлено, что болюсное введение и экспоненциальная инфузия не позволяют существенно понизить артериальное давление из-за сопутствующего усиления адренергической активности и значительного увеличения частоты сердечных сокращений. С другой стороны, постепенное повышение концентрации нифедипина до такого же уровня вызывало длительное устойчивое снижение артериального давления (74).
Для изучения изменений адренергической активности Frohlich с соавторами сравнивали эффекты коротко действующего нифедипина (применявшегося трижды в день) и нифедипина системы GITS и определяли концентрацию норадреналина в плазме крови. Минимальная концентрации норадреналина в крови больных, получавших нифедипин GITS, была практически такой же, как у пациентов, получавших плацебо (75). По сравнению с ними минимальная концентрация норадреналина у больных, которым вводили коротко действующий нифедипин, была значительно выше (75).
Вполне вероятно, что благодаря нейрогуморальной стимуляции нифедипины короткого действия способствуют возникновению предполагаемых побочных эффектов и, возможно, неблагоприятному исходу. Parmley с соавт. показали, что у больных, получавших препараты GITS, частота сердечных сокращений повышалась всего на 1,6 удара в минуту (7). Постепенное начало и прекращение антигипертензивного эффекта длительно действующих дигидропиридинов является дополнительным преимуществом, так как у больных гипертонией изменчивость артериального давления, независимо от его абсолютной величины, коррелирует со степенью поражения органов-мишеней. Было показано, что их поражение зависит как от среднесуточного артериального давления, так и от амплитуды его колебаний на протяжении суток (76,77).
Блокаторы кальциевых каналов обладают минимальными побочными эффектами и не влияют на обменные процессы, поэтому они хорошо переносятся больными. Длительно действующие антагонисты кальция должны оставаться краеугольным камнем терапевтической стратегии у больных с повышенным артериальным давлением.
Из сказанного выше следует, что нифедипины короткого действия, вызывающие значительные колебания артериального давления, не всегда предотвращают поражение органов-мишеней и не снижают смертность больных. Помимо прочего, это объясняет отсутствие лимитирующего действия на развитие атеро-склеротического процесса (исследование INTACT). Одной из предполагаемых причин повышенной смертности являются про аритмические эффекты. Однако эта гипотеза остается недоказанной из-за отсутствия в литературе соответствующих научных данных.
При метаанализе, проводившемся Furberg и Psaty (69), авторы пытались объяснить повышение частоты инфарктов миокарда под воздействием нифедипина связью про ишемических эффектов с «коронарным обкрадыванием». Существует, однако, большое число данных, несовместимых с этой гипотезой. Malakoff и соавт. использовали позитронную эмиссионную томографию с ксеноном-133 и показали, что нифедипин улучшает регионарный кровоток в ишемических сегментах миокарда (78). Kygiyaum с соавт. с использованием радиоизотопного исследования сердца (таллий-201) показали, что происходит увеличение продолжительности физических нагрузок при одновременном уменьшении дефекта перфузии под влиянием нифедипина. После введения бета-блокаторов наблюдалась совершенно противоположная картина (79). В ряде других исследований также отсутствовало отрицательное воздействие нифедипина на перфузию коронарных сосудов (80,81). По мнению некоторых авторов, нифедипин улучшает нарушенную при ишемии функцию левого желудочка, что противоречит гипотезе «коронарного обкрадывания» (82).
В одном из новейших исследований больных с хронической стабильной стенокардией Parmaley и соавт. показали, что препараты нифедипина GITS уменьшали количество приступов стенокардии в течение недели, а также ишемические изменения при проведении суточного мониторирования ЭКГ (7). Указанное действие проявлялось на протяжении 48-часов при применении нифедипинов или при их сочетании с бета-блокаторами. В описанном исследовании не наблюдались про-ишемические явления. Многие другие исследования также не выявили феномена «коронарного обкрадывания» при оценке перфузии коронарных сосудов на фоне терапии нифедипином. Большинство авторов считают, что нифедипин оказывает положительное действие на перфузию коронарных сосудов у человека (83-85).
Зависимость между дозой и эффектом
Антагонистам кальция присущ дозозависимый эффект. Контролируемые исследования и метаанализ не показали достоверного увеличение риска при использовании низких доз антагонистов кальция (68,69). Риск смерти значительно повышался только при использовании нифедипинов в больших дозах в исследовании на большом количестве пациентов. Эти данные совпадают с результатами другого исследования, включавшего больных с артериальной гипертонией, которые получали тиазидовые диуретики. В этом случае их применение в высоких дозах сопровождалось увеличением риска остановки сердца в 3,5 раза по сравнению с низкими дозами (86). Очевидно, что не сам препарат, а его доза определяет риск сердечнососудистых расстройств.
Риск инфаркта миокарда
Psaty с соавторами изучали риск возникновения инфаркта миокарда (68). Наиболее важным итогом этого исследования является вывод о том, что высокие дозы антагонистов кальция повышают риск развития инфаркта миокарда. Тем не менее, такое заключение вызывает серьезные сомнения из-за явных ограничений данного исследования:
- как и всякое контролируемое исследование оно характеризовалось неоднозначностью показаний к применению нифедипина;
- применение коротко действующих форм нифедипина и дилтиазема не было одобрено Управлением по контролю медикаментов, пищевых продуктов и косметических средств (FDA) для лечения гипертонии в США;
- большинство больных принимали указанные лекарственные средства только один или два раза в день.
Риск смерти
Furberg и соавт. (69) предприняли метаанализ с целью определения риска смерти при использовании коротко действующей формы нифедипина. Результаты анализа свидетельствуют о том, что риск смерти возрастает с увеличением дозы препарата. При дозе 30-50 мг/день он составлял 1,06; при 60 мг — 1,18; а при дозе 80 мг/день достигал 2,83. Данное исследование тоже имело ряд ограничений, в связи с чем возникает ряд серьезных вопросов и сомнений:
- в анализ были включены некоторые исследования, исключавшиеся из прежних метаанализов; другие исследования, включенное в данный метаанализ, были исключены из предшествующего анализа;
- анализировались гетерогенные и несопоставимые популяции; сравнивались пациенты с разной степенью риска (исследование INTACT);
- неправильно цитировались исходные данные некоторых оригинальных исследований;
- отсутствовал анализ результатов исследований с применением высоких доз нифедипина (например, исследования Muller et a/., 31); в двух из включенных в анализ исследований оценивалась смертность больных только в течение двух недель после окончания терапии, но не включалось наблюдение на протяжении шестимесячного периода;
- даже при использовании неправильных данных метаанализ не отвечал критериям приемлемой статистической достоверности, как отмечалось авторами в предыдущем сообщении.
Заключение
Если бы в метаанализ были включены результаты наблюдений в течение 6 месяцев после рандомизации Mueller и соавт., если бы были правильно представлены использовавшиеся в этом исследовании дозы нифедипина или если бы было исключено исследование INTACT, анализ не выявил бы существенных различий риска смерти у больных, получавших высокие дозы нифедипина и пациентов контрольной группы (р = 0,13).
Новейшие данные, свидетельствующие о безопасности блока/поров кальциевых каналов:
- Шанхайское исследование по применению нифедипина у пациентов пожилого возраста показало, что медленно высвобождающийся нифедипин приводит к статистически высокодостоверному (р < 0,0001) уменьшению общего числа патологических явлений (инсульта, сердечной недостаточности, уремии, инфаркта миокарда, стенокардии, тяжелой аритмии и других серьезных заболеваний, требующих госпитализации, а также смертности по сравнению с больными, получавшими плацебо) (87).
- Braun и соавт. провели оценку относительного риска смерти среди жителей Израиля с подтвержденным диагнозом коронарной болезни, которым назначались блокаторы кальциевых каналов, в том числе нифедипины. После внесения поправки на тяжесть заболевания повышения риска смерти обнаружено не было (88).
- Aursnes и соавт. показали, что относительный риск возникновения инфаркта миокарда при использовании антагонистов кальция был значительно ниже, чем при терапии другими антигипертензивными средствами. Скорректированный относительный риск составлял 0,6 у больных, получавших антагонисты кальция; 1,66 при применении диуретиков и бета-блокаторов; 0,93 при использовании альфа-блокаторов и 0,88 у пациентов, которым назначали ингибиторы ангиотензин-превращающего фермента (89).
- Jick и соавт. определили риск возникновения инфаркта миокарда у больных с эссенциальной гипертонией равным 0,75 при лечении блокаторами кальциевых каналов и 0,5 при использовании антагонистов кальция в сочетании с диуретиками. Аналогичный показатель для больных, принимающих бета-блокаторы, по данным этих авторов составляет 1,0. Различия между приведенными величинами статистически недостоверны, однако отражают сравнительно высокую безопасность терапии блокаторами кальциевых каналов (90).
- Предварительный анализ результатов двух самых крупномасштабных испытаний антигипертензивной терапии нифедипином GITS и амлодипином свидетельствует об отсутствии случаев смерти и такой же частоте инфарктов миокарда как при использовании диуретиков и бета-блокаторов (91).
- Анализ итогов еще одного исследования (Framing-ham Heart Study), в котором продолжительность отдаленных наблюдений за 3547 пациентами с артериальной гипертонией достигала 12,7 лет, не выявил повышенного риска смерти в результате применения антагонистов кальция (92).
- Leader и соавт. проводили исследование на большой группе больных с гипертонией, которым назначали длительно действующие антигипертензивные средства, включая нифедипин. Относительный риск развития инфаркта миокарда среди больных, принимавших антагонисты кальция, по сравнению с использовавшими диуретики составлял 0,59. Это различие было статистически недостоверно из-за небольшого количества развившихся инфарктов миокарда (93). Тем не менее, оно свидетельствует о тенденции к снижению риска смерти при терапии длительно действующими антагонистами кальция.
- Если бы в анализ были включены результаты наблюдений Mueller с соавт. на протяжении 6 месяцев после рандомизации, если бы правильно цитировались использовавшиеся в этом исследовании дозы нифедипина или если бы было исключено исследование INTACT, то метаанализ Furberg и соавт. не выявил бы существенных различий риска смерти у больных, получавших высокие дозы нифедипина, и пациентов контрольной группы (р = 0,13) (94).
- В начале 1996 г. Управление по контролю медикаментов, пищевых продуктов и косметических средств (FDA) опубликовало заявление относительно безопасности блокаторов кальциевых каналов на основании обзора имеющихся данных (95). Согласно этому документу следует прекратить применение короткодействующих дигидропиридинов для лечения гипертонии. В то же время нет оснований сомневаться в безопасности длительно действующих блокаторов кальциевых каналов.
Заключение
Принимая во внимание рассмотренные в настоящем обзоре данные, а также чрезвычайно высокую эффективность антагонистов кальция при лечении повышенного артериального давления и стенокардии практикующие врачи и их пациенты могут быть уверены в безопасности применения длительно действующих форм антагонистов кальция для лечения сердечнососудистых заболеваний (96).
Литература
1. Epstein M. Calcium antagonists and renal protection: current status and future prospective. Arch Intern Med 1992; 152:1573-1584.
2. Messerli FH, McLaughlin M. Cardiac effects of calcium antagonists in hypertension, in: Epstein M, ed. Calcium antagonists in clinical medicine. Philadelphia, Hanley and Belfus 1992:137-150.
3. Braun S, van der Wall E, Emanuelsson H, Kobrin I. Effects of a new calcium antagonist, miberfadil (Ro 40-5967), on silent ischemia in patients with stable chronic angina pectoris: a multicenter placebo-controlled study. The Mibefradil International Study Group. J Am Coll Cardiol 1996; 27 (2): 317-322.
4. Subramanian VB, Bowles MJ, Khurmi NS et al. Rationale for the choice of calcium antagonists in chronic stable angina: an objective double-blind, placebo-controlled comparison of nifedipine and verapamil. Am J Cardiol 1982; 50: 1173-1179.
5. Frishman W, Chartap S, Kimmel В et al. Dilitazem, nifedipinde, and their combination in patients with stable angina pectoris: effects on angina, exercise tolerance, and the ambulatory
electrocardiographic ST-segment. Circulation 1988; 77: 774-786.
6. Deedwania PC, Carbajal EV, Nelson JR et al. Anti-ischemic effects of atenolol versus nifedipine in patients with coronary artery disease and ambulatory silent ischemia. J Am Coll Cardioi 1991; 17: 963-969.
7. Parmley WW, Nesto RW, Singh BN etal. Attenuation of trie circadian patterns of myocardial ischemia with nifedipine GITS in patients with chronic stable angina. J Am Coll Cardiol 1992; 19:1380-1389.
8. Rogers WJ, Bourassa MG, Andrews TC et al. Asymptomatic Cardiac Ischemia Pilot (ACIP) study: outcome at 1 year for patients with asymptomatic cardiac ischemia randomized to medical therapy or revascularization. J Am Coll Cardiol 1995; 26: 594-605.
9. Tzivoni D, Braun S, Schelling A. Results of the Mibefradil Ischemia Suppression Trial (MIST). (Abstr.) J Am Coll Cardiol 1996; 27 (suppl A): 185A.
10. Pepine CJ. Effect of calcium antagonists in variant or Prinzmetall’s angina. Can J Cardiol 1995; 11: 952-956.
H.TurittoG, PezzelaA, Prati PL. Diltiazem in spontaneous angina: comparison with nifedipine and verapamil. J Ital Cardiol 1985; 15: 1019-1084.
12. Prida XE, Gelman JS, Feldman RL, Hill JA, Pepine CJ, Scott E. Comparison of diltiazem and nifedipine alone and in combination in patients with coronary artery spasm. J Am Coll Cardiol 1987; 9 (2): 412-419.
13. Specchia G, Ardissino D, Ghio S, Barberis P, Colombo ML, De Servi S. Increased coronary tone in exertional angina: the beneficial effects of calcium antagonists. Cardiovasc Drug Ther 1990; 4:893-898.
14. Ardissino D, DeServi S, Barberis P, Dinicheli G, Falcone C, Ochan M, Specchia G, Montemartini C. Significance of hyperventilation-induced ST-segment depression in patients with coronary artery disease. J Am Coll Cardiol 1990; 13:1-7.
15. Stone PH, Antman EM, Muller JE et al. Calcium channel blocking agents in the treatment of cardiovascular disorders. Part II: Hemodynamic effects and clinical applications. Ann Intern Med 1980; 93: 886-904.
16. Rice KR, Gervino E, Jarisch WR et al. Effects of nifedipine on myocardial perfusion during exercise in chronic stable angina. Am J Cardiol 1990; 65: 1097-1101.
17. Taylor SH. Usefulness of amlodipine for angina pectoris. Am J Cardiol 1994; 73:28A-33A.
18. Conn PF, Vetrovee GW, Nesto Ret al. The NifedipineTotal Ischemia Awareness Program: a national survey of painful and painless myocardial ischemia including results of anti-ischemic therapy. Am J Cardiol 1989; 63:534-539.
19. Stone DL, Stephens JD, Banim SO. Coronary haemodynamic effects of nifedipine: comparison with glyceryl trinitrate. Br Heart J 1983; 49:442-446.
20. Engel HJ, Liethlen PR. Beneficial enhancement of coronary blood flow by nifedipine: comparison with nitroglycerin and beta blocking agents. Am J Med 1981; 71: 658-665.
21. Rousseau MF, Vincent MF, Van Hoof F et al. Effects of nicardipine and nisoldipine on myocardial metabolism, coronary blood flow, and oxygen supply in angina pectoris. Am J Cardiol 1984; 54: 1189-1194.
22. Ferlinz J. Nifedipine in myocardial ischemia, systemic hypertension, and other cardiovascular disorders. Ann Intern Med 1986; 105:914-923.
23. Fox К, Mulkahy D, Findlay I . The Total Ischemic Burden Trial (TIBET). Eur Heart J 1996; 17: 96-103.
24. Rehuquist N, Hjeurdahl P, Billings E et al. The Angina Prognosis Study In Stockholm (APSIS). Eur HeartJ 1996; 17: 76-81.
25. Conti CR. Reexamining the clinical safety and roles of calcium antagonists in cardiovascular medicine. Am J Cardiol 1996; 78 (9A): 13-18.
26. Muller JE, Turi ZG, Pearte DL et al. Nifedipine and conventional therapy for unstable angina: a randomized double blind comparison. Circulation 1984; 69: 728-739.
27. Gerstenblith G, Ouyang P, Acheeff SC et al. Nifedipine in unstable angina: a double blind, randomized trial. N Engl J Med 1982; 306: 885-889.
28. Report of the Holland Interuniversity Nifedipine/Metoprolol Trial (HINT) Research Group. Early treatment of unstable agina in coronary care unit: a randomized, dobule blind, placebo controlled comparison of recurrent ischemia in patients treated with nifedipine ormetoprololorboth. BrHeartJ 1986; 56:400-413.
29. Theroux P, Tachymans Y, Morissette D et al. A randomized study comparing propranolol and diltiazem in the treatment of unstable angina. J Am Coll Cardiol 1985; 5: 717-722.
30. Andre-Fouet X, Uadin J P, Gayet С et al. Comparison of short-term efficacy of diltiazem and propranolol in unstable agina at rest: a randomized trial in 70 patients. Eur Heart J 1983; 4: 691-698.
31. Muller JE, Morrison J, Stone PH etal. Nifedipine therapy for patients with threatened and acute myocardial infarction: randomized, double blind, placebo-controlled comparison. Circulation 1984; 69:740-747.
32. Wilcox R, Hampton J, Banks S et al. Trial of early nifedipine in acute myocardial infarction. The TRENT study. BMJ 1986; 293: 1204.
33. The Israel SPRINT Study Group. Secondary Prevention Reinfarction Israeli Nifedipine Trial (SPRINT). A randomized intervention trial of nifedipine in patients with acute myocardial infarction. Eur Heart J 1988; 9: 354-364.
34. Simes PA, Overskeid K, Pedersen TRetal. Evolution of infarct size during the early use of nifedipine in patients with acute myocardial infarction. The Norwegian Nifedipine MulticenterTrial. Circulation 1984; 70: 638-644.
35. Multicenter Diltiazem Postinfarction Trial Research Group. The effect of diltiazem on mortality and reinfarction after myocardial infarction. N Engl J Med 1988; 319: 385-392.
36. The Danish Study Group Verapamil in Myocardial Infarction. Effect of verapamil on mortality and major events after acute myocardial infarction. The Danish Verapamil Infarction Trial II — DAVIT-II. Am J Cardiol 1990; 66:779-785.
37. Yusuf S, Held P, Furberg C. Update of effects of calcium antagonists in myocardial infarction or angina in light of the second Danish Verapamil Infarction Trial (DAVIT-II) and other recent studies. (Editorial) Am J Cardiol 1991; 67:1295-1297.
38. Gibson RS, Boden WE, Theroux P et al. Diltiazem and reinfarction in patients with non-Q-wave myocardial infarction. N Engl J Med 1986; 315:423-429.
39. Boden WE, Krone RJ, Kleiger RE et al. Diltiazem reduces long-term cardiac event rate after non-Q-wave infarction. Circulation 1988; 78 (suppl II-4): II-96.
40. Rengo F, Carbonin P, Pahor M et al. Acontrolled trial of verapamil in patients after myocardial infarction. Results of the Calcium Antagonist Reinfarction Italian Study (CRIS). Am J Cardiol 1996; 77: 365-369.
41. Vesselinovitch D, Mallan JF, Wissler RW et al. Carotid athero-genesis inhibited by sympathectomy, propranolol, and nifedipine in rhesus monkeys. (Abstr.) Arteriosclerosis 1986; 6: 561 a.
42. Rouleau JL, Parmley WW, Stevens J et al. Verapamil suppresses atherosclerosis in cholesterol-fed rabbits. J Am Coll Cardiol 1983; 1: 1453-1460.
43. Blumlein SL, Sievers R, Kidd P et al. Mechanisms of protection from atherosclerosis by verapamil in the cholesterol-fed rabbit. Am J Cardiol 1984; 54: 884-889.
44. Sugano M, Nakashima Y, Matsuhma et al. Suppression of atherosclerosis in cholesterol-fed rabbits by diltiazem injection. Arteriosclerosis 1986; 6:237-241.
45. Lichtlen PR, Hugenholtz PG, Rafflenbeul W et al. Retardation of angiographic progression of coronary artery disease by nifedipine. Results of the Interventional Nifedipine Trial on Antiatherosclerotic Therapy (INTACT). Lancet 1990; 335:1109-1113.
46. Schroeder JS, Gaos S-Z, Alderman EL etal. Preliminary study of diltiazem in the prevention of coronary artery disease in heart transplant receipients. N Engl J Med 1993; 328:164-170.
47. Ruzicka M, Leenen FH. Relevance of intermittent increases in sympathetic activity for adverse outcome on short-acting calcium antagonists. In: Laragh JH, Brenner BM (eds.) Hypertension: Pathophysiology, Diagnosis, and Management. 2nd ed. New York. Raven Press 1995:2815-2825.
48. Murray E. Calcium antagonist controversery: the emerging importance of drug formulation as a determinat of risk. Am J Cardiol 1997; 79 (10a): 9-19.
49. CaliffR.TardiffB, PeiperRetal. Use of calcium channel antagonists in myocardial revascularization procedures. Am J Cardiol 1996; 77: 260-310.
50. Waters D, Lesperance J, Francetich M et al. A controlled clinical trial to assess the effect of a calcium channel biocker on the progression of atherosclerosis. Circulation 1990; 82:1940 -1953.
51. Cruickshank J, Lewis J, Moore V et al. Reversibility of LVH by differing types of antihypertensive therapy. J Hum Hypertens 1992; 6:85.
52. Goldberg S, Reischek N, Wilson J et al. Nifedipine in the treatment of Prinzmetal’s (variant) angina. Am J Cardiol 1979; 44: 804.
53. Materson B, Reda D, Cushman W etal. Single drug therapy for hypertension in men: a comparison of six antihypertensive agents with placebo. N Engl J Med 1993; 328: 914
54. Neaton J, Girmm R Jr, Prineas R et al. Treatment of mild hypertension study: final results. JAMA 1993; 270: 713-724.
55. Lahiri A, Rodrigues EA, Carboni GP et al. Effects of long-term treatment with calcium antagonists on left ventricular diastolic function in stable agnina and heart failure. Circulation 1990; 81 (suppl III): 111-130—111-138.
56. Bonow R, Ostrow H, Rosing D et al. Effects of verapamil on left ventricular systolic and diastolic function in patients with hypertrophic cardiomyopathy: pressure volume analysis with a non-imaging scintillation probe. Circulation 1983; 68:1062-1073.
57. Figulla H, Gietem F, ZeymerU etal. Diltiazem improves cardiac function and exercise capacity in patients with ideopathic dilated cardiomyopathy: results of the diltiazem in dilated cardiomyopathy trial. Circulation 1996; 94: 346-352.
58. Packer M, Nicod P, Bijoy R etal. Randomized multicenter, double blind placebo controlled evaluation of amlodipine in patients with mild to moderate heart failure. J Am Coll Cardiol 1991; 17:274A.
59. O’Connor CM, Belkin RN, Carson PE et al. Effect of amlodipine
on mode of death in severe chronic heart failure. The PRAISE trial. Circulation 1995; 92 (suppl I): 1-143.
60. Cohn JN, Ziesche SM, Loss LE et al. Effect of felodipine on short-term exercise and neurohormones, and long-term mortality in heart failure: results of VHEFT III. Circulation 1995; 92 (suppl I): 1-143.
61. Scognamiglio R, Rahimtoola M, Fasoli G et al. Nifedipine in asymptomatic patients with severe aortic regurgitation and normal left ventricular function. N Engl J Med 1994; 331: 689-694.
62. DeFeyter PJ, Kerkkamph HJ, DeJong JP et al. Sustained beneficial effect of nifedipine in primary pulmonary hypertension. Am Heart J 1983; 105: 333-334.
63. Kambara H, Fujimoto K, Wakabayashi A et al. Primary pulmonary hypertension: beneficial therapy with diltiazem. Am Heart J 198; 101:230-231.
64. Rich S, Kaufrnann E, Levy PS et al. The effect of high doses of calcium channel blockers on survival in primary pulmonary hypertension. N Engl J Med 1992; 327: 76-81.
65. Smith CD, Mendry RJ. Controlled trial of nifedipine in the treatment of Raynaud’s phenomenon. Lancet 1982, II: 1299-1301.
66. Rodeheffer RJ, Rommer JA, Wigley F et al. Controlled double-blind trial of nfedipine in the treatment of Raynaud’s phenomenon. N Engl J Med 1983; 308: 880-883.
67. Corbin DO, Wood DA, Macintyre CA et al. A randomized double blind cross-over trial of nifedipine in the treatment of primary Raynaud’s phenomenon. Eur Heart J 1986; 7: 165-170.
68. PsatyBM, HeckbertSR, KoepsellTDetal.Theriskofmyocardial infarction associated with antihypertensive drug therapies. JAMA 1995; 274: 620-625.
69. Furberg CD, Psaty BM, Meyer JV. Dose-related increase in mortality in patients with coronary heart disease. Circulation 1995; 92: 1326-1331.
70. Pahor M, Gurinik JM, Corti MC et al. Long-term survival and use of antihypertensive medications in older persons. J Am Geriatr Soc1995;43: 1191-1197.
71. Burt VL, Whelton P, Roccella EJ et al. Prevalence of hypertension in the US adult population. Results from the Third National Health and Nutrition Examination Survey, 1988-1991. Hypertension 1995; 25: 305-313.
72. Cardiomonitor 1992. In: Hoise J, Wiklund I. Managing hypertension in general practice: can we do better? J Hum Hypertens 1995; 9 (supp 2): S15-S18.
73. Elliot WJ. Drug therapy and dropouts in a teritary hypertension clinic. (Abstr.) Am J Hypertens 1994, 7: 26A.
74. Kleinbloesem CH, van Brummelen P, Danlof M et al. Rate of increase in the plasma concentration of nifedipine as a major determinant of its hemodynamic effects in humans. Clin Pharmacol Ther 1987; 41: 26-30.
75. Frohlich ED, McLoughlin MJ, Losem CJ et al. Hemodynamic comparison of two nifedipine formulations in patients with essential hypertension. Am J Cardiol 1991; 68: 1346-1350.
76. Parati G, Pomidossi G, Albini F et al. Relationship of 24-hour blood pressure mean and variability to severity of target organ damage in hypertension. J Hypertens 1987; 5: 93-98.
77. Frattola A, Parati G, Cuspidi С et al. Prognostic value of 24-hour blood pressure variability. J Hypertens 1993,11:1133-1137.
78. Malakoff RF, Lorell BH, Mudge GH et al. Beneficial effects of nifedipine on regional myocardial blood flow in patients with
coronary artery disease. Circulation 1982; 65 (suppl I): I-32-I-37.
79. Kugiyama K, Yasue H, Horio Y et al. Effects of propranolol and nifedipine on exercise-induced attack in patients with variant angina: assessment by exercise Thallium-201 myocardial scintigraphy with quantitative rotational tomography. Circulation 1986; 74 (2): 374-380.
80. Bonaduce D, Muto P, Morgano G et al. Effect of nifedipine on dipyridamole Thallium-201 myocaridal scintigraphy. Clin Cardiol 1986; 9 (6): 285-288.
81. Hayward R, Hunter GJ, Swanton H et al. Effects of nifedipine on coronary perfusion: recent assessment by parametric digital subtraction. Eur Heart J 1987; 8 (suppl K): 1-7.
82. Nesto RW, White HD, Ganz P et al. Addition of nifedipine to maximal beta-blocker and nitrate therapy: effects on exercise capacity and global left ventricular performance at rest and during exercise. Am J CardioM985;55:3E-8E.
83. Myers MG, Raemsch KD etal. Comparative pharmcokinetics and antihypertensive effects of the nifedipine tablet and capsule. J Cardiovasc Pharmacol 1987; 10 (suppl 10): S76-S78.
84. Swanson DR, Barclay BL, Wong PS et al. Nifedipine gastrointestinal therapeutic system. Am J Med 1987; 83 (suppl 6B): 3-9.
85. Chung M, Reitberg DP, Gafney M et al. Clinical pharmacokinetics of nifedipine gastrointestinal therapeutic system. A controlled release formulation of nifedipine. Am J Med 1987; 83 (suppl 6B): 10-14.
86. Siscovick DS, Raghunathan ТЕ, Psaty BM et al. Diuretic therapy for hypertension and the risk of primary cardiac arrest. NEJM 1994; 330:1852-1857.
87. Gong L, Zhang W, Zhu J et al. Shanghai Trial Of Nifedipine in the Elderly (STONE). J Hypertens 1996; 14:1237-1245.
88. Braun S, Boyko V, Behar S et al. Calcium antagonist and mortality in patients with coronary artery disease: a cohort study of 11,575 patients. J Am Coll Cardiol 1996; 28(1): 7-11.
89. Aursnes I, Lffleskare I, Froyland H etal. Association between various drugs used for hypertension and risk of acute myocardial infarction. Blood Pres 1995; 4:157-163.
90. Jick H, Gurewich V, Vasilakis C. The risk of myocardial infarction associated with antihypertensive drug treatment in persons with uncomplicated essential hypertension. Pharmacotherapy 1996; 16: 321-326.
91. Kloner RA, Vetrovec G. Long-acting calcium channel blockers nifedipine GITS and amlodipine in hypertensin. Rate of myocardial infarction. (Abstr.) J Am Coll Cardiol 1996; 27 (suppl A): 177A
92. Abascal VM, Larson MG, Evans JC et al. Calcium channel blocker use is not associated with increased mortality. (Abstr.) Circulation 1996; 64 (suppl I): 3383.
93. Leader SG, Mallick R, Briggs NC. Myocardial infarction in newly diagnosed hypertensive Medicaid patients free of coronary heart disease and treated with calcium channel blockers. Am J Med 1997; 102:150-157.
94. Messerii FH. Safety of calcium antagonists: dissecting the evidence. Am J Cardiol 1996; 78 (9A): 19-24.
95. Warwick D. FDA gives calcium channel blockers clean bill of health but warns of short-acting nifedipine hazards. JAMA 1996; 275:423-424.
96. Vagelos RH, Schroeder JS. New development in the use of calcium entry blocking drops in cardiovascular disease. Cardiology Clinics 1997; 1: 11-28.
Комментарии
(видны только специалистам, верифицированным редакцией МЕДИ РУ)
Антагонисты кальция (АК) — органические соединения, ингибирующие деятельность потенциалзависимых кальциевых каналов и тем самым ограничивающие поступление ионов кальция в клетку. Эти препараты уменьшают потребление миокардом кислорода, изменяют силу сердечных сокращений, скорость атриовентрикулярного проведения, вызывают сосудорасширяющий эффект.
История изучения АК началась 30 лет назад. При исследовании свойств новых коронарорасширяющих препаратов из группы фенилалкиламинов — прениламина и вера-памила A. Fleckenstein обнаружил у них отрицательный инотропный эффект. Добавление кальция уменьшило феномен ухудшения сократимости мышечных волокон. В проведенной серии опытов было продемонстрировано блокирование этими препаратами возбуждения, вызванного притоком кальция по специфическим каналам внутрь клеток. Так появился термин «антагонисты кальция». В качестве близких понятий нередко используются словосочетания «блокаторы кальциевых каналов», «блокаторы медленных кальциевых каналов» [14], однако их нельзя считать синонимами понятия «антагонисты кальция». Блокада кальциевого тока несовместима с жизнью организма, поэтому в практической кардиологии целесообразнее употреблять термин «антагонисты кальция».
Антагонисты кальция быстро завоевали популярность среди практических врачей и с начала 70-х годов прочно вошли в медицинскую практику. Этому способствовал, во-первых, очень широкий спектр показаний к применению АК (лечение артериальной гипертензии (АГ), ишемической болезни сердца (ИБС), вазоспастических состояний, нарушений сердечного ритма). Во-вторых, АК, особенно группы нифедипина, казались безопасными, не требующими частого врачебного контроля по сравнению с бета-адреноблокаторами, другими антиаритмическими средствами, многими гипотензивными препаратами. Поэтому в 80-х годах АК широко применяли в фармакотерапии ИБС и АГ.
Однако исследование SPRINT на большом материале показало увеличение числа повторных инфарктов миокарда под влиянием лечения нифедипином в течение 10 мес по сравнению с плацебо [36]. В последнее десятилетие были проведены новые обширные проспективные исследования эффективности и безопасности АК у больных с разнообразной патологией. Так, в 1995 г. появились три очень важные работы. В первых двух отмечено, что АК короткого действия, в частности нифедипин, при длительном лечении способны повышать риск развития инфаркта миокарда и внезапной смерти у больных АГ [30, 31]. В третьей работе продемонстрировано увеличение смертности при использовании нифедипина у постинфарктных больных, у лиц со стабильной и нестабильной стенокардией [15].
Научная полемика о месте и роли АК в кардиологии продолжается до сих пор.
В настоящем обзоре сделана попытка отразить современные данные об эффективности и безопасности АК и дать практические рекомендации по их применению.
Имеется несколько классификаций АК, что свидетельствует о сложности и незавершенности проблемы. Самой удачной, на наш взгляд, является классификация, предложенная ВОЗ в 1987 г. Ее можно назвать химико-фармакологической, так как выделенные по химическому признаку категории включают препараты с близким фармакологическим эффектом (табл. 1).
Таблица 1. Классификация антогонистов кальция
|
Категория |
Химическая структура |
Препараты |
|
Селективно действующие на медленные кальциевые каналы |
||
|
1 |
Производные фенилалкиламинов или верапамилподобные |
Верапамил Анипамил Галлопамил |
|
2 |
Производные дигидропиридина или нифедипин подобные |
Нифедипин Фелодипин Нимодипин Нисолдипин Никардипин Амлодипин Исрадипин Лацидипин Нитрендипин Риодипин |
|
3 |
Производные бензотиазепинов или дилтиаземподобные |
Дилтиазем Бепридил |
|
Неселективно действующие на медленные кальциевые каналы |
||
|
4 |
Производные дифенилпиперазина или флунаризинподобные |
Флунаризин Циннаризин |
|
5 |
Производные прениламина или прениламинподобные |
В настоящее время не применяются |
|
6 |
Препараты различной химической структуры |
Мибефрадил Кароверин Пергексилин Лидафлазин |
К сожалению, ни одна из предложенных классификаций, в том числе ВОЗ, не удовлетворяет клиницистов в полной мере, поскольку все они построены по принципу учета какого-то одного критерия: химической структуры препарата, преимущественного влияния на сосуды или сердце, проводимости и т. п.
Препараты первой категории снижают сократительную функцию миокардиоцитов (отрицательное инотропное действие), подавляют активность синоатриального узла (урежение сердечного ритма), замедляют атриовентрикулярную проводимость, оказывают умеренное вазодилатирующее действие, в том числе на коронарные артерии.
Препараты второй категории практически не обладают отрицательным инотропным действием, не влияют на синоатриальный узел и атриовентрикулярную проводимость, но оказывают выраженное вазодилатирующее действие (в том числе на коронарные артерии), способствуют развитию рефлекторной тахикардии.
Препараты третьей категории сочетают в себе качества двух первых категорий с преобладанием первой.
Препараты четвертой категории избирательно действуют на мозговые артерии, практически не изменяя тонус коронарных и периферических артерий.
Средства, относящиеся к пятой категории, в настоящее время не применяются из-за их кардиотоксичности.
В литературе можно встретить понятия «АК первого и второго поколений». К препаратам первого поколения относятся верапамил, нифедипин и дилтиазем. Все остальные средства причисляются ко второму поколению, за исключением мибефрадила.
Существует также термин «селективность АК». Под ним понимают значительное преобладание сосудорасширяющего действия над эффектами в отношении миокарда и проводящей системы. Высокоселективные средства (амлодипин, фелодипин) практически не влияют на сердечную мышцу и проводящую систему. К сожалению, понятие «селективность» носит скорее экспериментальный, нежели клинический характер. В опытах показано, что нисолдипин в 1000 раз селективнее по отношению к венечным артериям, чем к миокарду. Можно предположить, что высокоселективный нисолдипин у больных ИБС будет гораздо эффективнее неселективного верапамила. Однако в сравнительных исследованиях показано, что верапамил у больных ИБС во многих случаях предпочтительнее нисолдипина [28].
В кардиологии применяются препараты первых трех категорий. Средства, относящиеся к четвертой категории (флунаризин, циннаризин), используются при лечении сосудистых заболеваний головного мозга.
Основные эффекты АК представлены в табл. 2.
Таблица 2. Основные эффекты антагонистов кальция
|
Препарат |
Периферическая вазодилатация |
Гипотензивное действие |
Подавление функции синусового узла и AV-проводимости |
Отрицательное инотропное действие |
Воздействие на сосуды мозга |
Частота сердечных сокращений |
|
Амлодипин |
++ |
+ |
— |
— |
— |
|
|
Бепридил |
+ |
— |
+ |
+ |
— |
|
|
Дилтиазем |
+ |
+ |
+ |
+ |
— |
|
|
Фелодипин |
++ |
+ |
— |
— |
— |
|
|
Флунаризин |
+ |
— |
— |
— |
+ |
— |
|
Исрадипин |
++ |
+ |
— |
— |
— |
|
|
Никардипин |
++ |
+ |
— |
— |
+ |
— |
|
Нифедипин |
++ |
+ |
— |
— |
— |
|
|
Нимодипин |
++ |
+ |
— |
— |
+ |
— |
|
Верапамил |
+ |
+ |
+ |
+ |
Аритмии. Антиаритмическим действием обладают препараты первой и третьей категорий. В эквивалентных концентрациях они подавляют активность синоатриального узла и угнетают атриовентрикулярную проводимость, поэтому показанием к применению этих средств являются наджелудочковые аритмии.
Анипамил и галлопамил по фармакологическим эффектам идентичны верапамилу, но оказывают более мягкое действие. Бепридил — относительно новое средство, которое расценивается как сильный антиангинальный препарат резерва, используемый при неэффективности рутинной терапии. В качестве антиаритмического средства бепридил не применяется из-за недостаточной изученности и медленного развития эффекта (около недели от начала терапии) [28].
Антиаритмические свойства верапамила более выражены, чем у дилтиазема. Положительным качеством дилтиазема является меньшее отрицательное инотропное действие. Поэтому фирмы-производители многих стран выпускают дилтиазем для внутривенного введения и рекомендуют применять его в ситуациях, когда сократительная функция сердца скомпрометирована. Так, дилтиазем эффективен при длительной внутривенной инфузии для купирования и профилактики фибрилляции и трепетания предсердий в кардиохирургии [10].
Верапамил и дилтиазем используются при следующих аритмиях:
* наджелудочковая экстрасистолия (лечение и профилактика);
* наджелудочковая пароксизмальная тахикардия (лечение и профилактика);
* купирование пароксизмов фибрилляции и трепетания предсердий (внутривенное введение или инфузия);
* профилактика пароксизмов фибрилляции и трепетания предсердий (прием внутрь);
* лечение постоянной формы мерцательной аритмии (совместно с дигоксином).
Сообщалось, что верапамил также эффективен при желудочковой пароксизмальной тахикардии, исходящей из задней ветви левой ножки пучка Гиса (конфигурация на ЭКГ, как при блокаде правой ножки пучка Гиса) [2].
Использование верапамила и дилтиазема при аритмиях имеет два серьезных ограничения. Во-первых, эти препараты нельзя применять у пациентов с синдромом Вольфа—Паркинсона—Уайта вследствие значительного риска учащения сердечного ритма и развития фибрилляции желудочков. Во-вторых, сочетание этих средств с некоторыми препаратами таит потенциальную угрозу.
Верапамил нельзя вводить внутривенно одновременно или последовательно с сердечными гликозидами, бета-адреноблокаторами и антиаритмическими препаратами I класса (новокаинамид, пропафенон, этацизин). Такие сочетания нередко приводят к развитию блокад и асистолии. Комбинация внутривенного введения дилтиазема с указанными средствами допустима, но с соблюдением двух правил: уменьшение доз вводимых препаратов и мониторирование ЭКГ.
Комбинированная терапия верапамилом или дилтиаземом с сердечными гликозидами (прием внутрь) является общепринятой. Следует помнить, что верапамил, как ни одно лекарственное средство, увеличивает содержание в крови и тканях сердечных гликозидов. Это требует уменьшения доз гликозидов как минимум на 1/3. Комбинация верапамила и бета-адреноблокаторов внутрь допустима, но также потенциально опасна. Описаны случаи развития выраженной брадикардии даже при использовании бета-блокатора тимолола (в виде глазных капель) совместно с верапамилом [28]. Комбинация АК дигидропиридинового ряда с бета-блокаторами безопасна.
Безопасность длительного использования верапамила и дилтиазема в качестве антиаритмических средств специально не изучалась. Обычно ссылаются на обширные проспективные исследования верапамила и дилтиазема у постинфарктных больных.
В исследовании MDPIT дилтиазем назначали 1232 больным после инфаркта миокарда в дозе 240 мг/сут на протяжении 25 мес. Аналогичная группа пациентов получала плацебо. Общая летальность в обеих группах была одинаковой. Однако после выделения подгруппы с достаточной сократительной функцией сердца (фракция выброса (ФВ) более 40%) отмечено увеличение выживаемости у больных, получавших дилтиазем [27].
В исследовании DAVIT-II верапамил назначался, начиная с подострого периода инфаркта миокарда, по 120 мг три раза в день (360 мг/сут) в течение 18 мес. Контролем служилианалогичные больные, получавшие плацебо. Общая летальность в группе верапамила составила 11,1%, в группе плацебо — 13,8%. После выделения больных с дисфункцией левого желудочка (ФВ менее 40%) в подгруппе с достаточной сократительной способностью сердца отмечено достоверное уменьшение общей смертности и случаев повторного инфаркта миокарда: 9% в группе верапамила против 16% в контрольной [38].
Таким образом, можно считать, что у больных ИБС без сердечной недостаточности длительное назначение верапамила или дилтиазема является безопасным.
Стабильная стенокардия. Общепризнано, что нифедипин и другие дигидропиридиновые препараты короткого действия небезопасны, так как создают потенциально серьезные изменения АД и симпатической активности [25]. Поэтому в последние годы обсуждается роль АК второго поколения (амлодипин, фелодипин, никардипин, нисолдипин), препаратов продленного действия, а также верапамила и дилтиазема в лечении ИБС.
Конечной целью лечения стабильной стенокардии является предупреждение внезапной смерти, инфаркта миокарда и других сердечно-сосудистых осложнений. В терапии стенокардии традиционно применяются три основные группы препаратов: нитраты, бета-адреноблокаторы и АК. При этом большинством кардиологов АК не расцениваются как средства первого ряда, за исключением случаев вазоспастической стенокардии. Дигидропиридиновые АК вызывают рефлекторную тахикардию и активацию симпатоадреналовой системы. Поэтому в большинстве случаев при лечении стенокардии АК дигидропиридинового ряда комбинируются с бета-адреноблокаторами или нитратами. Возможна монотерапия верапамилом или дилтиаземом, которые несколько замедляют сердечный ритм [15].
В 2-летнем исследовании TIBET изучалась эффективность терапии и влияние на прогноз у больных стабильной стенокардией бета-блокатора атенолола, нифедипина пролонгированного действия и их комбинации. 682 больных были разделены на три группы. Первая получала атенолол в дозе 50 мг два раза в сутки, вторая — нифедипин пролонгированного действия по 20—40 мг два раза в сутки, третья — атенолол и нифедипин в указанных дозах. В пересчете на один год случаи смерти от сердечных причин и нефатального инфаркта миокарда среди больных, получающих атенолол, составили 3,8%, среди получавших нифедипин — 4,5%, при комбинированной терапии — 2,5% [7].
В исследовании APSIS сравнивалось лечение верапамилом и метопрололом у 809 больных стабильной стенокардией в течение более трех лет. Выбор этих лекарственных препаратов обусловлен тем, что метопролол эффективен у больных ИБС, а верапамил по меньшей мере не увеличивал летальность у постинфарктных больных [38]. Число неблагоприятных исходов было примерно одинаковым: 2,6% в группе метопролола и 2,4% в группе верапамила в пересчете на один год лечения [32]. Селективные АК с выраженной коронародилатирующей активностью (амлодипин и фелодипин) не влияли на прогноз и не уменьшали риск внезапной смерти и инфаркта миокарда у больных ИБС [3, 29].
Таким образом, монотерапия стабильной стенокардии наиболее целесообразна селективными бета-адреноблокаторами или верапамилом. Эффективны комбинации дигидропиридиновых АК с бета-адреноблокаторами. Эффективность нитратов повышается в комбинации с бета-адреноблокаторами или АК. Следует иметь в виду, что нитраты значительно улучшают качество жизни у больных стенокардией, тем не менее в настоящее время нет оснований считать, что нитраты (даже при длительном приеме) улучшают прогноз у больных ИБС [8, 19].
Безболевая ишемия миокарда. Эта разновидность ИБС имеет ту же прогностическую значимость, что и стабильная стенокардия. Подавление эпизодов безболевой ишемии предупреждает внезапную смерть и инфаркт миокарда.
Результаты исследований последних 10 лет показывают, что дигидропиридиновые производные короткого действия менее эффективны в предупреждении ишемических эпизодов, нежели недигидропиридиновые АК или бета-адреноблокаторы [21, 23].
В исследовании ACIP сравнивалась эффективность нескольких препаратов у больных с безболевой ишемией миокарда. Показано, что ишемические эпизоды наиболее надежно подавляются комбинацией нифедипин пролонгированного действия + атенолол или дилтиазем + изосорбида динитрат [35].
Новый АК мибефрадил проявляет сильное антиишемическое действие. В многоцентровом плацебо-контролируемом исследовании мибефрадил существенно уменьшал число и длительность ишемических эпизодов. Амлодипин обладает менее выраженными антиишемическими свойствами по сравнению с мибефрадилом [37].
Нестабильная стенокардия. Цель лечения нестабильной стенокардии — ее перевод в стабильную, что значительно уменьшает риск инфаркта миокарда и внезапной смерти. Все дигидропиридиновые АК (за исключением амлодипина) вызывают рефлекторную тахикардию. Их коронарорасширяющий эффект не может компенсировать учащение сердечного ритма, что неблагоприятно сказывается на исходе болезни.
В метаанализе, проведенном Furberg с соавт. [16], оценивалась роль нифедипина у больных с различными формами ИБС, в том числе нестабильной стенокардией. Риск смерти при дозе нифедипина 30—50 мг/ сут составлял 1,06. Доза 60 мг/сут повышала риск до 1,18, а доза 80 мг/сут — до 2,83. Работа Furberg неоднократно подвергалась критике из-за включения в анализ различных форм ИБС. Но даже после вычленения больных со стабильной стенокардией в данной группе умерло 320 человек, принимавших нифедипин, в контрольной группе — 291 пациент [26].
Влияние нифедипина изучалось у 515 больных нестабильной стенокардией. Это исследование было прекращено досрочно, так как монотерапия нифедипином повышала риск развития инфаркта миокарда в 1,5 раза [33].
Считается, что дилтиазем и верапамил эффективны и безопасны для больных нестабильной стенокардией. АК дигидропиридинового ряда должны применяться только в комбинации с бета-адреноблокаторами [13, 33].
Возможности использования основных антиангинальных препаратов у больных стенокардией с сопутствующей патологией приведены в табл. 3.
Таблица 3. Основные антиангинальные средства для лечения стенокардии при наличии сопутствующих заболеваний
|
Сопутствующие заболевания |
Нитраты |
Бета-блокаторы |
Антагонисты кальция |
||
|
Нифедипин |
Дилтиазем |
Верапамил |
|||
|
Артериальная гипертензия |
± |
++ |
? |
+ |
+ |
|
Недавний инфаркт миокарда и постинфарктный кардиосклероз |
++ |
++ |
— |
± |
+ |
|
Дисфункция левого желудочка и сердечная недостаточность |
+ |
± |
— |
— |
— |
|
Суправентрикулярные аритмии |
0 |
++ |
— |
+ |
++ |
|
Бронхообструктивные заболевания |
+ |
— |
+ |
++ |
++ |
|
Заболевания периферических артерий |
++ |
+ |
++ |
++ |
++ |
|
Инсулинзависимый диабет |
++ |
± |
++ |
++ |
++ |
|
Инсулиннезависимый диабет |
++ |
+ |
++ |
++ |
++ |
|
Хронические заболевания почек |
++ |
+ |
++ |
++ |
++ |
|
Синусовая брадикардия или атриовентрикулярная блокада 1 ст. |
++ |
— |
++ |
± |
— |
Инфаркт миокарда. В зависимости от конкретного препарата, срока назначения и величины инфаркта миокарда (ИМ) результаты исследований эффективности АК у данной категории больных значительно различались.
Попытки применять различные АК в остром периоде болезни либо не влияли на исход, либо ухудшали прогноз [38, 39]. Принято считать, что в остром периоде ИМ оправдано внутривенное применение дилтиазема у больных с тахисистолической формой фибрилляции предсердий [4, 10]. Использование нифедипина после ИМ ухудшает выживаемость больных [36].
Из всех АК, изучавшихся в проспективных исследованиях у больных ИМ, только два препарата оказались эффективными и безопасными при длительном приеме. Верапамил и дилтиазем, назначаемые с подострого периода, улучшали прогноз у больных без систолической дисфункции левого желудочка. Прием верапамила на протяжении 18 мес по сравнению с плацебо существенно уменьшал общую смертность и число случаев повторного ИМ (9% против 16%) [38]. Дилтиазем у больных инфарктом миокарда без формирования зубца Q уменьшал вероятность внезапной смерти и повторного инфаркта (уровень риска 0,77 при Р=0,05) [27].
Применение дигидропиридиновых АК в любом периоде ИМ и в постинфарктном периоде нецелесообразно [4, 23, 28]. Верапамил или дилтиазем могут считаться препаратами первого ряда в лечении больных после ИМ без систолической дисфункции.
Артериальная гипертензия. Несмотря на большой опыт применения АК у больных с различными формами АГ, здесь существует немало нерешенных проблем. АК наряду с диуретиками, бета-адреноблокаторами и ингибиторами ангиотензинпревращающего фермента (ИАПФ) применяются у миллионов пациентов.
Psaty и соавт. [31] ретроспективно изучали лечение 1492 больных, у которых развился ИМ. Оказалось, что риск возникновения ИМ был непосредственно связан с приемом некоторых препаратов. Контрольной группой с риском развития ИМ 1,0 считались больные, принимавшие по поводу АГ небольшие дозы бета-адреноблокаторов. По мере увеличения дозы риск развития ИМ уменьшался. В отношении АК (нифедипин, дилтиазем и верапамил короткого действия) наблюдалась обратная связь. Риск развития ИМ у лиц, принимавших небольшие, средние и большие дозы АК, составлял 1,13; 1,42 и 1,81 соответственно. Подобная дозозависимость имела математически значимый характер для всех пациентов с гипертонической болезнью [31]. Сходные данные получены у пожилых людей, принимавших АК по поводу гипертензии [30].
В исследовании MIDAS изучалась роль исрадипина (АК второго поколения) у больных атеросклерозом сонных артерий и гипертензией. Лечение продолжалось около трех лет. Больные, получавшие исрадипин, по сравнению с пациентами, принимавшими гидрохлортиазид, имели повышенный риск ИМ, внезапной смерти и инсульта (уровень риска 1,78 при Р=0,07) [24]. В другом исследовании 1017 больных получали АК по поводу гипертензии. Эта группа сравнивалась с 1025 пациентами, принимавшими ИАПФ. Риск сердечно-сосудистых осложнений у больных, принимавших АК, был значительно выше и составил 3,0 при Р=0,02 [11].
В настоящее время в Северной Америке и Европе проводится 6 исследований влияния амлодипина, верапамила, фелодипина, нитрендипина и дилтиазема на долгосрочный прогноз у больных АГ. Предполагается включение в программу более 70 тыс. пациентов [4].
Из исследований DAVIT-1, DAVIT—II и MDPIT путем метаанализа была выделена подгруппа больных с АГ. В этой подгруппе (более 5000 чел.) многомесячный прием верапамила или дилтиазема у лиц после инфаркта без сердечной недостаточности (СН) улучшал прогноз [25].
Таким образом, рекомендации по долгосрочному использованию АК у больных с АГ в настоящее время затруднительны. Считается, что наиболее безопасны верапамил и дилтиазем. Кроме того, могут применяться длительно действующие препараты дигидропиридинового ряда. Лечение АГ следует начинать с бета-адреноблокаторов, ИАПФ, салуретиков и их комбинаций. АК в качестве монотерапии или в виде комбинаций могут быть присоединены в случае недостаточной эффективности указанных средств. Короткодействующую форму нифедипина можно использовать для купирования гипертонического криза и для лечения АГ в дозах не более 40 мг/сут в качестве временной терапии, если нет других способов эффективного контроля АД [1].
Сердечная недостаточность. По мере развития ультразвуковых методов исследования и экспериментальной кардиологии в практической медицине все прочнее утверждались понятия систолической и диастолической дисфункции сердца. Под сердечной недостаточностью в зарубежной литературе понимают систолическую дисфункцию левого желудочка с клиническими признаками. Диастолическую дисфункцию определяют как неполноту или нарушение расслабления миокарда, изменения тонуса миокарда в диастолу. Диастолическая дисфункция, как правило, предшествует систолической у больных АГ, гипертрофической кардиомиопатией, многими формами ИБС. При систолической дисфункции заметно снижается ФВ левого желудочка.
Теоретически АК должны вызывать благоприятный эффект при обоих видах дисфункций. Одним из главных патогенетических моментов диастолической дисфункции является так называемая кальциевая контрактура миокарда. При этом состоянии из-за перегрузки миокардиоцитов кальцием последние не могут полностью расслабиться, что нарушает процесс расслабления (диастолы) целостного миокарда. АК потенциально должны быть полезными при этом виде дисфункции.
Работа сердца облегчается также при уменьшении пред- и постнагрузки. Именно такой эффект обусловливают АК. В терапевтических концентрациях АК (за исключением верапамила и дилтиазема) практически не обладают отрицательным инотропным действием и вызывают коронародилатирующий эффект.
Некоторые АК показаны для лечения диастолической дисфункции, но ни один АК достоверно не улучшает течение и прогноз при систолической дисфункции и СН.
Диастолическая дисфункция.В развитии этого патологического состояния, помимо нарушения тока ионов через кальциевые каналы мембран клеток миокарда, большую роль играет длительность диастолы. При тахикардии, когда имеется укорочение диастолы, дисфункция миокарда развивается гораздо чаще. Вероятно, поэтому у больных с диастолической дисфункцией эффективен верапамил. Верапамил (и в меньшей степени дилтиазем) оказывал наиболее благоприятное влияние на диастолические параметры [21].
Гипертрофическая кардиомиопатия, при которой диастолическая дисфункция миокарда является ранним и обязательным признаком, особенно эффективно лечится верапамилом в комбинации с бета-адреноблокаторами [18]. Дилтиазем оказывает хорошее действие при дилатационной кардиомиопатии [12]. Эффективной комбинацией для лечения пожилых больных с диастолической дисфункцией, обусловленной АГ, считается верапамил + тиазидные диуретики [23]. АК дигидропиридинового ряда (нисолдипин, нифедипин) достаточного эффекта при диастолической дисфункции не вызывают [21].
Систолическая дисфункция.Верапамил и дилтиазем обладают отрицательным инотропным действием. Их непригодность в терапии СН была продемонстрирована в трех больших работах. Дилтиазем применялся у больных после инфаркта миокарда с ФВ менее 40% в виде монотерапии. По сравнению с аналогичными больными, получавшими плацебо, отмечено увеличение летальности [27].
В другом исследовании дилтиазем совместно с диуретиками, ИАПФ и дигоксином использовался у больных дилатационной кардкомиопатией, осложненной СН. Контролем служили больные, получавшие вышеназванный комплекс без дилтиазема. Через два года в основной группе умерло 12% больных, в контрольной — 17% (различие недостоверно). Таким образом, несмотря на комбинированную терапию, дилтиазем не оказывал существенного влияния на исход болезни [12].
В исследовании DAVIT—II верапамил применялся у больных после инфаркта миокарда в течение 18 мес. В подгруппе с дисфункцией левого желудочка (ФВ менее 40%) верапамил заметно не влиял на выживаемость [38].
После этого внимание исследователей в лечении СН переключилось на АК дигидропиридинового ряда, которые не обладают отрицательным инотропным эффектом. Однако нифедипин в виде монотерапии ухудшал течение СН, а в комбинации с изосорбида динитратом не повышал выживаемость больных [9].
Фелодипин (вазоселективный препарат) в пролонгированной форме назначался 451 пациенту с СН в дозе 2,5—5 мг дважды в сутки. Исходно больные получали эналаприл, петлевые диуретики, некоторые пациенты принимали дигоксин. Добавление фелодипина не повышало выживаемость больных [3].
Определенные надежды возлагались на работу, в которой оценивалась эффективность амлодипина у больных с выраженной СН (ФВ в среднем 21%). Амлодипин считается элитным препаратом — он высокоселективен по отношению к сосудистой стенке, не влияет на состояние сердечной мышцы, обладает большим периодом полувыведения, что позволяет создавать устойчивые концентрации. Исследование проводилось среди 1153 больных на протяжении 14 мес. Больные были рандомизированы по этиологическому признаку: ИБС или неишемические поражения миокарда. Предполагалось, что амлодипин будет особенно эффективен у больных ИБС. За время исследования в группе контроля умерло 38% пациентов, в основной группе — 33% (Р=0,07). Таким образом, было достигнуто уменьшение риска общей смертности на 16%, но это уменьшение не было статистически значимым. Отмечен парадоксальный факт, что в подгруппе неишемических поражений сердца амлодипин уменьшил смертность на 46%.
Таким образом, амлодипин проявил неожиданную эффективность улиц без ИБС. Это послужило основанием для начала нового исследования PRAISE—II: амлодипин у больных дилатационной кардиомиопатией [29].
Амлодипин не влиял на частоту обострений СН, требующих госпитализации, и на частоту развития ИМ. Среди больных, получающих амлодипин, чаще встречались отеки ног, острая левожелудочковая недостаточность, почечная недостаточность.
В настоящее время проводится крупное (2400 больных) исследование по оценке АК 6-й категории — мибефрадила [22]. Это препарат с необычными фармакологическими свойствами.
Несмотря на системную вазодилатацию и антиишемические свойства, ни один АК не продемонстрировал способности существенно улучшать течение и прогноз у больных СН как в виде монотерапии, так и в комбинациях. Возможно, амлодипин может применяться при лечении СН, что требует дальнейшего изучения. Отрицательные результаты лечения СН были зарегистрированы в первую очередь у больных, которые не принимали ИАПФ. Предполагается, что совместное применение некоторых АК с ИАПФ может улучшать прогноз [17].
Первичная легочная гипертензия.Это редкая патология с быстронарастающей СН по правожелудочковому типу. С момента установления диагноза средняя продолжительность жизни составляет около трех лет. Назначение АК в очень высоких дозах (нифедипин до 240 мг/сут или дилтиазем до 720 мг/сут) на 25% снижает давление в легочной артерии и улучшает показатели выживаемости [6, 34].
Синдром Рейно.АК эффективны при болезни и синдроме Рейно. Чаще других применяют нифедипин в дозе 30—60 мг/ сут, что уменьшает частоту и выраженность спастических приступов у 30—90% больных. Замечено, что эффективность терапии выше при первичном феномене (болезни) Рейно по сравнению с аутоиммунными заболеваниями и вторичным синдромом Рейно [5, 20].
Таким образом, лекарственные препараты группы АК сегодня достаточно широко применяются для лечения различных заболеваний сердечно-сосудистой системы. Их с успехом назначают при аритмиях, ИБС, АГ и других патологических состояниях. Рекомендации по клиническому применению АК представлены в табл. 4.
Таблица 4. Рекомендации по клиническому применению антагонистов кальция
|
Патология |
Препараты выбора |
|
Аритмии |
Верапамил и дилтиазем замедляют сердечный ритм и атриовентрикулярную проводимость. Применяются при фибрилляции предсердий, наджелудочковой пароксизмальной тахикардии и других наджелудочковых тахиаритмиях. |
|
Стабильная стенокардия |
Монотерапия АК показана главным образом при вазоспастической стенокардии. При других видах целесообразна комбинация с бета-адреноблокаторами или нитратами. |
|
Безболевая ишемия миокарда |
АК подавляют ишемические изменения на ЭКГ. Применяются пролонгированные формы дигидропиридиновых производных, верапамил или дилтиазем в комбинации с бета-блокаторами или нитратами. |
|
Нестабильная стенокардия |
Верапамил или дилтиазем. Дигидропиридиновые производные используются только в комбинации с бета-адреноблокаторами. |
|
Инфаркт миокарда |
В остром периоде АК относительно противопоказаны. Верапамил или дилтиазем могут назначаться с подострого периода у больных без систолической дисфункции левого желудочка. |
|
Диастолическая дисфункция |
Верапамил улучшает параметры диастолы. Препараты ди-гидропиридинового ряда неэффективны. |
|
Систолическая дисфункция |
АК не являются препаратами первого ряда при систолической дисфункции. При наличии специфических показаний могут применяться в комбинации с ИАПФ, сердечными гликозидами, диуретиками. |
До сегодняшнего дня, несмотря на многочисленные, в том числе кооперативные международные исследования, нет полной ясности относительно безопасности применения антагонистов кальция у больных нестабильной стенокардией, инфарктом миокарда и артериальной гипертензией. Большинство исследователей весьма сдержанно относятся к широкому использованию дигидропиридиновых производных короткого действия. Следует учитывать показания и противопоказания к применению данной группы лекарственных средств и в каждом случае использовать дифференцированный подход к выбору оптимального препарата. Антагонисты кальция, назначенные по показаниям, могут вызвать терапевтический эффект. Применение их без достаточных оснований во многих случаях неблагоприятно сказывается на исходе болезни и влияет на продолжительность жизни пациента.
ЛИТЕРАТУРА
1. Современная концепция применения антагонистов кальция в кардиологии: Решение ученого Совета НИИ кардиологии им. А. Л. Мясникова КНЦ РАМН // Клин. медицина. – 1996. – № 4. – С. 70–71.
2. Belhassen В., Shapiro J., Pelleg A. et al. //Amer. Heart J. – 1984. – V. 108. – P. 1034–1037.
3. Cohn J. N., Ziesche S. M., Smith R. et al. // Circulation. – 1997.–V. 96.–P. 856–863.
4.Conti C.R. //Amer. J. Cardiol. – 1996. – V. 78, snppl. 9A. – P 13–18.
5.Corbin D. О. С., Wood D. A., Macintyre С. C. A., Hously E. //Eur. Heart J. – 1986. –V. 7. – P. 165–170.
6.D’Alonzo G. E., BamR. J., Ayers S. M. et al. //Ann. Intern. Med. – 1991. –V. 115. – P. 343–347.
7.Dargie H. J., Ford I., Fox К. M. // Eur. Heart J. – 1996. – V. l.–P. 104–112.
8.Deedwania P. C, Carbajal E. V., Nelson J. R., Halt H. //Amer. Coll. Cardiol. – 1991. – V. 17. – P. 963–969.
9.Elkayam U., Amin I., Mehra A. et al. // Circulation. – 1990. – V. 82. – P. 1954–1961.
10.Ellenbogen K. A., Dias V. C., Plumb V. I. et al. //Amer. J. Coll. Cardiol. – 1991. –V. 18. – P. 891–897.
11.Ferguson I. J., Momomura S. // Circulation. – 1994. – V. 90. –P. 2194–2196.
12.Figulla H. R., Gietzen F., Zeymer U. et al. // Circulation. – 1996. – V. 94. – P. 346–352.
13.Fisher M., GrottaJ. // Drugs. – 1994. – V.47. – P. 331–336.
14.Fleckenstein A., Tritthard H., Fleckenstein B. et al. // Pflugers Arch. Physiol. – 1969. – V. 307. – P. 25.
15.Frishman W.. Charlap S., Kimmel B. et al. // Circulation. – 1988.–V. 77.–P. 774–786.
16. Furberg C. D., Psaty В. M., Meyer I. V. // Circulation. – 1995.–V. 92.– P. 1326–1331.
17.Gheorghiade M., Benatz D., Konstam M.A. et al. //Amer. J. Cardiol. – 1997. – V. 80, Suppl. 8B. – P. 14H–27H.
18.GouserM., Vetter K., NoakF.// Lancet. – 1995. – V. 345. –P. 1304–1309.
19.Hjemdahl P., Eriksson S. V., Held K., Rehnqvist N. //Amer. J. Cardiol. – 1996. –V. 77. – P. 6D–15D.
20.Kiowsky W., Erne P., Buhler F. R. //Cardiovasc. Drugs Ther. – 1990. – V. 4. – P. 935–940.
21.Lahiri A., Rodrigues E. A., Carbony G. P.. Raftery E. B. // Circulation. – 1996. – V. 27. – P. 426–432.
22.Levine Т. B. // Clin. Cardiol. – 1997. – V. 20. – P. 320–326.
23.Luscher T. F, Wenzel R. R., Noll L. // Deutch. Med. Wochenschr. – 1996. – Bd 126. – S. 532–536.
24.Mc Clellan T. // Inpharma Wkly. – 1994. – V. 932. – P.4.
25.Messerli F. H., Boden W. E., Fisher N. J., Schechtman К. B. //J. Amer. Coll. Cardiol. – 1996. – V. 7. – P. 178A.
26.MesserliF. H. //Amer. J. Cardiol. – 1996. – V. 78, suppl. 9A. – P. 19–23.
27.Multicenter Diltiazem Postinfarction Trial Research Group. The effect of diltiazem on mortality and reinfarction after myocardial infarction // N. Engl. J. Med. – 1988. – V. 319. – P. 385–392.
28.Myocardial Protection by Calcium Antagonists / Ed. L. H.Opie. – New York: Author’s Publ. House, 1994. – 195p.
29.Packer M., O’Connor С. M., Ghali I. K. et al. // N. Engl. J. Med. – 1996.–V. 335.– P. 1107–1114.
30.Pahor M., Guralnik I. M., Corti M. C. et al. // J. Amer. Geriatr. Soc. – 1995. –V. 43.–P. 1191–1197.
31.Psaty В. M., Heckbert S. R., Koepsell T. D. et al. // JAMA. –1995.–V. 274. –P. 620–625.
32.Rehnqvist N., Hjemdahl P., Billing E. et al. //Eur. Heart J. – 1996. – V. 17. – P. 76–81.
33.Report of the Holland Interuniversity Nifedipine / Metoprolol Trial (HINT) Reseach Group. Early treatment of unstable angina in the coronary unit: a randomised, double–blind, placebo–controlled comparison of reccurcnt ischemia in patients treated with nifedipine or metoprolol or both // Brit.Heart J.– 1986. – V. 56. – P. 400–413.
34.Rich S. // Amer. J. Cardiol. – 1995. – V. 75, suppl. – P. 63A–66A.
35.Rogers W. J., Bourassa M. G., Andrews Т. C. et al. //J. Amer. Coll. Cardiol. – 1995. – V. 26. – P. 594–605.
36.The Israeli SPRINT Study Group. Secondary Prevention Reinfarction Israeli Nifedipine Trial (SPRINT). A randomised interventional trial of nifedipine in patients with acute myocardial infarction // Eur. Heart J. – 1988. – V. 9. – P. 354– 364.
37.Tzivoni D., Braun S., Shelling A., Kobrin I. //J. Amer. Coll. Cardiol. – 1996. – V. 27, suppl. A. – P. 185A.
38.Yusuf S., Held P., Furberg C. D. // Amer. J. Cardiol – 1991. – V. 67.–P.1295–1297.
39.Zaunad F., Sadoul N. // J. Cardiovasc. Pharmacol. – 1990.– V. 16, suppl. – S. 16, 19.
Медицинские новости. – 1998. – №11. – С. 3-10.
Внимание! Статья адресована врачам-специалистам. Перепечатка данной статьи или её фрагментов в Интернете без гиперссылки на первоисточник рассматривается как нарушение авторских прав.